题目内容
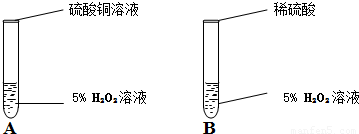
在一次实验室分组实验中,李武同学不小心把硫酸铜溶液(CuSO4固体溶于水形成的混合物)滴加到盛有5%H2O2溶液的试管中,立即产生大量的气泡.硫酸铜溶液中含有三种微粒( H2O、Cu2+、SO42- ),他想知道硫酸铜溶液中的哪一种微粒能使双氧水分解的速率加快.他和同学一起通过以下实验完成这次探究活动,并填写空白.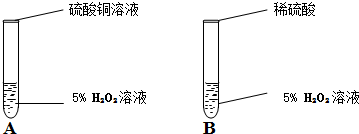
(1)你认为最不可能的是哪一种微粒?
(2)用化学式表示实验A发生的化学反应
(3)在实验B中加入稀硫酸(含有H2O、H+、SO42-)后,无明显变化,证明
结论:硫酸铜溶液中,加快双氧水分解速率的微粒是
(4)要验证双氧水分解速率与双氧水的浓度有关,可以进行以下实验:取两套相同装置,其中一套加入5%的双氧水溶液和MnO2,你认为另一套装置所加药品应该是
a.15%的双氧水溶液 b.MnO2 c.5%的双氧水溶液 d.硫酸铜溶液
(5)小东同学注意到试管内只有15%的双氧水时就有少量小气泡浮起,将这支试管浸入约80°C的热水中,气泡明显增多,由此小东认为,双氧水分解速率还与

(1)你认为最不可能的是哪一种微粒?
H2O(或水分子)
H2O(或水分子)
.理由是双氧水溶液中含有水分子
双氧水溶液中含有水分子
.(2)用化学式表示实验A发生的化学反应
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
,检验该反应产生气体的方法是
| ||
用带火星的木条伸入到试管A中,木条复燃,证明是氧气
用带火星的木条伸入到试管A中,木条复燃,证明是氧气
.(3)在实验B中加入稀硫酸(含有H2O、H+、SO42-)后,无明显变化,证明
SO42-(或硫酸根离子)
SO42-(或硫酸根离子)
不起催化作用.结论:硫酸铜溶液中,加快双氧水分解速率的微粒是
Cu2+(或铜离子)
Cu2+(或铜离子)
.(4)要验证双氧水分解速率与双氧水的浓度有关,可以进行以下实验:取两套相同装置,其中一套加入5%的双氧水溶液和MnO2,你认为另一套装置所加药品应该是
a
a
和b
b
(填序号).a.15%的双氧水溶液 b.MnO2 c.5%的双氧水溶液 d.硫酸铜溶液
(5)小东同学注意到试管内只有15%的双氧水时就有少量小气泡浮起,将这支试管浸入约80°C的热水中,气泡明显增多,由此小东认为,双氧水分解速率还与
温度
温度
有关.分析:(1)根据双氧水中本身含有水考虑;
(2)根据双氧水分解的反应原理以及氧气的助燃性考虑;
(3)根据硫酸中含有的微粒考虑;
(4)根据实验目的考虑;
(5)根据试管内只有15%的双氧水时有少量小气泡浮起,将这支试管浸入约80°C的热水中,气泡明显增多,分析解答.
(2)根据双氧水分解的反应原理以及氧气的助燃性考虑;
(3)根据硫酸中含有的微粒考虑;
(4)根据实验目的考虑;
(5)根据试管内只有15%的双氧水时有少量小气泡浮起,将这支试管浸入约80°C的热水中,气泡明显增多,分析解答.
解答:解:(1)双氧水是水溶液,一定含有水,但分解速率慢,所以水分子不会是催化剂;
(2)氧气有助燃性,检验氧气可用带火星的小木条伸入试管,木条复燃,证明是氧气;
(3)因为稀硫酸中含有三种粒子(H2O、SO42-、H+)且硫酸不能加快过氧化氢分解的速度,所以硫酸根离子不能使过氧化氢分解的速度加快;根据上面的分析可知水分子、硫酸根离子不能使过氧化氢分解速度加快,所以是铜离子使双氧水分解的速率加快;
(4)要验证双氧水分解速率与双氧水的浓度有关,可以进行以下实验:取两套相同装置,其中一套加入5%的双氧水溶液和MnO2,则另一套装置所加药品应该是浓度不同的双氧水溶液和MnO2;
(5)试管内只有15%的双氧水时有少量小气泡浮起,将这支试管浸入约80°C的热水中,气泡明显增多,说明双氧水分解速率还与温度有关;
故答案为:
(1)H2O(或水分子);双氧水溶液中含有水分子;
(2)2H2O2
2H2O+O2↑;用带火星的木条伸入到试管A中,木条复燃,证明是氧气;
(3)SO42-(或硫酸根离子);Cu2+(或铜离子);
(4)a;b;
(5)温度.
(2)氧气有助燃性,检验氧气可用带火星的小木条伸入试管,木条复燃,证明是氧气;
(3)因为稀硫酸中含有三种粒子(H2O、SO42-、H+)且硫酸不能加快过氧化氢分解的速度,所以硫酸根离子不能使过氧化氢分解的速度加快;根据上面的分析可知水分子、硫酸根离子不能使过氧化氢分解速度加快,所以是铜离子使双氧水分解的速率加快;
(4)要验证双氧水分解速率与双氧水的浓度有关,可以进行以下实验:取两套相同装置,其中一套加入5%的双氧水溶液和MnO2,则另一套装置所加药品应该是浓度不同的双氧水溶液和MnO2;
(5)试管内只有15%的双氧水时有少量小气泡浮起,将这支试管浸入约80°C的热水中,气泡明显增多,说明双氧水分解速率还与温度有关;
故答案为:
(1)H2O(或水分子);双氧水溶液中含有水分子;
(2)2H2O2
| ||
(3)SO42-(或硫酸根离子);Cu2+(或铜离子);
(4)a;b;
(5)温度.
点评:本题考查了学生掌握双氧水分解的反应原理、催化剂的性质、氧气的性质等知识,并根据题意分析和解决问题的能力.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目