网址:http://m.1010jiajiao.com/timu_id_6741[举报]
(一)选择题
1.B 2.D 3.B、D 4.A 5.B、D 6.C 7.B 8.C 9.D 10.C 11.2, 11.A 12.B 13.B 14.B 15.C 16.D 17.A 18.A
(二)非选择题
1.MgH2,酸足量时△1=,酸不足时 Δ1=A-1。AlH2,碱足量时Δ2=,碱不足时Δ2=B-3.
①酸碱均过量时,要使天平平衡需Δ1=Δ2,有的关系,取值范围0<A<12是对的。0<B<27是不对的,因为产生等量H2时 耗Al量比Mg少,故应由B==12.3 75,得0<B<12.375.②酸碱均不足时,并非A=B>12,应是A-1=B-3,即A=B-2,这是关 键,取值范围B>27,A>25而无上限(只需符合A=B-2)。③酸对Mg不足,碱对Al有余时,应为A-1=。取值范围怎样?酸对Mg不足,当然需A>12,这时B应由A-1=算式而定,将A>12代入知B>12.375,故B的取值范围为27>B>1 2.375.而Mg是否为27>A>12?不是的。当B<27时,A应由=A-1决 定,即=A-1得A=25,令B<27,则A<25,A的取值范围为12<A<25。④酸对Mg有余,碱对Al不足时,应有=B-3,而A<12,B>27,可见这种情况是不可能的。
2.(1)80% (2)40%
3.(1)因为在10℃、40℃、75℃时剩余固体量依次减少,所以说明10℃和40℃时溶液一定是 饱和的。
设加入的水为x.
(104-81)∶100=(201-132)∶x,解得x=300 g
(2)在75℃时,混合物中硝酸钠是否全部溶解了?设40℃到70℃时,在300g水中又溶解了y g 硝酸钠。
(150-104)∶100=y∶300,解得y=138 g>(132-72) g
说明硝酸钠在70℃之前就已全部溶解了。
设10℃时300 g水中溶解了z g硝酸钠。
81∶100=z∶300, z=243 g
从10℃到75℃又溶解的硝酸钠:201-72=129(g)
混合物中总共含硝酸钠:243+129=372(g)。
(3)设t℃时硝酸钠恰好溶解在300 g水中,此时硝酸钠的溶解度为S g。
S∶100=372∶300, S=124 g
查硝酸钠溶解度表可得温度为60℃。故完全溶解混合物中硝酸钠所需最低温度为60℃。
4.(1)20 (2)50
5.(1)0.15 mol (2)141.4 g (3)7
6.(1)20% (2)3.93 mol/L (3)4.27 mol
7.有关反应的化学方程式:Zn+FeCl2Fe+ZnCl2
Zn+CuCl2Cu+ZnCl2
(1)根据溶液Cl-的物质的量和反应前后固体的质量变化两关系可求得Fe2+和Cu2+的量。
设FeCl2 x mol,CuCl2y mol,则有
解得:x=,
则[Cu2+]=,
[Fe2+]=。
(2)由于x+y=0.2a mol,且b g Zn粉为过量,则b≥0.2a?65 g,即b≥13a g。
(3)在Cl-的总量一定的情况下,溶液中Cu2+和Fe2+总量也一定,消耗的Zn的总量也不变,所以滤液c的质量越大,则生成的Cu越多,原溶液中CuCl2的含量越大;当原溶液中只含CuCl2时,滤渣c的质量最大。
即Fe2+=0,有b-0.2a-c=0,c=b-0.2a。
8.40.4% (12)n=1 9.(1)2,5
W、W(H2O)
W、W(Cu)
W、V(H2)
W(H2O)、W(Cu)
W(Cu)、V(H2)
(2)
10.(1)1cm3中阴、阳离子总数=()3
1cm3中Ni2+―O2-离子对数=()3×
密度=
(2)解法Ⅰ:设1 mol中含Ni3+x mol, Ni2+(0.97-x)mol。
根据电中性 3x mol +2(0.97-x)mol=2×1 mol ∴x=0.06
Ni2+为(0.97-x)mol=0.91 mol
离子数之比 Ni3+:Ni2+=0.06∶0.91=6∶91
11.(1)M(OH)2+2NaHCO3=MCO3↓+Na2CO3+2H2O (2)②
(3)M的相对原子质量为137,NaHCO3的质量58.8 g
12.(1)2CaO2CaO+O2 (2)80.0% (3)
13.(1)要求由质量、摩尔质量以及体积、浓度分别列出酸和碱的物质的量,再根据中和反应中酸碱物质的量关系列式求得碱的浓度。
∵
∴
(2)在上题求得的基础上,同样利用酸碱中和反应,求得食醋稀释液中CH3COO H的物质的量,经换算后得出C3COOH%的表示式。
∵
∵CH3COOH%=
与第(1)题相比,由于需要经过换算以及正确理解CH3COOH%的含义,所以难度略有上升。
(3)要求学生能迅速接受并理解试题给出的两个信息,据此做出判断。这两条信息是:①由第(1)上题得知,KHC8H4O4可以进一步与NaOH发生中和反应,说明KHC8H4O4溶 液呈酸性(从指示剂颜色变化可知,它与NaHCO3不同,NaHCO3是呈弱碱性的)。②0.1mol /L邻苯二甲酸(H2C8H4O4)溶液的pH大于1,说明溶液的浓度大于电离出的,证明这是弱酸,既然是弱酸,当它完全中和后生成的正盐溶液应呈弱碱性(强碱弱酸盐 水解,溶液呈弱碱性),所以,邻苯二甲酸和KOH溶液混合后,若pH=7,说明邻苯二甲酸和第 一步中和反应(生成KHC8H4O4)已完全,即>1,但第 二步中和反应(KHC8H4O4K2C8H4O4)尚不完全,即<2,现在酸和碱的体积相同,所以在1 ~2之间,即2>x>1,答案为C。
14.(1)SO2+CaCO3+O2+2H2OCaSO4?2H2O+CO 2
SO2+Ca(OH)2+O2+H2OCaSO4?2H2O
(2)=10000×0.0015×24=360(m3)=3.6×105(dm3)
=15276.86(mol)
=15267.86×100=1526786(g)=1.53×103(kg)
(3)=15267.86×172=2626071.92(g)=2.63×103
15.(1)OH-向右移动 Na+向左移动
(2)0.3C 0.3C
(3)2H2O2H2+O2?
(4)电,化学,内,Iεt-I2(R+r)t
(5)(1)0.062(6.2%);4.75mol
(6)19mol
 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:(1)一定温度下,在一个固定容积的密闭容器中,可逆反应 A(g)+2B(g)=4C (g)△H>0 达到平衡时,c(A)=2mol?L-1,c(B)=7mol?L-1,c(C)=4mol?L-1.试确定B的起始浓度c(B)的取值范围是
A.增加C的物质的量 B.加压 C.升温 D.使用催化剂
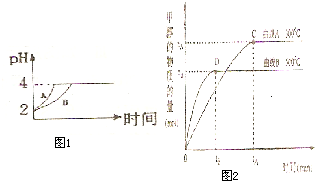
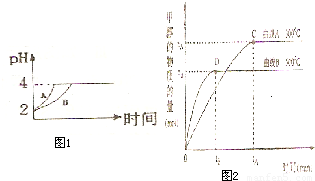
(2)常温下,取 pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图1所示.则图中表示醋酸溶液中pH变化曲线的是
(3)在体积为3L的密闭容器中,CO与H2在一定条件下反应生成甲醇:CO(g)+2H2(g)→CH3OH(g).反应达到平衡时,平衡常数表达式K=
| c(CH3OH) |
| c(CO)×c2(H2) |
| c(CH3OH) |
| c(CO)×c2(H2) |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
(4)难溶电解质在水溶液中存在着电离平衡.在常温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数.例如:
Cu(OH)2(s)=Cu2+(aq)+2OH-(aq),Ksp=c(Cu2+)[c(OH-)]2=2×10-20
当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.若某CuSO4溶液里c( Cu2+)=0.02mol?L-1,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于
(5)常温下,某纯碱(Na2CO3) 溶液中滴入酚酞,溶液呈红色.则该溶液呈
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b 的值
③实验4,若900℃时,在此容器中加入10molCO,5molH2O,2molCO2,5molH2,则此时V正
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO (g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
③H2O(g)=H2O(l)△H=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(4)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9.CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol/L,则生成沉淀所需CaCl2溶液的最小浓度为
(5)甲醇可制作燃料电池.写出以稀硫酸为电解质溶液的甲醇燃料电池负极反应式
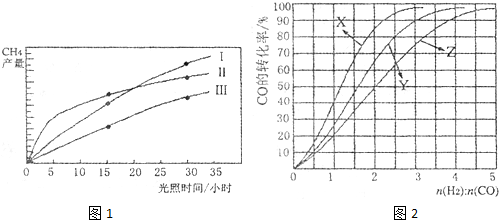
(1)在O?30小时内,CH4的平均生成速率v(Ⅰ)、v(Ⅱ)和v(Ⅲ)由大到小的顺序为
(2)将所得CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g)?CO(g)+3H2(g);△H=+206kJ.mol-1.将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,此时测得CO的物质的量为O.10mol,CH4的平衡转化率为91%,则此温度下该反应的平衡常数为
(3)该反应产生的CO和H2可用来合成可再生能源甲醇,已知CO(g)、CH3OH(l)的燃烧热△H分别为-283.0kJ?mol-1和-726.5kJ?mol-1,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为
(4)工业上常利用反应CO(g)+2H2(g)?CH3OH(g),△H<0合成甲醇,在230℃?270℃最为有利.为研究合成气最合适的起始组成比n(H2):n(CO),分别在230℃、250℃和270℃进行实验,结果如图2.
①270℃的实验结果所对应的曲线是
②230℃时,工业生产适宜釆用的合成气组成n(H2):n(CO)的比值范围是
A.1?1.5 B.2.5?3 C.3.5?4.5
(5)某同学以石墨为电极,以KOH溶液为电解质设计甲醇燃料电池,其负极的电极反应式为
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应 A(g)+2B(g)=4C (g)△H>0 达到平衡时,c(A)=2mol?L-1,c(B)=7mol?L-1,c(C)=4mol?L-1.试确定B的起始浓度c(B)的取值范围是______;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是______.
A.增加C的物质的量 B.加压 C.升温 D.使用催化剂
(2)常温下,取 pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图1所示.则图中表示醋酸溶液中pH变化曲线的是______ ( 填“A”或“B”). 设盐酸中加入的Zn质量为m1,醋酸溶液中加人的Zn质量为 m2. 则 m1______ m2 ( 选填“<”、“=”、“>”)
(3)在体积为3L的密闭容器中,CO与H2在一定条件下反应生成甲醇:CO(g)+2H2(g)→CH3OH(g).反应达到平衡时,平衡常数表达式K=______,升高温度,K值______(填“增大”、“减小”或“不变”).在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=______.
(4)难溶电解质在水溶液中存在着电离平衡.在常温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数.例如:
Cu(OH)2(s)=Cu2+(aq)+2OH-(aq),Ksp=c(Cu2+)[c(OH-)]2=2×10-20
当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.若某CuSO4溶液里c( Cu2+)=0.02mol?L-1,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于______; 要使0.2mol?L-1的CuSO4 溶液中Cu2+沉淀较为完全 (使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH值为______.
(5)常温下,某纯碱(Na2CO3) 溶液中滴入酚酞,溶液呈红色.则该溶液呈______性.在分析该溶液遇酚酞呈红色原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH 所致;乙同学认为是溶液中Na2CO3电离出的CO32-水解所致.请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论)______.
 查看习题详情和答案>>
查看习题详情和答案>>
 (2012?枣庄二模)碳和碳的化合物在人类生产、生活中的应用非常广泛,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
(2012?枣庄二模)碳和碳的化合物在人类生产、生活中的应用非常广泛,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.(1)化学与以节能减排为基础的低碳经济密切相关.下列做法违背发展低碳经济的是
A.提高原子利用率,发展绿色化学
B.大力发展汽车产业,鼓励市民购买家用汽车
C.推广煤的气化、液化技术,提供清洁高效燃料
D.开发利用太阳能、风能、氢能、核能等能源
(2)在载人航天器的生态系统中,不仅要求分离除去CO2,还要求提供充足的O2.某种电化学装置可实现如下转化:2CO2═2CO+O2,CO可用作燃料.已知该反应的阳极反应式为:4OH--4e-→O2↑+2H2O,则阴极反应式为
(3)CO2可转化成有机物实现碳循环.在体积为lL的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1,
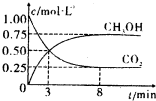
则得CO2和CH2OH(g)的浓度随时间变化如图所示.
①从3min到8min,v(H2)=
②能说明上述反应达到平衡状态的是
A.反应中CO2与CH2OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时闻的变化而变化
C.单位时间内每消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(4)已知:
①C(s)+O2(g)═CO2(g),△H1=-437.3kJ?mol-1
②2H2(g)+O2(g)═2H2O(g),△H2=-571.6kJ?mol-1
③2CO(g)+O2(g)═2CO2(g),△H3=-566.0kJ?mol-1
则:C(s)+H2O(g)═CO(g)+H2(g),△H=
(5)某文献报道:在30℃、30MPa条件下,以Fe、COCl2作催化剂,CO2和H2反应生成丁烷和戊烷.假定在一容器中充入一定量的CO2和H2,加入催化剂,若CO2和H2的转化率均为100%,产物只有丁烷和戊烷,
| n(H2) | n(CO2) |