网址:http://m.1010jiajiao.com/timu_id_67188[举报]
1B
3D
5D
10BC
12AD
13BD
14BC
15.(12分)(1)x=1.5 (2)c(3)2Na2CO4=2Na2CO3+O2↑
(4)2CO42-+4H+=2CO2↑+O2↑+H2O
(5)g→h→e→f→d→c→b,
16.(8分)(1)CO(NH2)2 (2)AlO2-+CO2+H2O==Al(OH)3↓+HCO3-
(3)2Al2O3+2N2+
(4)CO2在水中的溶解度远小于NH3,若先通入CO2,则反应③中K的产率很低
17.(12分)(1)①(1分) (2)①②⑤(2分)
NO+NO2+2NaOH=2NaNO2+H2O(1分) 88.5%(2分)
(3)4FeS2+15O2+2H2O 2Fe2(SO4)3+2H2SO4(2分)
2Fe2(SO4)3+2H2SO4(2分)
Cu2S+10Fe3++4H2O 2Cu2++10Fe2++8H++SO42-(2分)
2Cu2++10Fe2++8H++SO42-(2分)
(4)3NO=N2O十NO2(1分),由于2NO2 N2O4,即生成的NO2又双聚成N2O4,导致气体分子数减少,使其压强路小于1.01×107 Pa的2/3(1分)
N2O4,即生成的NO2又双聚成N2O4,导致气体分子数减少,使其压强路小于1.01×107 Pa的2/3(1分)
18.(10分)(1)ABEF(2分)
(2)c(SO42-)>c(Fe2+)>c(H+)>c(OH-) (2分)
(3)硫酸作用Fe2+抑制的水解,铁皮的作用防止Fe3+的氧化。(2分,各1分)
(4)在试管中取滤液少许,加入足量的NaOH溶液,加热,用湿润的红色石蕊试纸检验,若试纸变兰色,则证明滤液中含有NH4+。(2分)
(5)FeSO4+2NH4HCO3 →FeCO3↓+( NH4)2 SO4+ CO2↑+H2O(2分)
19. (12分)(1)F: I:  (2分)(2)加成、消去 (2分)
(2分)(2)加成、消去 (2分)
 |
(3) (2分) 2(1分)
(4)4 (2分)
(5)
 |
(3分
20(8分)(1)Cu+2H++H2O2==Cu2++2H2O (2分) (2) 淀粉溶液为指示剂,当最后一滴Na2S2O3溶液滴入时,溶液蓝色褪去。(2分)
(3)n(Cu)=1/2n(I2) = n(S2O32-)=6.45×0.01100=0.07095mmol
ωCu=0.07095×10-3×64×250.00/50.00/1.1=0.02064(4分)
21.(10分)(5)2分,其它每空1分
(1)Ar (2)极性 (3)5 1 (4)D是CH3OH,分子之间能形成氢键
(5)CO中第一个π键的键能是273kJ/mol,N2中第一个π键的键能是523.3kJ/mol,所以CO的第一个键比N2更容易断。
(6)1s22s22p63s23p6 3d104s1
(7)分子晶体
www.ks5u.com
 Ⅰ高纯MnCO3是制备高性能磁性材料的主要原料.
Ⅰ高纯MnCO3是制备高性能磁性材料的主要原料.实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:
在烧瓶中(装置见右图)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h.停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO3=MnSO4+H2O).
①石灰乳作用
②若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图.导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是

(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7,请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH].
①
Ⅱ锌铝合金的主要成分有Zn、Al、Cu、Si等元素.实验室测定其中Cu含量的步骤如下:
①称取该合金样品1.1g,用HCl和H2O2溶解后,煮沸除去过量H2O2,过滤,滤液定容于
250mL容量瓶中.
②用移液管移取50.00mL滤液于250mL碘量瓶中,控制溶液的pH=3~4,加入过量KI溶液(生成CuI和I2)和指示剂,
用0.01100mol?L-1Na2S2O3溶液滴定生成的I2至终点(反应:I2+2S2O32-=2I-+S4O62-),消耗Na2S2O3溶液6.45mL.
(1)判断步骤②滴定终点的方法是
(2)计算合金中Cu的质量分数
Ⅰ、高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:在烧瓶中(装置见图)加入一定量MnO2 和水,搅拌,通入 SO2和N2混合气体,反应3h。停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO3=MnSO4+H2O)。
①石灰乳作用: 。
②若实验中将 换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是 。
换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是 。
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH="7.7," 请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤:
[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH]。
① ;
② ;
③检验SO42-是否被洗涤除去; ④用少量乙醇洗涤; ⑤低于100℃干燥。
Ⅱ、锌铝合金的主要成分有Zn、Al、Cu、Si等元素。实验室测定其中Cu含量的步骤如下:①称取该合金样品1.1g,用HCl和H2O2溶解后,煮沸除去过量H2O2,过滤,滤液定容于250mL容量瓶中。
②用移液管移取50.00mL滤液于250mL碘量瓶中,控制溶液的pH=3~4,加入过量KI溶液(生成CuI和I2)和指示剂,用0.01100mol×L-1Na2S2O3溶液滴定生成的I2至终点(反应:I2 + 2S2O32- = 2I- + S4O62-),消耗Na2S2O3溶液6.45mL。
(1)判断步骤②滴定终点的方法是 。
(2)计算合金中Cu的质量分数 。
Ⅰ、高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:在烧瓶中(装置见图)加入一定量MnO2 和水,搅拌,通入 SO2和N2混合气体,反应3h。停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO3=MnSO4+H2O)。
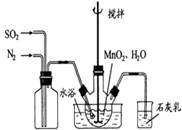
①石灰乳作用: 。
②若实验中将 换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是
。
换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是
。
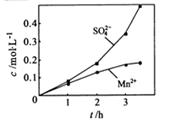
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿 时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7, 请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤:
[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH]。
① ;
② ;
③检验SO42-是否被洗涤除去; ④用少量乙醇洗涤; ⑤低于100℃干燥。
Ⅱ、锌铝合金的主要成分有Zn、Al、Cu、Si等元素。实验室测定其中Cu含量的步骤如下:①称取该合金样品1.1g,用HCl和H2O2溶解后,煮沸除去过量H2O2,过滤,滤液定容于250mL容量瓶中。
②用移液管移取50.00mL滤液于250mL碘量瓶中,控制溶液的pH=3~4,加入过量KI溶液(生成CuI和I2)和指示剂,用0.01100mol×L-1Na2S2O3溶液滴定生成的I2至终点(反应:I2 + 2S2O32- = 2I- + S4O62-),消耗Na2S2O3溶液6.45mL。
(1)判断步骤②滴定终点的方法是 。
(2)计算合金中Cu的质量分数 。
查看习题详情和答案>>
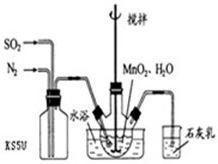 Ⅰ高纯MnCO3是制备高性能磁性材料的主要原料.
Ⅰ高纯MnCO3是制备高性能磁性材料的主要原料.
实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:
在烧瓶中(装置见右图)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h.停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO3=MnSO4+H2O).
①石灰乳作用______.
②若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图.导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是______.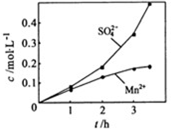
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7,请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH].
①______;②______;③检验SO42-是否被洗涤除去;④______;⑤低于100℃干燥.
Ⅱ锌铝合金的主要成分有Zn、Al、Cu、Si等元素.实验室测定其中Cu含量的步骤如下:
①称取该合金样品1.1g,用HCl和H2O2溶解后,煮沸除去过量H2O2,过滤,滤液定容于
250mL容量瓶中.
②用移液管移取50.00mL滤液于250mL碘量瓶中,控制溶液的pH=3~4,加入过量KI溶液(生成CuI和I2)和指示剂,
用0.01100mol?L-1Na2S2O3溶液滴定生成的I2至终点(反应:I2+2S2O32-=2I-+S4O62-),消耗Na2S2O3溶液6.45mL.
(1)判断步骤②滴定终点的方法是______.
(2)计算合金中Cu的质量分数______.
查看习题详情和答案>>
实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:
在烧瓶中(装置见右图)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h.停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO3=MnSO4+H2O).
①石灰乳作用______.
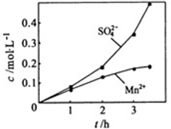
②若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图.导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是______.
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7,请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH].
①______;②______;③检验SO42-是否被洗涤除去;④______;⑤低于100℃干燥.
Ⅱ锌铝合金的主要成分有Zn、Al、Cu、Si等元素.实验室测定其中Cu含量的步骤如下:
①称取该合金样品1.1g,用HCl和H2O2溶解后,煮沸除去过量H2O2,过滤,滤液定容于
250mL容量瓶中.
②用移液管移取50.00mL滤液于250mL碘量瓶中,控制溶液的pH=3~4,加入过量KI溶液(生成CuI和I2)和指示剂,
用0.01100mol?L-1Na2S2O3溶液滴定生成的I2至终点(反应:I2+2S2O32-=2I-+S4O62-),消耗Na2S2O3溶液6.45mL.
(1)判断步骤②滴定终点的方法是______.
(2)计算合金中Cu的质量分数______.
