摘要:市售浓硫酸质量分数为98%.密度为1.84g/cm3.现用这样的浓硫酸加入稀释.配成10%的稀硫酸(密谋为1.07g/cm3)1000mL用于实验.请将有关步骤简要填写在下面空格中: ⑴计算: ⑵量取浓硫酸和水 ⑶配制溶液
网址:http://m.1010jiajiao.com/timu_id_571652[举报]
市售浓硫酸质量分数为98%,密度为1.84g/cm3。现用这样的浓硫酸加入稀释,配成10%的稀硫酸(密谋为1.07g/cm3)1000mL用于实验,请将有关步骤简要填写在下面空格中:
⑴计算:______________________________________________________
⑵量取浓硫酸和水______________________________________________
⑶配制溶液____________________________________________________
查看习题详情和答案>>根据图所示的市售浓硫酸的标签计算:已知该浓硫酸的溶质质量分数为
98%,现要配制10%的稀硫酸2 940g作为钢铁表面的清洗剂(酸洗液),需要浓硫酸___________g,换算成体积约为___________mL,还需要水(密度约为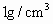 )__________mL(计算结果保留整数).
)__________mL(计算结果保留整数).

 如图所示的市售浓硫酸的标签计算:已知该浓硫酸的溶质质量分数为98%,现要配制:10%的稀硫酸2940g作为钢铁表面的酸洗液,需要浓硫酸
如图所示的市售浓硫酸的标签计算:已知该浓硫酸的溶质质量分数为98%,现要配制:10%的稀硫酸2940g作为钢铁表面的酸洗液,需要浓硫酸163
163
毫升,需要水2640
2640
毫升(密度约为1g/cm3)?(结果保留整数).
