网址:http://m.1010jiajiao.com/timu_id_56729[举报]
第I卷
题号
1
2
3
4
5
答案
C
A
D
A
A
题号
6
7
8
9
10
11
12
13
答案
C
C
B
C
A
D
C
C
题号
14
15
16
17
18
19
20
21
答案
D
AD
C
BC
B
A
D
AC
第II卷
22.(18分) 【答案】 Ⅰ.
Ⅱ.① 乙;
②见下图; ③  (或
(或 )
)
N1为电压表V1指针所指的刻度数,U2为标准电压表V2的读数.
 |
23.(14分)【解析】
(1) 
 (7分)
(7分)
(2)
 (7分)
(7分)
24.(18分) 【解析】
 ⑴ 静止释放后小球做自由落体运动到a,轻绳被拉紧时与水平方向成
⑴ 静止释放后小球做自由落体运动到a,轻绳被拉紧时与水平方向成 角,再绕O点向下做圆周运动,由机械能守恒定律得:
角,再绕O点向下做圆周运动,由机械能守恒定律得: (1分)
(1分)
轻绳被拉紧瞬间,沿绳方向的速度变为0,沿圆周切线方向的速度为: (1分)
(1分)
小球由a点运动到最低点b点过程中机械能守恒: (2分)
(2分)
设小球在最低点受到轻绳的拉力为F,则, (2分)
(2分)
联立解得: N (2分)
N (2分)
⑵ 小球与B碰撞过程中动量和机械能守恒,则
 (2分)
(2分)
 (2分)
(2分)
解得: v1=0,v2=vb= ,碰撞后小球与B交换速度 (1分)
,碰撞后小球与B交换速度 (1分)
B在木板A上滑动,系统动量守恒,设B滑到木板A最右端时速度为v,则
 (2分)
(2分)
B在木板A上滑动的过程中,系统减小的机械能转化为内能,由能量守恒定律得  (2分)
(2分)
联立解得
代入数据解得L=2.5m (1分)
25.(22分)【解析】
(1)设两板间电压为 时,带电粒子刚好从极板边缘射出电场,
时,带电粒子刚好从极板边缘射出电场,
则有 (2分)
(2分)
 代人数据,解得:
代人数据,解得: (2分)
(2分)
在电压低于100 V时,带电粒子才能从两板间射出,电压高于100 V时,带电粒子打在极板上,不能从两板间射出.粒子刚好从极板边缘射出电场时,速度最大,设最大速度为
则有: (2分)
(2分)
解得: (2分)
(2分)
(2)设粒子进入磁场时速度方向与 夹角为
夹角为 ,则速度大小
,则速度大小 (2分)
(2分)
粒子在磁场中做圆周运动的轨道半径 (2分)
(2分)
粒子从磁场中飞出的位置与进入磁场的位置之间的距离 (2分)
(2分)
代入数据,解得 与
与 无关,即射出电场的任何一个带电粒子进入磁场的入射点与出射点间距离恒为定值 (2分)
无关,即射出电场的任何一个带电粒子进入磁场的入射点与出射点间距离恒为定值 (2分)
 (3)粒子飞出电场进入磁场,在磁场中按逆时针方向做匀速圆周运动.粒子飞出电场时的速度方向与
(3)粒子飞出电场进入磁场,在磁场中按逆时针方向做匀速圆周运动.粒子飞出电场时的速度方向与 的最大夹角为
的最大夹角为
 (2分)
(2分)
当粒子从下板边缘飞出电场再进入磁场时,在磁场中运动时间最长,
 (2分)
(2分)
当粒子从上板边缘飞出电场再进入磁场时,在磁场中运动时间最短
 (2分)
(2分)
26.(每空2分,共14分)
(1)略, (2)Na+[:H] -
(3)促进,NH4++H2O NH3•H2O+
H+, 负
NH3•H2O+
H+, 负
(4)A、D、E
(5)3Na2O2+2Fe2++4H2O=2Fe(OH)3+O2↑+6Na++2OH-
27.(每空3分,共15分)
(1) (3分)
(3分)
(2)Cu+4H++2NO3-=Cu2++2NO2↑+2H2O (3分)
(3)2H2O-4e-=4H++O2↑或4OH--4e-=2H2O +O2↑ (3分)
(4)3CuO+2NH3 3Cu+N2+3H2O(3分)
3Cu+N2+3H2O(3分)
(5)1∶2(3分)
28.(共17分,除标明的外,每空2分)
(1)Cu+H2O2+2H+=Cu2++2H2O

作图:以铜为阳极,以盐酸为电解质溶液的电解池装置。
(2)原电池;Cu―2e―= Cu2+;4OH――4e―=2H2O+O2;1.8g
(3)不同意;等质量的铜片与等体积、过量的浓硝酸、稀硝酸反应,所得溶液中Cu2+的浓度基本相等。
29.(每空2分,共14分)
⑴
①②③(有错不给分)
 |
⑵
 ⑶
⑶
 |
⑷6
30.(共24分,每空2分,第Ⅱ题(4)图解6分)
Ⅰ.(1)AABB、AaBB、AABb、AaBb (2)AaBb×AaBB或AaBB×AaBB (3)青色壳:灰白色壳:花斑色壳 =9:2:3
Ⅱ.(1)限制性内切 (2)有丝 减数 (3)Bb×bb 测交  (4)2 遗传图解如下:
(4)2 遗传图解如下:

31.(共18分,每空2分)
(1)CO2 (2)B处O2多于D处,D处CO2多于B处 (3)减少 增加 上升 (4)装置中CO2量越来越少,暗反应速率下降,导致ATP和NADPH积累,进而使光反应速率下降 乳酸 (5)15N2→15NH3→氨基酸及蛋白质(或含15N的有机物) 根瘤菌、大豆
为了验证该同学的推断是否正确,甲、乙、丙三位同学各设计了一个实验方案.
甲同学的方案:将盛绿色溶液的试管加热,看是否有红棕色的气体产生.
(1)你认为甲同学的方案的不妥之处是什么?
乙同学的方案:用双氧水和二氧化锰制得氧气,并把氧气通入绿色溶液中,观察其溶液是否变蓝色.
(2)请用化学方程式表示其中的化学反应原理
丙同学的方案:在通风橱内,将一根下端弯成螺旋状且可抽动的铜丝插入盛有足量浓硝酸的试管A中,立即可观察到试管中充满红棕色的NO2气体.将NO2气体经导管通入到倾斜的另一支装有淡蓝色Cu(NO3)2溶液的试管B中,随着实验进行,试管B中的溶液蓝色加深,很快又转变为绿色,继续通入NO2,绿色保持不变,向上抽起铜丝,使反应停止.
(3)简述丙同学的方案中的溶液变色的原因.
(4)从环保的角度看,你认为三个方案中最好的是哪一个?说明理由.
分别将等质量的铜片与等体积均过量的浓硝酸、稀硝酸反应,所得到的溶液前者成绿色,后者呈蓝色,某同学提出这可能是Cu2+浓度差异引起的,你同意这种看法吗?________(填“同意”或“不同意”),原因是________________________________________;另一同学提出溶液呈“绿色”是Cu2+与NO2混合的结果,请你设计一个实验证明之(简述实验方案和实现现象)______________________________________________________________________________。
查看习题详情和答案>>从含银、铜、金和铂的金属废料中提取金、银、铂的一种工艺如下:
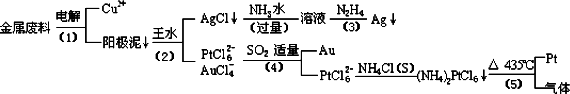
根据以上工艺回答下列问题:
(1)电解时,以金属废料为阳极,纯铜为阴极,CuSO4溶液为电解液,写出电解反应的阳极方程式:________
(2)写出步骤(4)的离子反应方程式:________;
(3)金和浓硝酸反应的化学方程式为:Au+6HNO3(浓)=Au(NO3)3+3NO2↑+3H2O但该反应的平衡常数很小,所以金和浓硝酸几乎不反应,但金却可以溶于王水,试简要解释之:________.
(4)我们知道,稀盐酸与铜不反应.在稀盐酸中加入H2O2等氧化剂后,则可使铜顺利溶解.某同学未加入氧化剂,而是设计了一个实验装置,也能使铜溶于稀盐酸.请在方格中画出该装置:
(5)分别将等质量的铜片与分别等体积、过量的浓硝酸、稀硝酸反应,所得到的溶液前者呈绿色,后者呈兰色,甲同学提出可能是Cu2+浓度不同引起的,乙同学提出溶液呈“绿色”是溶液中Cu2+与NO2共存的结果,请你设计实验探究甲乙两同学的说法谁更正确(简述实验方案和实验现象及由此得出的结论:________________
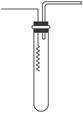
图4
(1)某研究性学习小组为了证明并观察到铜与稀硝酸反应的产物为NO,设计了如图4所示的实现装置。请你根据他们的思路,选择下列药品,完成该实验,并叙述实验步骤。
药品:稀硝酸、稀盐酸、Zn粒、CaCO3固体
步骤:①检查装置的气密性; ②____________;③____________;④______________;
⑤用注射器向试管内推入氧气(或空气)。
(2)推入氧气或空气的目的是________________________________________________。
(3)分别将等质量的铜片与等体积均过量的浓硝酸、稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出这可能是Cu2+浓度差异引起的,你是否同意这种看法?? _______(填“同意”或“不同意”),原因是________________;另一同学提出溶液呈“绿色”是Cu2+与NO2混合的结果,请你设计一个实验证明之。(简述实验方案和实验现象)
查看习题详情和答案>>
①用稀HNO3清洗做过银镜反应实验的试管
②用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物
③读取滴定管内液体的体积,俯视读数导致读数偏小
④不慎将苯酚溶液沾到皮肤上,立即用酒精清洗
⑤向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸,以制备Fe(OH)3胶体
⑥向2.0mL浓度均为0.1mol/L的KCl、KI混合溶液中滴加1~2滴0.01mol/L AgNO3
溶液,振荡,沉淀呈黄色
(2)某课外小组对一些金属单质和化合物的性质进行研究.
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分:
| 实验步骤 | 实验现象 |
| 将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中 | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色 |
反应结束后分离出溶液备用 | |
| 红色固体用蒸馏水洗涤后,置于潮湿空气中 | 一段时间后固体由红色变为绿色[其主要成分为Cu2(OH)2CO3] |
置换反应______
化合反应______.
②用石墨作电极,电解上述实验分离出的溶液,两极产生气泡.持续电解,在阴极附近的溶液中还可观察到的现象是______,解释此现象的离子方程式是______
(2)探究氧化铜性质
①取A、B两支试管,向A中先加入适量CuO粉末,再分别向A和B中加入等体积的3% H2O2溶液,只观察到A中有大量气泡.实验结论是______.
②用收集气体并测定其体积的方法探究试管A中反应的速率,必需的实验仪器有:______.
查看习题详情和答案>>