网址:http://m.1010jiajiao.com/timu_id_565374[举报]
一、选择题:
1.B 2.A 3.C 4.B 5.D 6.B 7.B 8.C 9.A 10.B 11.A 12.C
二、选择题:
13.B  14.BC 15.B 16.C.17.AD 18.BC 19.AB 20.C
14.BC 15.B 16.C.17.AD 18.BC 19.AB 20.C
三、
21.B C D E
22.⑴K2CO3 、AlCl3、BaCl2;
⑵产生白色沉淀,后沉淀逐渐溶解;
⑶①中;②Ba2++OH-+H++SO2- 4=BaSO4↓+H2O;③13
四、
23.本题答案有开放性,合理即可给分。
⑴①C(或Fe) ②
⑶①CaC2+2H2O=Ca(OH)2+C2H2↑ ;②麦芽糖;
⑷①Na2CO3+CO2+H2O=2NaHCO3 ;②红褐色固体。
24.
编号
1
2
3
4
5
X的化学式
Na
Na2O
Na2O2
NaOH
NaH
加入X的质量(g)
4.6
6.2
7.8
8.0
4.8
五、
25.(1)醛基;略(为羧基的结构式);
(2)氧化反应;酯化反应;

 (3)
(4)
(3)
(4)

六、
26.

(0, 0.7) (0.1, 0.4) (0.2, 0.3) (0.3, 0.4) (0.4, 0.7) (0.5, 0.7)
(每1折点1分,离子方程式每个1分)
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
实验室配制500mL0.2mol·L-1的FeSO4溶液,具体操作步骤为:
①在天平上称取一定质量的绿矾(FeSO4·7H2O),把它放在烧杯中,用适量的蒸馏水使其完全
溶解;
②把制得的溶液小心的注入500mL的容量瓶中;
③继续向容量瓶中滴加蒸馏水至液面距刻度线1~2cm处时,改用胶头滴管小心滴加,直到
溶液的凹液面恰好与刻度线相切为止;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次的洗涤液都转入容量瓶中,并轻轻摇匀;
⑤将容量瓶塞好,充分摇匀。 请填写下列空白。
⑴用托盘天平称取的绿矾的质量为: ;
⑵上述操作的正确顺序为: ;
⑶本次实验用到的仪器有:玻璃棒、 ,
在配制溶液的过程中多次用到玻璃棒,在溶解时玻璃棒的作用是: ,
在移液时玻璃棒的作用是: 。
⑷观察液面时,若俯视刻度线,会使所配制的溶液的浓度 (填“偏高”、“偏低”
或“无影响”下同);加蒸馏水时不慎超过了刻度线后倒出部分溶液,使液面与刻度线相切,
会 ;
⑸用ρ=1.84g·mL-1,质量分数为98%的浓硫酸配制200mL1mol·L-1的稀硫酸与上述配制溶液的步骤上的差别主要有三点:
①计算:理论上应取浓硫酸的体积V= mL(精确到小数点后两位);
②量取:由于量筒是一种粗略的量具,如想精确量取,必需选用 (填仪器名称)。
③溶解:稀释浓硫酸的方法
。
查看习题详情和答案>>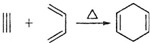 ,如果要合成
,如果要合成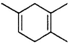 所用的原始原料可以是
所用的原始原料可以是A.2-甲基-l,3-丁二烯和2-丁炔 B.1,3-戊二烯和2-丁炔
C.2,3-二甲基-1,3-戊二烯和乙炔 D.,3-二甲基-l,3-丁二烯和丙炔
II(A~G都是有机化合物,它们的转化关系如下:
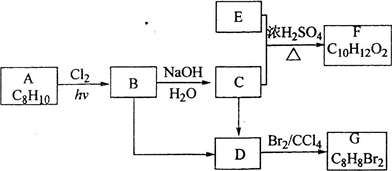
请回答下列问题:
(1)已知:6.0g化合物E完全燃烧生成8.8g C02和3.6g H20;E的蒸气与氢气的相对密度为30,则E的分子式为
(2)A为一取代芳烃,B中含有一个甲基.由B生成C的化学方程式为
| NaOH |
| △ |
| NaOH |
| △ |
(3)由B生成D、由C生成D的反应条件分别是
(4)由A生成B、由D生成G的反应类型分别是
(5)F存在于栀子香油中,其结构简式为


(6)在G的同分异构体中,苯环上一硝化的产物只有一种的共有



请根据以上流程,回答相关问题:

(1)操作①的名称是:
(2)参照右图溶解度曲线,固体B的主要成分
(3)同学甲提出一些新的方案,对上述操作②后无色溶液进行除杂提纯,其方案如下:
(有关资料)
| 化学式 | BaCO3 | BaSO4 | Ca(OH)2 | MgCO3 | Mg(OH)2 |
| Ksp | 8.1×10一9 | 1.08×10一10 | 1.0×10一4 | 3.5×10一5 | 1.6×10一11 |

(i)若在操作⑤结束后发现溶液B略有浑浊,应采取的措施是
(ii)混合液A的主要成分是
(检验除杂效果)
(ⅲ)为检验Mg2+、SO42-是否除尽,通常分别取悬浊液A上层清液于两试管中.进行如下实验:
步骤一:检验Mg2+是否除尽.向其中一支试管中加入某溶液,如果没有沉淀生成,则表明Mg2+已除尽.效果最好的是
A.K2 CO3 B.KOH C.CaCl2
步骤二:检验SO42-是否除尽.向另一支试管中加入BaCl2溶液,如果无有沉淀生成,则SO42-已除尽.
(获取纯净氯化钾)
(ⅳ)对溶液B加热并不断滴加l mol?L一1的盐酸溶液,同时用pH试纸检测溶液,直至pH=5时停止加盐酸,得到溶液C.
(ⅴ)将溶液C倒入
(问题讨论)
(ⅵ)进行操作⑤前,需先加热,使沉淀颗粒增大,便于过滤;该操作中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,此时溶液B中Mg2+物质的量浓度
| A、0.14mol | B、0.16mol | C、0.21mol | D、0.24mol |