摘要:C2H2 (g)+O2 (g) 2CO2 (g)+H2O(g),△H=-1 256KJ/mol D.葡萄糖的实验式:CH2O
网址:http://m.1010jiajiao.com/timu_id_554781[举报]
已知热化学方程式C2H2(g)+O2(g)=2CO2(g)+H2O(g);ΔH=-1256 kJ·mol-1,下列说法正确的是 ( )
A.乙炔的燃烧热为1256 kJ·mol-1
B.若转移10 mol电子,则消耗2.5 mol O2
C.若生成2 mol液态水,则ΔH=-2512 kJ·mol-1
D.若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ
查看习题详情和答案>>
已知热化学方程式C2H2(g)+O2(g)=2CO2(g)+H2O(g);ΔH=-1256 kJ·mol-1,下列说法正确的是 ( )
| A.乙炔的燃烧热为1256 kJ·mol-1 |
| B.若转移10 mol电子,则消耗2.5 mol O2 |
| C.若生成2 mol液态水,则ΔH=-2512 kJ·mol-1 |
| D.若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ |
已知热化学方程式C2H2(g)+O2(g)=2CO2(g)+H2O(g);ΔH=-1256 kJ·mol-1,下列说法正确的是
[ ]
A.乙炔的燃烧热为1256 kJ·mol-1
B.若转移10 mol电子,则消耗2.5 mol O2
C.若生成2 mol液态水,则ΔH=-2512 kJ·mol-1
D.若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ
查看习题详情和答案>>
B.若转移10 mol电子,则消耗2.5 mol O2
C.若生成2 mol液态水,则ΔH=-2512 kJ·mol-1
D.若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ
已知热化学方程式C2H2(g)+O2(g)=2CO2(g)+H2O(g);ΔH=-1256 kJ·mol-1,下列说法正确的是 ( )
| A.乙炔的燃烧热为1256 kJ·mol-1 |
| B.若转移10 mol电子,则消耗2.5 mol O2 |
| C.若生成2 mol液态水,则ΔH=-2512 kJ·mol-1 |
| D.若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ |
已知充分燃烧a g乙炔气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是( )
| A.2C2H2(g)+5O2 (g)===4CO2 (g)+2H2O (l);ΔH=-4b kJ/mol |
B.C2H2(g)+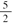 O2(g)===2CO2 (g)+H2O (l);ΔH=2b kJ/mol O2(g)===2CO2 (g)+H2O (l);ΔH=2b kJ/mol |
| C.2C2H2(g)+5O2 (g)===4CO2 (g)+2H2O (l);ΔH=2b kJ/mol |
| D.2C2H2(g)+5O2 (g)===4CO2 (g)+2H2O (l);ΔH=b kJ/mol |