题目内容
已知热化学方程式C2H2(g)+O2(g)=2CO2(g)+H2O(g);ΔH=-1256 kJ·mol-1,下列说法正确的是 ( )
| A.乙炔的燃烧热为1256 kJ·mol-1 |
| B.若转移10 mol电子,则消耗2.5 mol O2 |
| C.若生成2 mol液态水,则ΔH=-2512 kJ·mol-1 |
| D.若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ |
B
燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物时所放出的能量。A不正确,氢对应的是液态水。1mol氧气得到4mol电子,所以选项B正确。△H和方程式的计量数及物质的状态有关系,C不正确。形成4 mol碳氧共用电子对,说明CO2是1mol,所以D是错误的。答案选B。

练习册系列答案
相关题目
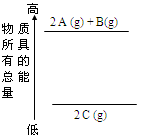
 FeO(s) ?
FeO(s) ?  =-272.0KJ/mol
=-272.0KJ/mol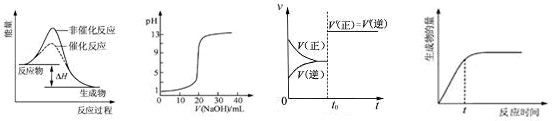
 2H2↑+O2↑。制得的氢气可用于燃料电池。
2H2↑+O2↑。制得的氢气可用于燃料电池。