网址:http://m.1010jiajiao.com/timu_id_53716[举报]
1
2
3
4
5
6
C
B
D
D
D
C
7
8
9
10
11
12
C
B
C
B
A
C
13
14
15
16
17
18
B
B
D
A
C
A
19
20
21
22
23
24
A
D
B
A
D
B
25、氧化剂:KMnO4 还原剂:HCl 质量比:316∶511
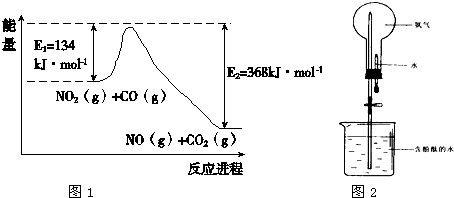
(1)根据图1能量变化示意图:写出CO和NO2反应生成NO和CO2的热化学方程式
(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的关系如下表,试判断K1
| T/K | 298 | 398 |
| 平衡常数K | K1 | K2 |
a.v正(H2)=3v逆(N2)
b.容器内压强保持不变
c.容器中混合气体的密度保持不变
d.N2、H2、NH3的浓度之比为1:3:2
(4)氨气极易溶于水,常用如图2实验来验证,在标准状况下,烧瓶中的氨水使酚酞变红.请回答:
①用化学用语说明所得氨水能使酚酞变红的原因
②25℃时,将一定量的氨水与盐酸混合后pH=7,测该混合溶液中c(Cl-)与c(NH4+)关系为
a.c(Cl-)>c(NH4+) b.c(Cl-)﹦c(NH4+)
c.c(Cl-)<c(NH4+) d.无法判断.

(1)填写装置的作用:B
(2)先点燃
(3)证明有SO2生成的现象是
(4)可以证明气体X中含有氢气的实验现象是:
(5)反应后A的溶液中含有Fe3+和Fe2+,检验其中的Fe2+的方法是
求(1)气体A中各成分气体的体积比
(2)反应中共消耗锌多少克?
可能用到的相对原子质量:H:1 O:16 S:32 Fe:56 Ba:137 Al:27 Zn:65 Cl:35.5 N:14 Na:23 Mg:24.
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表:
| T℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应正向为ΔH 0;若该反应符合下图所示的关系,则在图中,Y轴是指 。
(2)能判断该反应达到化学平衡状态的依据是 (多选扣分)。
a.容器中压强不变 b.混合气体中c(CO)不变
c.v (H2) 正=v (H2O) 逆 d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式: 0.9·c(CO2)·c(H2)=c(CO)·c(H2O),由此可以判断此时的温度为 ℃。其它条件不变,升高温度,原化学平衡向 反应方向移动(填“正”或“逆”),容器内混合气体的密度 (填“增大”、“减小”或“不变”),气体平均相对分子质量 (填“增大”、“减小”或“不变”)。
(4)若在一密闭容器中,将一定量的CO与H2O混合加热到830℃下达到平衡。若反应开始时CO与H2O的浓度分别为0.200 mol/L和0.100 mol/L,平衡时CO的转化率 。
查看习题详情和答案>>
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表:
| T℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |

回答下列问题:
(1)该反应正向为ΔH 0;若该反应符合下图所示的关系,则在图中,Y轴是指 。
(2)能判断该反应达到化学平衡状态的依据是 (多选扣分)。
a.容器中压强不变 b.混合气体中c(CO)不变
c.v (H2) 正=v (H2O) 逆 d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式: 0.9·c(CO2)·c(H2)=c(CO)·c(H2O),由此可以判断此时的温度为 ℃。其它条件不变,升高温度,原化学平衡向 反应方向移动(填“正”或“逆”),容器内混合气体的密度 (填“增大”、“减小”或“不变”),气体平均相对分子质量 (填“增大”、“减小”或“不变”)。
(4)若在一密闭容器中,将一定量的CO与H2O混合加热到830℃下达到平衡。若反应开始时CO与H2O的浓度分别为0.200 mol/L和0.100 mol/L,平衡时CO的转化率 。
查看习题详情和答案>>