题目内容
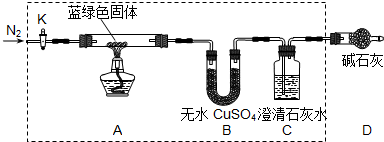
某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体.为此,他们设计了如下装置验证所产生的气体.

(1)填写装置的作用:B
(2)先点燃
(3)证明有SO2生成的现象是
(4)可以证明气体X中含有氢气的实验现象是:
(5)反应后A的溶液中含有Fe3+和Fe2+,检验其中的Fe2+的方法是

(1)填写装置的作用:B
防止倒吸
防止倒吸
,C验证有SO2生成,同时除去SO2
验证有SO2生成,同时除去SO2
,G防止空气中的H2O进入F
防止空气中的H2O进入F
.(2)先点燃
A
A
处酒精灯(填“A”或“E”),点燃E处酒精灯前一步操作检验氢气的纯度
检验氢气的纯度
.(3)证明有SO2生成的现象是
酸性高锰酸钾溶液颜色变浅
酸性高锰酸钾溶液颜色变浅
.(4)可以证明气体X中含有氢气的实验现象是:
E中黑色(CuO)变成红色(Cu),F中白色粉末变成蓝色
E中黑色(CuO)变成红色(Cu),F中白色粉末变成蓝色
.如果去掉装置D,还能否根据F中的现象判断气体中有氢气?不能
不能
(填“能”或“不能”),原因是因为混合气体中可能含H2O,会干扰H2的检验
因为混合气体中可能含H2O,会干扰H2的检验
.(5)反应后A的溶液中含有Fe3+和Fe2+,检验其中的Fe2+的方法是
取A的溶液,滴加酸性高锰酸钾溶液,若红色褪去,证明有Fe2+
取A的溶液,滴加酸性高锰酸钾溶液,若红色褪去,证明有Fe2+
.分析:(1)熄灭A装置中酒精灯时,会造成倒吸;酸性高锰酸钾溶液能和二氧化硫发生反应而褪色;空气中的H2O会进入F产生影响;
(2)A装置中酒精灯的作用是使浓硫酸和铁反应生成二氧化硫,氢气和氧化铜的反应中要检验氢气的纯度,否则后产生安全事故;
(3)二氧化硫能和酸性高锰酸钾溶液反应而使其褪色;
(4)氢气和氧化铜反应生成铜单质,水能使无水硫酸铜变蓝,加热时水会蒸发而导致产生的气体中含有水蒸气,从而造成干扰;
(5)亚铁离子能使酸性高锰酸钾溶液褪色.
(2)A装置中酒精灯的作用是使浓硫酸和铁反应生成二氧化硫,氢气和氧化铜的反应中要检验氢气的纯度,否则后产生安全事故;
(3)二氧化硫能和酸性高锰酸钾溶液反应而使其褪色;
(4)氢气和氧化铜反应生成铜单质,水能使无水硫酸铜变蓝,加热时水会蒸发而导致产生的气体中含有水蒸气,从而造成干扰;
(5)亚铁离子能使酸性高锰酸钾溶液褪色.
解答:解:(1)熄灭A装置中酒精灯时,A装置中气体冷却压强减小,C装置中溶液易进入A试管中产生倒吸现象,所以B装置的作用是防止倒吸;酸性高锰酸钾溶液有强氧化性,二氧化硫能和酸性高锰酸钾溶液发生氧化还原反应而使其褪色,所以酸性高锰酸钾的作用是:验证有SO2生成,同时除去SO2;空气中含有水蒸气,如果没有G装置,水蒸气进入F装置干扰实验,所以G的作用是:防止空气中的H2O进入F,
故答案为:防止倒吸;验证有SO2生成,同时除去SO2;防止空气中的H2O进入F;
(2)A装置的目的是制取气体,E装置的目的是检验生成的气体,所以先点燃A处酒精灯;氢气是可燃性气体,在一定范围内易产生爆炸,为防止安全事故产生所以点燃E处酒精灯前一步操作是:检验氢气的纯度,
故答案为:A;检验氢气的纯度;
(3)二氧化硫有还原性,酸性高锰酸钾有强氧化性,二者能发生氧化还原反应而使酸性高锰酸钾溶液颜色变浅,
故答案为:酸性高锰酸钾溶液颜色变浅;
(4)生成的气体经洗气和干燥后剩余的气体就是氢气,氢气有还原性能和氧化铜在加热条件下发生置换反应生成铜单质,生成的水遇无水硫酸铜时白色固体变蓝色,所以证明含有氢气的现象是:E中黑色(CuO)变成红色(Cu),F中白色粉末变成蓝色;制取的气体中含有水蒸气,如果去掉D装置,会干扰H2的检验,所以不能,
故答案为:E中黑色(CuO)变成红色(Cu),F中白色粉末变成蓝色;不能;因为混合气体中可能含H2O,会干扰H2的检验;
(5)酸性高锰酸钾有强氧化性,能氧化二氧化硫而使其褪色,所以检验亚铁离子的方法是:取A的溶液,滴加酸性高锰酸钾溶液,若红色褪去,证明有Fe2+,
故答案为:取A的溶液,滴加酸性高锰酸钾溶液,若红色褪去,证明有Fe2+.
故答案为:防止倒吸;验证有SO2生成,同时除去SO2;防止空气中的H2O进入F;
(2)A装置的目的是制取气体,E装置的目的是检验生成的气体,所以先点燃A处酒精灯;氢气是可燃性气体,在一定范围内易产生爆炸,为防止安全事故产生所以点燃E处酒精灯前一步操作是:检验氢气的纯度,
故答案为:A;检验氢气的纯度;
(3)二氧化硫有还原性,酸性高锰酸钾有强氧化性,二者能发生氧化还原反应而使酸性高锰酸钾溶液颜色变浅,
故答案为:酸性高锰酸钾溶液颜色变浅;
(4)生成的气体经洗气和干燥后剩余的气体就是氢气,氢气有还原性能和氧化铜在加热条件下发生置换反应生成铜单质,生成的水遇无水硫酸铜时白色固体变蓝色,所以证明含有氢气的现象是:E中黑色(CuO)变成红色(Cu),F中白色粉末变成蓝色;制取的气体中含有水蒸气,如果去掉D装置,会干扰H2的检验,所以不能,
故答案为:E中黑色(CuO)变成红色(Cu),F中白色粉末变成蓝色;不能;因为混合气体中可能含H2O,会干扰H2的检验;
(5)酸性高锰酸钾有强氧化性,能氧化二氧化硫而使其褪色,所以检验亚铁离子的方法是:取A的溶液,滴加酸性高锰酸钾溶液,若红色褪去,证明有Fe2+,
故答案为:取A的溶液,滴加酸性高锰酸钾溶液,若红色褪去,证明有Fe2+.
点评:本题考查了常见气体的制备原理及其性质,难度不大,明确二氧化硫的性质是解本题的关键,注意亚铁离子、铁离子的检验方法是高考的热点,是学习的重点.

练习册系列答案
相关题目
 工业上常用铁质容器盛装冷浓硫酸.某兴趣小组的同学发现:将一定量的铁钉与浓硫酸加热时,观察到铁钉完全溶解,并产生大量气体.实验室现有下列试剂:0.01mol/L 酸性KMnO4溶液、0.10mol/L KI溶液、新制氯水、淀粉溶液、蒸馏水.请你协助他们探究所得溶液和气体的成分.
工业上常用铁质容器盛装冷浓硫酸.某兴趣小组的同学发现:将一定量的铁钉与浓硫酸加热时,观察到铁钉完全溶解,并产生大量气体.实验室现有下列试剂:0.01mol/L 酸性KMnO4溶液、0.10mol/L KI溶液、新制氯水、淀粉溶液、蒸馏水.请你协助他们探究所得溶液和气体的成分.
 (2010?揭阳模拟)铁在冷的浓硫酸中能发生钝化.某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体.实验室现有下列试剂:0.01mol/L 酸性KMnO4溶液、0.1mol/L KI溶液、3%H2O2溶液、淀粉溶液、蒸馏水.请你协助他们探究所得溶液和气体的成分.
(2010?揭阳模拟)铁在冷的浓硫酸中能发生钝化.某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体.实验室现有下列试剂:0.01mol/L 酸性KMnO4溶液、0.1mol/L KI溶液、3%H2O2溶液、淀粉溶液、蒸馏水.请你协助他们探究所得溶液和气体的成分. 铁在冷的浓硫酸中能发生钝化.某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体.请你协助他们探究所得气体的成分.
铁在冷的浓硫酸中能发生钝化.某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体.请你协助他们探究所得气体的成分.