摘要:B.
网址:http://m.1010jiajiao.com/timu_id_53687[举报]
1
2
3
4
5
6
C
B
D
D
D
C
7
8
9
10
11
12
C
B
C
B
A
C
13
14
15
16
17
18
B
B
D
A
C
A
19
20
21
22
23
24
A
D
B
A
D
B
25、氧化剂:KMnO4 还原剂:HCl 质量比:316∶511
B.请写出以乙烯为有机原料合成乙酸乙酯的各步反应方程式,并注明反应类型.
查看习题详情和答案>>
CH2=CH2+H2O
CH3CH2OH
| 催化剂 |
CH2=CH2+H2O
CH3CH2OH
:加成反应| 催化剂 |
2CH3CH2OH+O2
2CH3CHO+2H2O
| Cu |
| △ |
2CH3CH2OH+O2
2CH3CHO+2H2O
:| Cu |
| △ |
氧化反应
氧化反应
2CH3CHO+O2
2CH3COOH
| 催化剂 |
2CH3CHO+O2
2CH3COOH
:氧化反应.| 催化剂 |
 B.电解原理在化学工业中广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
B.电解原理在化学工业中广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入酚汰试液,则
①Y电极上的电极反应式为
2C1-=C12+2e-
2C1-=C12+2e-
.②在X电极附近观察到的现象是
溶液变红色,产生无色气泡
溶液变红色,产生无色气泡
.③要使电解后溶液恢复到电解前的状态,则需加入(或通入)
HC1(或氯化氢)
HC1(或氯化氢)
.(2)如果要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是
铜(或纯铜)
铜(或纯铜)
,电极反应式为Cu2++2e-→Cu
Cu2++2e-→Cu
.②电解完成后,硫酸铜溶液的浓度
变小
变小
(填“变大”、“变小”或“不变”)(3)若X、Y都是铜电极,a是浓度均为2mol?L-1的AgNO3与Cu(NO3)2的混合溶液1L,电解一段时间后X电极上有3.2g铜析出,此时直流电源已输出
2.1
2.1
mol电子.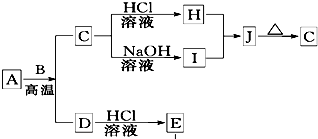 B、D是常见金属单质,A是一种红棕色金属氧化物,电解熔融态的C得到B单质,J是一种难溶于水的白色固体.
B、D是常见金属单质,A是一种红棕色金属氧化物,电解熔融态的C得到B单质,J是一种难溶于水的白色固体.(1)在E的溶液中加入氢氧化钠溶液,可以观察到的现象是
先生成白色沉淀,迅速变为灰绿色,最终变为红褐色
先生成白色沉淀,迅速变为灰绿色,最终变为红褐色
.(2)按要求写化学方程式或离子方程式:
①A与B在高温条件下生成C和D的化学方程式:
Fe2O3+2Al
Al2O3+2Fe
| ||
Fe2O3+2Al
Al2O3+2Fe
;
| ||
②在E的水溶液中通入氯气后的生成物和I溶液反应的离子方程式:
Fe3++3AlO2-+6H2O═3Al(OH)3↓+Fe(OH)3↓
Fe3++3AlO2-+6H2O═3Al(OH)3↓+Fe(OH)3↓
.(3)由D和A组成的混合物与稀HCl作用,固体恰好溶解,所得溶液中滴加KSCN溶液不显红色,且生成的E与H2的物质的量之比为4:1.则反应物中A、D、HCl的物质的量之比为
1:2:8
1:2:8
.