网址:http://m.1010jiajiao.com/timu_id_52273[举报]
(14分)某学生用0.l000mol.L-l盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应)。实验步骤如下:
(1)配制待测液:用2.50 g含有少量杂质的固体烧碱样品配制500 mL溶液。需用的玻璃仪器除了烧杯、胶头滴管、玻璃棒外,还需要 。
(2)滴定:
I.用蒸馏水洗涤酸式滴定管,并立即注入盐酸标准溶液至“O”刻度线以上
Ⅱ.固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”或“O”刻度线以下,并记录读数
Ⅲ.移取20.OOmL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液
Ⅳ,用标准液滴定至终点,记录滴定管液面读数。
①上述滴定步骤中有错误的是(填编号) ,该错误操作会导致测定结果 (填“偏大”、“偏小”或“无影响”)。
②步骤Ⅳ中滴定时眼睛应 :判断滴定终点的现象是 。
③若步骤II中仰视读数,步骤Ⅳ中俯视读数,则会使测定结果 (填“偏大”、“偏小”或“无影响’')。
(3)按正确操作测得有关数据记录如下: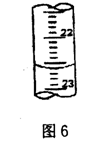
| 滴定次数 | 待测液体积 | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.20 | 20.38 |
| 第二次 | 20.00 | 4.00 | 24.20 |
| 第三次 | 20.00 | 2.38 | a |
②烧碱样品的纯度为 % 。 查看习题详情和答案>>
(12分)某学生用0.l000mol.L-l盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应)。实验步骤如下:
(1)配制待测液:用2.50 g含有少量杂质的固体烧碱样品配制500 mL溶液。需用的玻璃仪器除了烧杯、胶头滴管、玻璃棒外,还需要 。
(2)滴定:
I.用蒸馏水洗涤酸式滴定管,并立即注入盐酸标准溶液至“O”刻度线以上
Ⅱ.固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”或“O”刻度线以下,并记录读数
Ⅲ.移取20.OOmL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液
Ⅳ.用标准液滴定至终点,记录滴定管液面读数。
①上述滴定步骤中有错误的是(填编号) ,该错误操作会导致测定结果 (填“偏大”、“偏小”或“无影响”)。
②步骤Ⅳ中滴定时眼睛应 :判断滴定终点的现象是 。
③若步骤II中仰视读数,步骤Ⅳ中俯视读数,则会使测定结果 (填“偏大”、“偏小”或“无影响’')。
(3)按正确操作测得有关数据记录如下:
| 滴定次数 | 待测液体积 | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.20 | 20.38 |
| 第二次 | 20.00 | 4.00 | 24.20 |
| 第三次 | 20.00 | 2.38 | a |
②烧碱样品的纯度为 % 。 查看习题详情和答案>>
(14分)某学生用0.l000mol.L-l盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应)。实验步骤如下:
(1)配制待测液:用2.50 g含有少量杂质的固体烧碱样品配制500 mL溶液。需用的玻璃仪器除了烧杯、胶头滴管、玻璃棒外,还需要 。
(2)滴定:
I.用蒸馏水洗涤酸式滴定管,并立即注入盐酸标准溶液至“O”刻度线以上
Ⅱ.固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”或“O”刻度线以下,并记录读数
Ⅲ.移取20.OOmL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液
Ⅳ,用标准液滴定至终点,记录滴定管液面读数。
①上述滴定步骤中有错误的是(填编号) ,该错误操作会导致测定结果 (填“偏大”、“偏小”或“无影响”)。
②步骤Ⅳ中滴定时眼睛应 :判断滴定终点的现象是 。
③若步骤II中仰视读数,步骤Ⅳ中俯视读数,则会使测定结果 (填“偏大”、“偏小”或“无影响’')。
(3)按正确操作测得有关数据记录如下:
|
滴定次数 |
待测液体积 |
标准盐酸体积(mL) |
|
|
滴定前读数(mL) |
滴定后读数(mL) |
||
|
第一次 |
20.00 |
0.20 |
20.38 |
|
第二次 |
20.00 |
4.00 |
24.20 |
|
第三次 |
20.00 |
2.38 |
a |
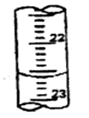
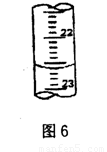
①a的读数如图6所示,则a= ;
②烧碱样品的纯度为 % 。
查看习题详情和答案>>
(1)配制待测液:用2.50 g含有少量杂质的固体烧碱样品配制500 mL溶液。需用的玻璃仪器除了烧杯、胶头滴管、玻璃棒外,还需要 。
(2)滴定:
I.用蒸馏水洗涤酸式滴定管,并立即注入盐酸标准溶液至“O”刻度线以上
Ⅱ.固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”或“O”刻度线以下,并记录读数
Ⅲ.移取20.OOmL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液
Ⅳ.用标准液滴定至终点,记录滴定管液面读数。
①上述滴定步骤中有错误的是(填编号) ,该错误操作会导致测定结果 (填“偏大”、“偏小”或“无影响”)。
②步骤Ⅳ中滴定时眼睛应 :判断滴定终点的现象是 。
③若步骤II中仰视读数,步骤Ⅳ中俯视读数,则会使测定结果 (填“偏大”、“偏小”或“无影响’')。
(3)按正确操作测得有关数据记录如下:
| 滴定次数 | 待测液体积 | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.20 | 20.38 |
| 第二次 | 20.00 | 4.00 | 24.20 |
| 第三次 | 20.00 | 2.38 | a |

②烧碱样品的纯度为 % 。
某同学在用稀盐酸与铁制取氢气的实验中,发现加入少量氯化铜溶液可加快氢气的生成速率。请回答下列问题:
(1)要加快上述实验中气体产生的速率,还可采取的措施有
(答两种);
(2)实验室中现有NaCl、CuSO4、FeCl2、ZnCl2等4种溶液,可与实验中CuCl2溶液起相似作用的是 ;
(3)为了进一步研究氯化铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验(混合溶液) | A | B | C | D | E | F |
| 4mol/L 盐酸/mL | 60 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuCl2溶液/mL | 0 | 1.0 | 5.0 | 10 | V6 | 40 |
| H2O/mL | V7 | V8 | V9 | V10 | 20 | 0 |
①请完成此实验设计,其中:V1= ,V6= ,V9= ;
②该同学最后得出的结论为:当加入少量CuCl2溶液时,生成氢气的速率会
大大提高。但当加入的CuCl2溶液超过一定量时,生成氢气的速率反而会下降。
请分析氢气生成速率下降的主要原因
查看习题详情和答案>>