网址:http://m.1010jiajiao.com/timu_id_515318[举报]
第I卷(共126分)
一、选择题(78分)
1.B 2.C 3.D 4.A 5.D 6.B 7.C 8.A 9.D 10.B 11.D
12.A 13.C
二、选择题(48分)
14.A 15.C 16.D 17.C 18.BD 19.CD 20.B 21.AC
第Ⅱ卷(共174分)
.files/image271.jpg) 22.(17分)
22.(17分)
(1)①BCD全对得2分,对而不全得1分,有错不得分。
②.files/image273.gif) 3分
3分
(2)①如图1所示 2分
②B E D 每空2分, 共6分
③.files/image275.gif) 2分
2分 .files/image277.gif) 2分
2分
23.(16分)解:(1)设两人奔跑的最大速度为.files/image279.gif) ,乙在接力区跑出的距离为
,乙在接力区跑出的距离为.files/image281.gif) 时速度达到
时速度达到.files/image283.gif) ,根据运动学公式有
,根据运动学公式有.files/image285.gif) 2分
2分
.files/image287.gif) 2分
2分
解得.files/image289.gif) 3分
3分
(2)设乙在距甲.files/image291.gif) 处开始起跑,到乙接棒时乙跑过的距离为
处开始起跑,到乙接棒时乙跑过的距离为.files/image281.gif)
根据运动学公式有.files/image294.gif) 2分
2分
.files/image296.gif) 2分
2分
且.files/image298.gif) 2分
2分
解得.files/image300.gif) 3分
3分
24.(19分)解:粒子在点场中做类平抛运动,有.files/image302.gif) 设
设.files/image134.gif) 两点间电势差为
两点间电势差为.files/image305.gif) ,由动能定理有
,由动能定理有
.files/image307.gif) 3分
3分
解得:.files/image309.gif) 2分
2分
(2)粒子在.files/image311.gif) 的区域内运动的轨迹如图2所示。设其在匀强磁场中做匀速圆周运动的轨道半径为
的区域内运动的轨迹如图2所示。设其在匀强磁场中做匀速圆周运动的轨道半径为.files/image313.gif) ,磁场的磁感应强度为
,磁场的磁感应强度为.files/image315.gif) 。由题意,粒子做圆周运动的圆心一定在
。由题意,粒子做圆周运动的圆心一定在.files/image223.gif) 轴上
轴上
.files/image318.jpg) 由牛顿第二定律
由牛顿第二定律.files/image320.gif) 2分
2分
解得.files/image322.gif) 1分
1分
由几何知道得.files/image324.gif) 1分
1分
解得.files/image326.gif) 1分
1分
所以.files/image328.gif) 2分
2分
(3)由题意,当以粒子进入磁场的位置和射出磁场的位置的连线作为磁场的直径时,磁场面积最小 1分
设磁场的最小面积为.files/image330.gif)
由几何知道得磁场面积最小时的半径.files/image332.gif) 2分
2分
解得最小面积为.files/image334.gif)
.files/image335.jpg) 25.(20分)解:(1)金属棒在图3所示各力作用下,先做加速度逐渐减小的加速运动,当加速度为零时,金属棒达到最大速度,此后开始做匀速直线运动。设最大速度为
25.(20分)解:(1)金属棒在图3所示各力作用下,先做加速度逐渐减小的加速运动,当加速度为零时,金属棒达到最大速度,此后开始做匀速直线运动。设最大速度为.files/image337.gif) ,金属棒达到最大速度的一半时的加速度为
,金属棒达到最大速度的一半时的加速度为.files/image095.gif)
.files/image340.jpg) 则速度达到最大时有
则速度达到最大时有.files/image342.gif) 1分
1分
.files/image344.gif) 1分
1分
.files/image346.gif) 1分
1分
由以上各式解得 .files/image348.gif) 1分
1分
金属棒达到最大速度的一半时,由牛顿第二定律有
.files/image350.gif) 2分
2分
.files/image352.gif)
解得.files/image354.gif) 1分
1分
(2)设整个电路放出的电热为.files/image146.gif) ,由能量守恒定律有
,由能量守恒定律有
.files/image357.gif) 2分
2分
代入上面的.files/image337.gif) 值,可得
值,可得.files/image360.gif) 1分
1分
因.files/image362.gif)
故金属棒放出的电热.files/image364.gif) 2分
2分
(3).files/image366.gif) 上消耗的功率
上消耗的功率.files/image368.gif) 1分
1分
.files/image370.gif)
.files/image372.gif)
.files/image374.gif) 3分
3分
.files/image376.gif) 1分
1分
当.files/image378.gif) 时
1分
时
1分
.files/image366.gif) 消耗的功率最大
消耗的功率最大 .files/image381.gif) 2分
2分
26.(13分)
(1).files/image223.gif) 的电子式:
的电子式:.files/image384.jpg) 2分 非极性1分
2分 非极性1分
(2)87 1分
(3)C 1分
(4)碱(1分) .files/image386.gif) 2分
2分
.files/image388.gif) 2分
2分
(5).files/image390.gif) 2分 减小1分
2分 减小1分
.files/image392.jpg) 27.(16分)
27.(16分)
(1).files/image394.gif) (2分)
1分
(2分)
1分
(2)①⑥(各1分,共2分。答③不扣分,其余有错扣1分)
(3)羟基1分 羧基1分
.files/image396.jpg)
.files/image398.jpg)
.files/image400.jpg)
28.(16分)
(1).files/image402.gif) 2分 沸腾炉1分
2分 沸腾炉1分
(2)氯酸钾 (或.files/image404.gif) ) 1分 镁条(或
) 1分 镁条(或.files/image406.gif) ) 1分
) 1分
(3).files/image408.gif) 2分
2分
防止产生的.files/image234.gif) 和
和.files/image059.gif) 混和发生爆炸 1分 ,避免
混和发生爆炸 1分 ,避免.files/image234.gif) 和
和.files/image413.gif) 反应,使生成的
反应,使生成的.files/image413.gif) 不纯1分
不纯1分
(4).files/image416.gif) 2分
2分
(5)I.不合理(1分),该反应为放热反应,升高温度会降低.files/image243.gif) 的产率,但温度过低,
的产率,但温度过低,
反应速率很小,经济效益较低。因此,应选择适当的温度。(2分)
29.(15分)
(1)增大铜粉与氧接触面积,使反应迅速、充分(2分)
(2).files/image419.gif) (1分) 排出D中的空气(1分) 关闭
(1分) 排出D中的空气(1分) 关闭.files/image256.gif) (1分) 打开
(1分) 打开.files/image422.gif) (1分)
(1分)
(3)锥形瓶中玻璃管液面上升(1分)
(4).files/image424.gif) (2分)
(2分)
(5)向下调节量气管(或及时关闭.files/image256.gif) ) (1分,其他合理答案也可给分)
) (1分,其他合理答案也可给分)
(6)I.0.0720.files/image427.gif) (2分)
(2分)
Ⅱ.有(1分) E装置中生成100mL、0.0720 .files/image427.gif) 硝酸时产生的
硝酸时产生的.files/image429.gif) 约为80.6mL,而
约为80.6mL,而
试管中原有50mL.files/image419.gif) ,二者之和小于139.00mL,说明生成
,二者之和小于139.00mL,说明生成.files/image432.gif) 的同时有NO生成(2分)
的同时有NO生成(2分)
30.(24分)I(8分,每空2分)
J 天敌 竞争 抵抗力
Ⅱ(16分)
(1)原因:肝细胞利用保存液中葡萄糖有氧呼吸(2分),线粒子体产生的.files/image267.gif) 扩散进入细
扩散进入细
胞质基质中。(1分)改进措施:用不含葡萄糖的保存液(2分)
(2)胰蛋白(2分) (3)结构的完整性(2分)
(4)丙铜酸进一步分解的产物有.files/image267.gif) (2分),检验是否有
(2分),检验是否有.files/image267.gif) 产生可判断丙铜酸是否被
产生可判断丙铜酸是否被
分解。(2分)
(5)分别给1号和2号试管设空白对照组1’和2’,(1分) 1’和2’试管所装物质分
别与1号和2号相同,只是下一步不加入丙铜酸(1分),而加入生理盐水。(1分)
31.(18分)(除(2)②小题每空3分外,其余每空2分)
(1)①.files/image437.gif) ②
②.files/image439.gif) ③
③.files/image441.gif)
(2)①雄鸡全为芦花,雌鸡全为非芦花 ②雌鸡全为芦花,雄鸡有芦花与非芦花两中雌鸡
和雄鸡均有芦花与非芦花两种
(3).files/image443.gif) 在雏鸡阶段淘汰绒羽为黑色且头顶有黄
在雏鸡阶段淘汰绒羽为黑色且头顶有黄
色斑点的个体,其于个体全部保留饲养
.files/image445.gif) www.ks5u.com
www.ks5u.com
(10分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中C02的含量及有效地开发利用CO2,引起了各国的普遍重视。
(1)下列关于C02的用途不正确的是 (填序号)。
A.二氧化碳能溶于水,可用于生产碳酸型饮料
B.固体二氧化碳俗称干冰,可用于人工降雨
C.二氧化碳用于灭火是因为降低了可燃物的着火点
D.超临界二氧化碳作萃取溶剂用于从天然产物提取和净化活性组分
E.二氧化碳可以作为气肥,提高农作物的产量
(2)目前工业上有一种方法是用C02来生产甲醇。为探究其反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:C02(g)+
3 H2(g) ![]() CH30H(g)+H20(g) ΔH=-49.0kJ.m01-1,测得C02和CH3OH(g)的浓度随时间变化如图所示。
CH30H(g)+H20(g) ΔH=-49.0kJ.m01-1,测得C02和CH3OH(g)的浓度随时间变化如图所示。
①从反应开始到平衡,氢气的平均反应速率:v(H。)= 。
②该反应的平衡常数为 。
(3)以KHC03溶液为电解质,用电解的方法也可以将C02还原为甲醇。请写出电解时阴极的离子方程式:
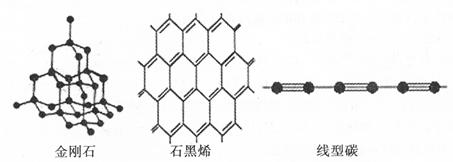
(4)金刚石、石墨烯、线型碳是碳的几种同素异形体。从键的类型分析它们的稳定性由强到弱的顺序为
查看习题详情和答案>>
(10分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中C02的含量及有效地开发利用CO2,引起了各国的普遍重视。
(1)下列关于C02的用途不正确的是 (填序号)。
A.二氧化碳能溶于水,可用于生产碳酸型饮料
B.固体二氧化碳俗称干冰,可用于人工降雨
C.二氧化碳用于灭火是因为降低了可燃物的着火点
D.超临界二氧化碳作萃取溶剂用于从天然产物提取和净化活性组分
E.二氧化碳可以作为气肥,提高农作物的产量
(2)目前工业上有一种方法是用C02来生产甲醇。为探究其反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:C02(g)+
3 H2(g) 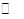 CH30H(g)+H20(g)
ΔH=-49.0kJ.m01-1,测得C02和CH3OH(g)的浓度随时间变化如图所示。
CH30H(g)+H20(g)
ΔH=-49.0kJ.m01-1,测得C02和CH3OH(g)的浓度随时间变化如图所示。

①从反应开始到平衡,氢气的平均反应速率:v(H。)= 。
②该反应的平衡常数为 。
(3)以KHC03溶液为电解质,用电解的方法也可以将C02还原为甲醇。请写出电解时阴极的离子方程式:
(4)金刚石、石墨烯、线型碳是碳的几种同素异形体。从键的类型分析它们的稳定性由强到弱的顺序为

查看习题详情和答案>>
(1)氢能在二十一世纪有可能在世界能源舞台上成为一种举足轻重的二次能源。
①硫-碘循环分解水制氢主要涉及下列反应:
I.SO2+2H2O+ I2=H2SO4+2HI
Ⅱ.2HI
 H2+I2
H2+I2 Ⅲ.2H2SO4=2SO2+O2+2H2O
分析上述反应,下列判断正确的是_________(填序号,下同)。
a.反应Ⅲ易在常温下进行
b.反应I中SO2氧化性比HI强
c.循环过程中需补充H2O
d.循环过程中产生1 mol O2的同时产生1 mol H2
②利用甲烷与水反应制备氢气,因原料价廉产氢率高,具有实用推广价值,已知该反应为:
CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH =+206.1 kJ·mol-1
若800℃时,反应的平衡常数K1=1.0,某时刻测得该温度下,密闭容器中各物质的物质的量浓度分别为:c(CH4)=3.0 mol·L-1;c(H2O)=8.5 mol·L-1;c(CO)=2.0 mol·L-1;c(H2)=2.0 mol·L-1,则此时正逆反应速率的关系是v正___________(填“>”、“<”或“=”) v逆。
③实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡____________移动(填“向左”、“向右”或“不”);若加入少量下列试剂中的_____________,产生H2的速率将增大。
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇: CO(g)+2H2(g)
 CH3OH(g) 分析该反应并回答下列问题:
CH3OH(g) 分析该反应并回答下列问题: ①下列各项中,不能说明该反应已达到平衡的是______________。
a.恒温、恒容条件下,容器内的压强不发生变化
b.一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
c.一定条件下,CO、H2和CH3OH的浓度保持不变
d.一定条件下,单位时间内消耗1 mol CO,同时生成l mol CH3OH
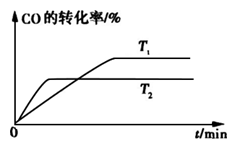
②如图是该反应在不同温度下CO的转化率随时间变化的曲线。
③已知甲醇燃料电池的工作原理如图所示。

(1)氢能在二十一世纪有可能在世界能源舞台上成为一种举足轻重的二次能源.
①硫-碘循环分解水制氢主要涉及下列反应:
I.SO2+2H2O+I2=H2SO4+2HIⅡ.2HI
 H2+I2Ⅲ.2H2SO4=2SO2+O2+2H2O
H2+I2Ⅲ.2H2SO4=2SO2+O2+2H2O分析上述反应,下列判断正确的是______(填序号,下同).
a.反应Ⅲ易在常温下进行 b.反应I中SO2氧化性比HI强
c.循环过程中需补充H2O d.循环过程中产生l mol O2的同时产生1mol H2
②利用甲烷与水反应制备氢气,因原料价廉产氢率高,具有实用推广价值,已知该反应为:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.1kJ?mol-1若800℃时,反应的平衡常数K1=1.0,某时刻测得该温度下,密闭容器中各物质的物质的量浓度分别为:c(CH4)=3.0mol?L-1;c(H2O)=8.5mol?L-1;c(CO)=2.0mol?L-1;c(H2)=2.0mol?L-1,则此时正逆反应速率的关系是v正______v逆.(填“>”、“<”或“=”)
③实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡______移动(填“向左”、“向右”或“不”);若加入少量下列固体试剂中的______,产生H2的速率将增大.
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)
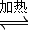 CH3OH(g)分析该反应并回答下列问题:
CH3OH(g)分析该反应并回答下列问题:①下列各项中,不能说明该反应已达到平衡的是______.
a.恒温、恒容条件下,容器内的压强不发生变化
b.一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
c.一定条件下,CO、H2和CH3OH的浓度保持不变
d.一定条件下,单位时间内消耗1mol CO,同时生成l mol CH3OH
②如图甲是该反应在不同温度下CO的转化率随时间变化的曲线.T1和T2温度下的平衡常数大小关系是K1______ K2.(填“>”、“<”或“=”)
③已知甲醇燃料电池的工作原理如图乙所示.
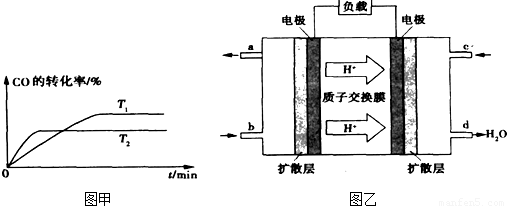
①该电池工作时,b口通入的物质为______,该电池正极的电极反应式为:______,工作一段时间后,当6.4g甲醇(CH3OH)完全反应生成CO2时,有______mol电子发生转移.
查看习题详情和答案>>
(1)下列关于C02的用途不正确的是 (填序号)。
| A.二氧化碳能溶于水,可用于生产碳酸型饮料 |
| B.固体二氧化碳俗称干冰,可用于人工降雨 |
| C.二氧化碳用于灭火是因为降低了可燃物的着火点 |
| D.超临界二氧化碳作萃取溶剂用于从天然产物提取和净化活性组分 |
(2)目前工业上有一种方法是用C02来生产甲醇。为探究其反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-49.0kJ.m01-1,测得C02和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0kJ.m01-1,测得C02和CH3OH(g)的浓度随时间变化如图所示。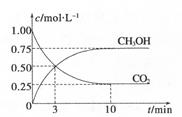
①从反应开始到平衡,氢气的平均反应速率:v(H。)= 。
②该反应的平衡常数为 。
(3)以KHC03溶液为电解质,用电解的方法也可以将CO2还原为甲醇。请写出电解时阴极的离子方程式:
(4)金刚石、石墨烯、线型碳是碳的几种同素异形体。从键的类型分析它们的稳定性由强到弱的顺序为