网址:http://m.1010jiajiao.com/timu_id_50022[举报]
一、

17.(每小题2分,共8分)(1)极性,非极性;(2)Mg,C;(3)C+4HNO3(浓) CO2↑+4NO2↑+2H2O
(4)2NO2=N2O4
18.(每小题2分,共8分)
(1)H C
(2)NH4+ +H2O NH3•H2O + H+
NH3•H2O + H+
(3)c (Na+)>c (HCO3-)>c (CO32-)>c (OH-)>c (H+)
(4)4NH3(g)+3O2(g)=2N2(g)+6H2O(l);ΔH=-1264.8 kJ/mol(2分)
19.(3分)②⑧
20.(共10分)(1)仪器连接好后,将止水夹夹紧,在A中加入水使U型管左右两边管中产生液面差,一段时间后,U型管中左右两边管中的液面未发生变化(3分,其他合理答案也给分)
(2)①(2分) ;③(2分)。(3)取pH=3的乙酸溶液加入蒸馏水稀释100倍,用pH试纸测定溶液的pH小于5(3分)。
21.(共9分)
(1) ①④ (2分)(2)(a)①③ (2分)(b) (2分)
(2分)
 (3)
(3)
(3分)
22.(14分)(1)AB (2)0.1mol.L-1.min-1 14.3% (3)A D (4)向右 增大 (5)80%
下图实验装置示意图中A是简易的H2发生器,B是大小适宜的的圆底烧瓶,C是装有干燥剂的U形管。A是旋转活塞,D是装有还原铁粉的反应管,E是装有酚酞的试管。实验前先检查装置的气密性。实验开始时,先关闭活塞a,并取下烧瓶B;向A制加入一定量浓度适当的盐酸,产生H2。:经必要的“操作”后,在导管口处点燃H2,然后如图所示套上烧瓶B,塞紧烧瓶,H2在烧瓶中继续燃烧,用酒精灯加热反应管D中的还原铁粉,待B中H2的火焰熄灭后,打开活塞a,气体通过反应管D进入烧杯E中,使酚酞试液呈红色。
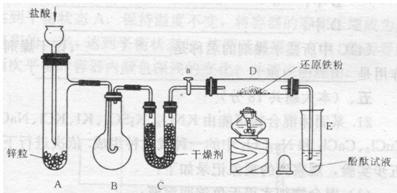
请回答下列问题。
(1)实验前如何检查整套装置的气密性? 。
(2)题干中必要操作步骤指的是
(3)操作中先加热D后打开a的目的是
(4)写出B、D中分别发生反应的化学方程式:B中 ,
D中 。
(5)C中的干燥剂的名称是 ,该干燥剂的作用是 。
查看习题详情和答案>>(14分)某同学用图示装置进行铁和稀硝酸反应的实验并进行相关的实验探究。
a.向广口瓶内注入足量热NaOH溶液,将盛有一定质量的纯铁粉的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸人瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中缓慢滴入一定量的4mol·L-1的稀硝酸,
铁粉完全溶解。
(一)气体产物成分探究
(1)实验前如何检查该装置的气密性? 。
(2)燃烧红磷的目的是 。
(3)为证明气体产物为NO,步骤c后还缺少的一步主要操作是 。
(二)产物中铁元素价态探究:
(1)提出合理假设:
假设1:产物中只有+2价铁;假设2: ,假设3:产物中既有+2价铁,又有+3价铁。
(2)设计实验方案,验证假设1成立(写出实验操作步骤、现象和结论): 。
(三)问题讨论
(1)广口瓶中热NaOH溶液的主要作用是 。
(2)若假设3成立,且所得溶液中n(Fe2+):n(Fe3+)=3:1时,则对应的离子反应方程式为 。
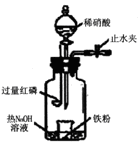
a.向广口瓶内注入足量热NaOH溶液,将盛有一定质量的纯铁粉的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸人瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中缓慢滴入一定量的4mol·L-1的稀硝酸,
铁粉完全溶解。
(一)气体产物成分探究
(1)实验前如何检查该装置的气密性? 。
(2)燃烧红磷的目的是 。
(3)为证明气体产物为NO,步骤c后还缺少的一步主要操作是 。
(二)产物中铁元素价态探究:
(1)提出合理假设:
假设1:产物中只有+2价铁;假设2: ,假设3:产物中既有+2价铁,又有+3价铁。
(2)设计实验方案,验证假设1成立(写出实验操作步骤、现象和结论): 。
(三)问题讨论
(1)广口瓶中热NaOH溶液的主要作用是 。
(2)若假设3成立,且所得溶液中n(Fe2+):n(Fe3+)=3:1时,则对应的离子反应方程式为 。
有下列实验装置:
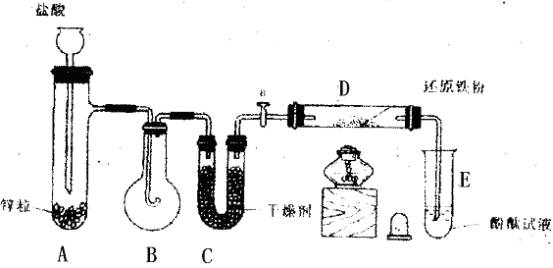
示意图中A是简易的氢气发生器,B是大小适宜的圆底烧瓶,C是装有干燥剂的U形管,a是旋转活塞,D是装有还原铁粉的反应管,E是装有酚酞试液的试管。
实验前先检查实验装置的气密性。实验开始时,先关闭活塞a,并取下烧瓶B;向A中加入一定量浓度适当的盐酸,发生氢气。经必要的“操作”[见问题(2)]后,在导管的出口处点燃氢气,然后如图所示套上烧瓶B,塞紧瓶塞,氢气在烧瓶中继续燃烧。用酒精灯加热反应管D中的还原铁粉,待B中氢气的火焰熄灭后,打开活塞a,气体通过反应管D进入试管E中,使酚酞试液呈红色;请回答下列问题。
(1)实验前如何检查装置的气密性?
(2)点燃氢气前必须进行操作 ,进行该操作的方法是 。
(3)写出B、D中分别发生的化学反应方程式:
B中:
D中:
(4)C中所盛干燥剂的名称是 ;该干燥剂的作用是 。
查看习题详情和答案>>
有下列实验装置:
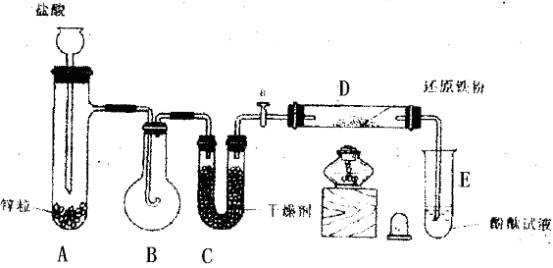
示意图中A是简易的氢气发生器,B是大小适宜的圆底烧瓶,C是装有干燥剂的U形管,a是旋转活塞,D是装有还原铁粉的反应管,E是装有酚酞试液的试管。
实验前先检查实验装置的气密性。实验开始时,先关闭活塞a,并取下烧瓶B;向A中加入一定量浓度适当的盐酸,发生氢气。经必要的“操作”[见问题(2)]后,在导管的出口处点燃氢气,然后如图所示套上烧瓶B,塞紧瓶塞,氢气在烧瓶中继续燃烧。用酒精灯加热反应管D中的还原铁粉,待B中氢气的火焰熄灭后,打开活塞a,气体通过反应管D进入试管E中,使酚酞试液呈红色;请回答下列问题。
(1)实验前如何检查装置的气密性?
(2)点燃氢气前必须进行操作 ,进行该操作的方法是 。
(3)写出B、D中分别发生的化学反应方程式:
B中:
D中:
(4)C中所盛干燥剂的名称是 ;该干燥剂的作用是 。
查看习题详情和答案>>