网址:http://m.1010jiajiao.com/timu_id_499270[举报]
1.D 2.A 3.A 4.C 5.C 6.AC 7.D 8.D 9.BD 10.AB 11.B
12.D 13.B 14.B 15.A 16.B 17.B 18.B 19.A 20.B 21.C 22.D
23.(1)< (2)右侧的3处
(3)< B相当于减压了,减压后平衡向 分解的方向移动,使B中
分解的方向移动,使B中 的量减少了.
的量减少了.
24.①提高,降低;②b=4;③ ;④
;④ 或
或 或ac+bc=ab
或ac+bc=ab
25.(1)B.根据反应:

 ,
,

 ,若要充分利用原料,显然要求原料与
,若要充分利用原料,显然要求原料与 反应产生的
反应产生的 和
和 物质的量之比等于或接近于3∶1,上述反应趋于恰好反应,原料得以充分利用.
物质的量之比等于或接近于3∶1,上述反应趋于恰好反应,原料得以充分利用. w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m




(2)①

 ②不合理.因为BiOCl中,Cl的化合价为-1价.③浓NaOH溶液中,
②不合理.因为BiOCl中,Cl的化合价为-1价.③浓NaOH溶液中, 抑制
抑制 的溶解,使
的溶解,使 的浓度减小,盐酸中
的浓度减小,盐酸中 抑制
抑制 的水解.
的水解.
26.(1)2、1、3、2 (2)A为气态,B为固态或气态,D为气态 (3)放热
27.(1)按1分钟计,生成0.5 mol C产生热量45 kJ,而容器散热
 ,所以应用加热器每分钟提供热量120
kJ-45 kJ=75 kJ
,所以应用加热器每分钟提供热量120
kJ-45 kJ=75 kJ
(2)容器半径和高度都变为原来10倍,则表面变为原来1000倍,平均每分钟生成C为0.5 mol×1000=500 mol,放出热量45000kJ,而容器散热12000 kJ,所以冷却器每分钟吸收热量45000 kJ-12000 kJ=33000 kJ
(3)不变
28.a=1 b=2
29.(1) (2)1/10500 (3)10
(2)1/10500 (3)10
30.①39% ②12.5% 31.(1)① 体积
体积
②当活塞由C向B移动时,因体积扩大使平衡:

 向体积扩大方向移动以至混合气体物质的量增大.增大的物质的量可由下式求出
向体积扩大方向移动以至混合气体物质的量增大.增大的物质的量可由下式求出



起始:0.08 mol 0
平衡:

因平衡时混合气体总的物质的量为0.07 mol,由于活塞由C移至B,体积扩大,故 ,可知充入
,可知充入 物质的量必小于0.01
mol
(2)
物质的量必小于0.01
mol
(2)
 www.ks5u.com
www.ks5u.com
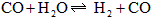 若起始浓度
若起始浓度[CO]为
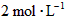 、[
、[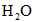 ]为
]为 ,反应达平衡时,
,反应达平衡时,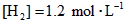 ;如果[CO]不变而将
;如果[CO]不变而将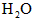 的起始浓度加大到
的起始浓度加大到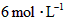 。则平衡时
。则平衡时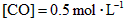 。
。请注意上述有关数据,总结出其中的规律,根据此规律,填写以下空白:
设830 K时,起始浓度[CO]为
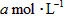 ,[
,[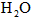 ]为
]为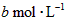 ,反应达平衡时[
,反应达平衡时[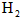 ]为
]为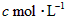
(1)当b不变,a减小,重新达平衡时,CO的转化率________,
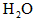 的转化率________(均填“提高”、“降低”或“不变”)
的转化率________(均填“提高”、“降低”或“不变”) (2)当a=5,
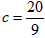 时,b=________;
时,b=________; (3)当a=b时
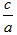 =________;
=________; (4)当b=4,c=2时,a= _________;
(5)用以表示a、b、c之间关系的代数式为:_________。
 CO2(g)+H2(g),若起始浓度co(CO)=2mol?L-1,co(H2O)=3mol?L-1,反应平衡时CO的转化率α(CO)=60%,如果将H2O的起始浓度加大到6mol?L-1,则CO的转化率α(CO)=75%。请注意上述有关数据,总结出其中的规律,填写以下空白:
CO2(g)+H2(g),若起始浓度co(CO)=2mol?L-1,co(H2O)=3mol?L-1,反应平衡时CO的转化率α(CO)=60%,如果将H2O的起始浓度加大到6mol?L-1,则CO的转化率α(CO)=75%。请注意上述有关数据,总结出其中的规律,填写以下空白:设830K时,起始浓度co(CO)=amol?L-1,co(H2O)=bmol?L-1,达平衡时[H2]=cmol?L-1。
(1)当b不变、a减小时,重新达到平衡,则α(CO)_____(填“增大”、“减小”或“不变”,下同);α(H2O)______。
(2)当a=5、c=20/9时,b=________。
(3)当a=b时,c/a=________。
(4)用以表示a、b、c之间的关系的代数式为____。 查看习题详情和答案>>
 CO2(g)+H2(g),达到平衡时,K=
CO2(g)+H2(g),达到平衡时,K=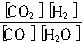 ,K是常数,只与温度有关,与浓度无关。
,K是常数,只与温度有关,与浓度无关。(1)830K时,若起始时,c0(CO)=2mol?L-1、c0(H2O)=3mol?L-1,平衡时CO的转化率为60%,水蒸气的转化率为________;K值为_______。
(2)830K,若只将起始时的c0(H2O)改为6mol?L-1,则水蒸气的转化率为____________。
(3)若830K时,起始浓度c0(CO)=amol?L-1、c0(H2O)=bmol?L-1,H2的平衡浓度[H2]=cmol?L-1。
①a、b、c之间的关系式是________;
②当a=b时,a= _____c。 查看习题详情和答案>>