题目内容
在温度为830K时,下述可逆反应及其平衡具有某些特殊性:CO(g)+H2O(g) CO2(g)+H2(g),若起始浓度co(CO)=2mol?L-1,co(H2O)=3mol?L-1,反应平衡时CO的转化率α(CO)=60%,如果将H2O的起始浓度加大到6mol?L-1,则CO的转化率α(CO)=75%。请注意上述有关数据,总结出其中的规律,填写以下空白:
CO2(g)+H2(g),若起始浓度co(CO)=2mol?L-1,co(H2O)=3mol?L-1,反应平衡时CO的转化率α(CO)=60%,如果将H2O的起始浓度加大到6mol?L-1,则CO的转化率α(CO)=75%。请注意上述有关数据,总结出其中的规律,填写以下空白:设830K时,起始浓度co(CO)=amol?L-1,co(H2O)=bmol?L-1,达平衡时[H2]=cmol?L-1。
(1)当b不变、a减小时,重新达到平衡,则α(CO)_____(填“增大”、“减小”或“不变”,下同);α(H2O)______。
(2)当a=5、c=20/9时,b=________。
(3)当a=b时,c/a=________。
(4)用以表示a、b、c之间的关系的代数式为____。
解析:设总体积为1L,在830K时,可逆反应:CO(g)+H2O(g) CO2(g)+H2(g),当α(CO)=60%时,即有2mol?L-1×1L×60%=1.2molCO参加了反应,必有1.2molH2O同时参加反应,
CO2(g)+H2(g),当α(CO)=60%时,即有2mol?L-1×1L×60%=1.2molCO参加了反应,必有1.2molH2O同时参加反应,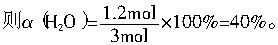
当α(CO)=75%时,则有2mol?L-1×1L×75%=1.5molCO参加了反应,也有1.5molH2O同时参加了反应,即α(H2O)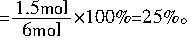
从中可以看出,增加c(H2O)时,α(CO)升高(60%→75%,升高了15%),而α(H2O)降低(40%→25%,降低了15%),并且符合60%+40%=100%,75%+25%=100%。
由此可得出此题中的“某些规律”:
①增大一种反应物的浓度,则该物质的转化率降低,而使另一种反应物的转化率升高,且升高率与该物质的转化率降低率相等。那么第(1)问则为:当b不变、a减小时,α(CO)增大,α(H2O)减小。
②各反应物的转化率之和总为100%。若用代数式表示则为: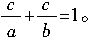
这就是第(4)问的答案。再将第(2)问和第(3)问的有关数据代入即得:(2)当a=5、c=20/9时,b=4;(3)当a=b时,c/a=0.5。
【试题分析】

练习册系列答案
相关题目
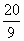 时,b=________.
时,b=________.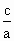 =________.
=________.