摘要:2.乙烯 (1)乙烯的燃烧 实验:点燃纯净的乙烯.观察乙烯燃烧时的现象. 现象与解释:乙烯在空气中燃烧.火焰明亮.并伴有黑烟.乙烯中碳的质量分数较高.燃烧时有黑烟产生. (2)乙烯使KMnO4酸性溶液褪色 实验:把乙烯通入盛有KMnO4酸性溶液的试管里.观察试管里溶液颜色的变化. 现象与解释:KMnO4酸性溶液的紫色褪去.说明乙烯能被氧化剂KMnO4氧化.它的化学性质比烷烃活泼. (3)乙烯使溴的四氯化碳溶液褪色 实验:把乙烯通入盛有溴的四氯化碳溶液的试管里.观察试管里溶液颜色的变化. 现象与解释:溴的红棕色褪去.说明乙烯与溴发生了反应.
网址:http://m.1010jiajiao.com/timu_id_498332[举报]
乙烯的产量可以用来衡量一个国家的石油化工发展水平.请回答:
(1)乙烯的电子式是
 .
.
(2)可以用来鉴别甲烷和乙烯的试剂是
A.水 B. 稀硫酸 C.溴的四氯化碳溶液 D.酸性高锰酸钾溶液
(3)在一定条件下,乙烯能与水反应生成有机物A. A的结构简式是
(4)同学们在学习A的知识后,设计了如下两个实验.
方案Ⅰ:在盛有少量无水A的试管中,加入一粒除去煤油的金属钠,在试管口迅速塞上配有尖嘴导管的单孔塞,点燃放出的气体,并把一干燥的小烧杯罩在火焰上,在烧杯壁上出现液滴后,迅速倒转烧杯,向烧杯中加入少量的澄清石灰水,观察有无混浊产生.
①请写出A与钠反应的化学方程式:
②以上实验设计因缺少必要的步骤而存在安全隐患,请你指出所缺少必要的步骤是
③若向烧杯中加入少量澄清石灰水后发现有混浊,则燃烧产生CO2的物质最可能是
方案Ⅱ:
a、在试管里加入2mL A;
b、把一端弯成螺旋状的铜丝放在酒精灯外焰中加热;
c、立即将铜丝插入盛有A的试管里,反复操作几次;
d、闻生成物的气味,观察铜丝表面的变化.
①该实验的目的是
②第④步操作中,铜丝表面的变化是
③写出该反应总的化学方程式
查看习题详情和答案>>
(1)乙烯的电子式是


(2)可以用来鉴别甲烷和乙烯的试剂是
CD
CD
.A.水 B. 稀硫酸 C.溴的四氯化碳溶液 D.酸性高锰酸钾溶液
(3)在一定条件下,乙烯能与水反应生成有机物A. A的结构简式是
CH3CH2OH
CH3CH2OH
.(4)同学们在学习A的知识后,设计了如下两个实验.
方案Ⅰ:在盛有少量无水A的试管中,加入一粒除去煤油的金属钠,在试管口迅速塞上配有尖嘴导管的单孔塞,点燃放出的气体,并把一干燥的小烧杯罩在火焰上,在烧杯壁上出现液滴后,迅速倒转烧杯,向烧杯中加入少量的澄清石灰水,观察有无混浊产生.
①请写出A与钠反应的化学方程式:
2Na+2CH3CH2OH═2CH3CH2ONa+H2↑
2Na+2CH3CH2OH═2CH3CH2ONa+H2↑
.②以上实验设计因缺少必要的步骤而存在安全隐患,请你指出所缺少必要的步骤是
点燃放出的气体之前没有检验纯度
点燃放出的气体之前没有检验纯度
.③若向烧杯中加入少量澄清石灰水后发现有混浊,则燃烧产生CO2的物质最可能是
乙醇蒸气
乙醇蒸气
(写名称).方案Ⅱ:
a、在试管里加入2mL A;
b、把一端弯成螺旋状的铜丝放在酒精灯外焰中加热;
c、立即将铜丝插入盛有A的试管里,反复操作几次;
d、闻生成物的气味,观察铜丝表面的变化.
①该实验的目的是
乙醇的催化氧化反应
乙醇的催化氧化反应
;②第④步操作中,铜丝表面的变化是
铜丝表面由黑色变为红色
铜丝表面由黑色变为红色
;③写出该反应总的化学方程式
2CH3CH2OH+O2
2CH3CHO+2H2O
| Cu |
| △ |
2CH3CH2OH+O2
2CH3CHO+2H2O
.| Cu |
| △ |
测定有机物中碳和氢的质量分数,常用燃烧分析法,在750°C左右使有机物在氧气流中全部氧化成CO2和H2O;分别用装有固体NaOH和Mg(ClO4)2的吸收管吸收CO2和H2O.某课外活动小组,设计利用如图所示装置取纯净的乙烯,并测定乙烯分子中碳、氢原子的个数比;甲为燃烧管,当乙烯和氧气通过时,由于催化剂的存在而不会发生爆炸,乙烯被氧化成CO2和H2O.请回答下列问题: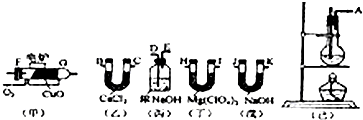
(1)已知整套装置的连接顺序(按气流方向从左到右填写仪器的接口字母):A接D,E接B,C接F,G接H,I接J…则丙装置的作用 .丁装置的作用 甲装置中CuO的作用是
(2)烧瓶中发生反应的化学方程式是:
(3)实验时应使烧瓶中溶液的温度迅速升至170°C,原因是 ;
(4)若测得的比值偏高,导致这种误差的可能的原因是 .
A.乙烯中混有少量的乙醚(C2H5OC2H5)
B.乙烯进入燃烧管时,含有少量的水蒸气
C.乙烯中混有少量的CO
D.乙烯进入燃烧管时,含有少量的CO2
(5)若准确称取0.90g样品(只含C、H、O三种元素中的两种或三种)经充分燃烧后,戊质量增加1.32g,丁质量增加0.54g,则该有机物的最简式为 .
查看习题详情和答案>>
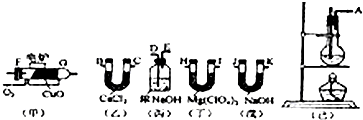
(1)已知整套装置的连接顺序(按气流方向从左到右填写仪器的接口字母):A接D,E接B,C接F,G接H,I接J…则丙装置的作用
(2)烧瓶中发生反应的化学方程式是:
(3)实验时应使烧瓶中溶液的温度迅速升至170°C,原因是
(4)若测得的比值偏高,导致这种误差的可能的原因是
A.乙烯中混有少量的乙醚(C2H5OC2H5)
B.乙烯进入燃烧管时,含有少量的水蒸气
C.乙烯中混有少量的CO
D.乙烯进入燃烧管时,含有少量的CO2
(5)若准确称取0.90g样品(只含C、H、O三种元素中的两种或三种)经充分燃烧后,戊质量增加1.32g,丁质量增加0.54g,则该有机物的最简式为
(13分)乙醇在实验中用途广泛。
(1)下图为实验室用乙醇制取乙烯并与溴水作用制取1,2—二溴乙烷的部分装置图,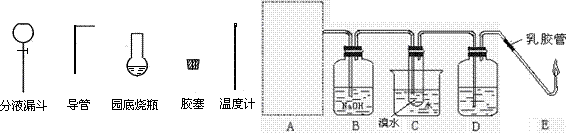
①请选用左图实验仪 器示意图在方框内画出乙烯的发生装置(夹持装置不必画出,需要加热的仪器下方用△标出)。
器示意图在方框内画出乙烯的发生装置(夹持装置不必画出,需要加热的仪器下方用△标出)。
②B和D装置都盛有NaOH溶液,它们的作用是:B ____ __、D_________________。
③试写出以乙醇、浓硫酸、溴水为主要原料制取1,2—二溴乙烷的主要化学反应方程式。
_________________________________________________
_________________________________________________
④实验室用E图装置点燃乙烯,燃烧时 会产生黑烟,实验时若要迅速熄灭火焰,最简单、安全的操作方法是: 。
会产生黑烟,实验时若要迅速熄灭火焰,最简单、安全的操作方法是: 。
(2)实验室可用C2H518OH和乙酸按图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)
请填空:
①写 出实验室制乙酸乙酯的化学方程式(要标出氧-18示踪原子)
出实验室制乙酸乙酯的化学方程式(要标出氧-18示踪原子)
_______________________________________________________
②实验中加热试管的目的是:
③试管b中加有饱和Na2CO3溶液,其作用是
④反应结束后,振荡试管b静置,观察到的现象是