摘要:21.放热 (2) “减小 平衡逆向移动 (3)否.反应热由始末状态决定.(4)减小.减小.
网址:http://m.1010jiajiao.com/timu_id_453381[举报]
 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.(1)该反应是
放热
放热
(填“吸热”“放热”)反应.(2)当反应达到平衡时,升高温度,A的转化率
减小
减小
(填“增大”“减小”或“不变”),原因是该反应正反应为放热反应,升高温度使平衡向逆反应方向移动
该反应正反应为放热反应,升高温度使平衡向逆反应方向移动
.(3)反应体系中加入催化剂对反应热是否有影响并说明原因
不影响;催化剂不改变平衡的移动
不影响;催化剂不改变平衡的移动
.(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:?E1
减小
减小
,E2减小
减小
(填“增大”“减小”或“不变”).平衡向不会
不会
移动. 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题:
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题:(1)该反应是
放热
放热
反应(填“吸热”“放热”);△H<
<
(填“<0”或“>0”).(2)当反应达到平衡时,升高温度,A的转化率
减小
减小
(填“增大”“减小”“不变”),原因是该反应正反应为放热反应,升高温度使平衡向逆反应方向移动
该反应正反应为放热反应,升高温度使平衡向逆反应方向移动
.(3)反应体系中加入催化剂对反应热是否有影响?
不影响,催化剂不改变平衡的移动
不影响,催化剂不改变平衡的移动
.(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
减小
减小
,E2减小
减小
(填“增大”“减小”、“不变”).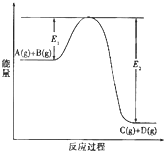 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.(1)该反应是
(2)当反应达到平衡时,升高温度,正反应速率变化是
(3)在该反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
(1)合成氨反应N2(g)+3H2(g)?2NH3(g),若在恒温、恒压条件下,向平衡体系中通入氩气,平衡
(2)一定温度下,在恒容密闭容器中N2O5可发生化学反应:2N2O5(g)?4NO2(g)+O2(g)△H>0
①下表为反应T1温度下的部分实验数据:
则500s内N2O5的分解速率为
②在T2温度下,反应1000s时测得NO2的浓度为4.98mol?L-1,则T2
(3)已知肼分子(H2N-NH2)可以在氧气中燃烧生成氮气和水.
①利用肼、氧气与KOH溶液组成碱性燃料电池,请写出电池负极的电极反应式
②用电离方程式表示肼的水溶液呈碱性的原因
③肼是强还原剂,与氧化剂反应时放出大量的热,如:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-642.2kJ?mol-1因此肼可以作为火箭推进剂.根据上述信息,你认为是否可以通过改变反应条件,由氮气和水蒸气来制取肼
查看习题详情和答案>>
(1)合成氨反应N2(g)+3H2(g)?2NH3(g),若在恒温、恒压条件下,向平衡体系中通入氩气,平衡
向左
向左
移动(填“向左”“向右”或“不”);使用催化剂后反应的△H(填“增大”“减小”或“不改变”)不改变
不改变
.(2)一定温度下,在恒容密闭容器中N2O5可发生化学反应:2N2O5(g)?4NO2(g)+O2(g)△H>0
①下表为反应T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| C(N2O5)/mol?L-1 | 5.00 | 3.52 | 2.48 |
0.00296 mol?L-1?S-1
0.00296 mol?L-1?S-1
.②在T2温度下,反应1000s时测得NO2的浓度为4.98mol?L-1,则T2
<
<
T1(填“>”“<”“=”)(3)已知肼分子(H2N-NH2)可以在氧气中燃烧生成氮气和水.
①利用肼、氧气与KOH溶液组成碱性燃料电池,请写出电池负极的电极反应式
N2H4-4e-+4OH-=N2+4H2O
N2H4-4e-+4OH-=N2+4H2O
;②用电离方程式表示肼的水溶液呈碱性的原因
H2N-NH2?H2O?H2N-NH3++OH-
H2N-NH2?H2O?H2N-NH3++OH-
③肼是强还原剂,与氧化剂反应时放出大量的热,如:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-642.2kJ?mol-1因此肼可以作为火箭推进剂.根据上述信息,你认为是否可以通过改变反应条件,由氮气和水蒸气来制取肼
不可以
不可以
.说明原因因为该反应的逆反应是吸热反应,即△H>0,且熵减小,属于不自发反应,故不能用氮气和水来制取肼
因为该反应的逆反应是吸热反应,即△H>0,且熵减小,属于不自发反应,故不能用氮气和水来制取肼
.在体积为1L的两个恒容密闭容器中,分别充入1molCO和1molH2O(g)的混合气体,进行如下化学反应:CO(g)+H2O(g)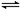 CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
| | 0min | 10min | 20min | 30min | 40min | 50min |
| 830℃ | 1mol | 0.8mol | 0.65mol | 0.55mol | 0.5mol | 0.5mol |
| 1100℃ | 1mol | 0.75mol | 0.6mol | 0.6mol | 0.6mol | 0.6mol |
(2)1100℃时化学平衡常数K=_______,该反应为________反应(填“吸热”和“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是____________________。
(a)容器中压强不变 (b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O) (d)c(CO2)=c(CO)
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),平衡_____________________移动(选填“向正反应方向”或“向逆反应方向”或“不”),再达到平衡时,H2百分含量________________(选填“增大”或“减小”或“不变”)。
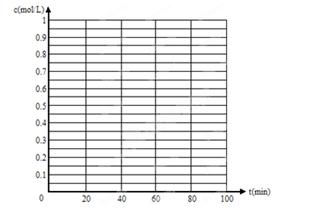
(5)830℃时,若在体积为2L的密闭容器中充入1molCO2和1molH2的混合气体,60min时反应达平衡状态,画出c(CO)和c(H2)随时间变化而变化的趋势图。
 查看习题详情和答案>>
查看习题详情和答案>>