网址:http://m.1010jiajiao.com/timu_id_4449978[举报]
(10分)甲酸甲酯水解反应方程式为:
![]()
![]()
![]()
![]()
某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的起始量如下表:
![]()
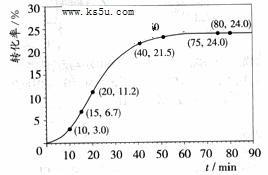
甲酸甲酯转化率在温度T1下随反应时间(t)的变化如下图:

(1)根据上述条件,计算不同时间范围内甲酸甲酯的平均反应速率,结果见下表:

请计算15~20min范围内甲酸甲酯的减少量为 mol,甲酸甲酯的平均反应速率
为 mol?min-1(不要求写出计算过程)。
(2)依据以上数据,写出该反应的反应速率在不同阶段的变化规律及其原因: 。
(3)上述反应的平衡常数表达式为:![]() ,则该反应在温度T1下的K值为 。
,则该反应在温度T1下的K值为 。
(4)其他条件不变,仅改变温度为T2(T2大于T1),在答题卡框图中画出温度T2下甲酸甲酯转化率随反应时间变化的预期结果示意图。
查看习题详情和答案>>甲酸甲酯水解反应方程式为:
![]()
![]()
![]()
![]()
![]()
![]() 某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的起始量如下表:
某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的起始量如下表:
![]()
![]()
![]() 甲酸甲酯转化率在温度T1下随反应时间(t)的变化如下图:
甲酸甲酯转化率在温度T1下随反应时间(t)的变化如下图:
![]()
![]()
![]() (1)根据上述条件,计算不同时间范围内甲酸甲酯的平均反应速率,结果见下表:
(1)根据上述条件,计算不同时间范围内甲酸甲酯的平均反应速率,结果见下表:
![]()

![]() 请计算15~20min范围内甲酸甲酯的减少量为 mol,甲酸甲酯的平均反应速率
请计算15~20min范围内甲酸甲酯的减少量为 mol,甲酸甲酯的平均反应速率
![]() 为 mol?min-1(不要求写出计算过程)。
为 mol?min-1(不要求写出计算过程)。
![]() (2)依据以上数据,写出该反应的反应速率在不同阶段的变化规律及其原因: 。
(2)依据以上数据,写出该反应的反应速率在不同阶段的变化规律及其原因: 。
![]() (3)上述反应的平衡常数表达式为:
(3)上述反应的平衡常数表达式为:![]() ,则该反应在温度T1下的K值为 。
,则该反应在温度T1下的K值为 。
![]() (4)其他条件不变,仅改变温度为T2(T2大于T1),在答题卡框图中画出温度T2下甲酸甲酯转化率随反应时间变化的预期结果示意图。
(4)其他条件不变,仅改变温度为T2(T2大于T1),在答题卡框图中画出温度T2下甲酸甲酯转化率随反应时间变化的预期结果示意图。
![]()
甲酸甲酯水解反应方程式为: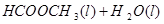
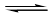
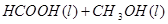
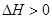
某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的起始量如下表: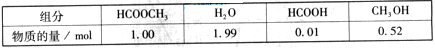
甲酸甲酯转化率在温度T1下随反应时间(t)的变化如下图: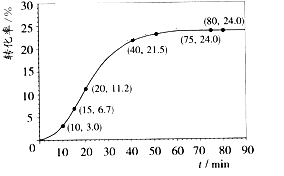
(1)根据上述条件,计算不同时间范围内甲酸甲酯的平均反应速率,结果见下表:
请计算15~20min范围内甲酸甲酯的减少量为 mol,甲酸甲酯的平均反应速率为 mol·min-1(不要求写出计算过程)。
(2)依据以上数据,推测该反应在10~40分钟间反应速率较快的原因: 。
甲酸甲酯水解反应方程式为:
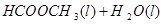
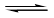
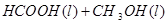
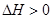
某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的起始量如下表:
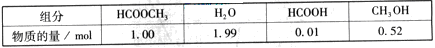
甲酸甲酯转化率在温度T1下随反应时间(t)的变化如下图:
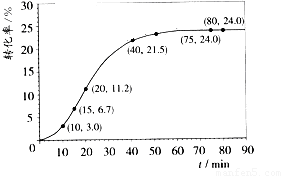
(1)根据上述条件,计算不同时间范围内甲酸甲酯的平均反应速率,结果见下表:

请计算15~20min范围内甲酸甲酯的减少量为 mol,甲酸甲酯的平均反应速率为 mol·min-1(不要求写出计算过程)。
(2)依据以上数据,推测该反应在10~40分钟间反应速率较快的原因: 。
查看习题详情和答案>>
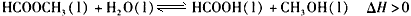
某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的起始量如下表
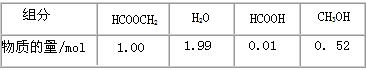

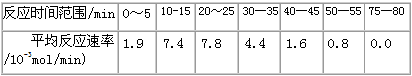
(2)依据以上数据,写出该反应的反应速率在不同阶段的变化规律及其原因:___________________________________
(3)上述反应的平衡常数表达式为:
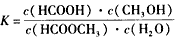 则该反应在温度T1下的K值为________________
则该反应在温度T1下的K值为________________ (4)其他条件不变,仅改变温度为T2(T2大于T1),画出温度T2下甲酸甲酯转化率随反应时间变化的预期结果示意图。______________________