题目内容
甲酸甲酯水解反应方程式为:
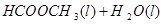
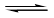
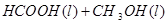
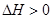
某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的起始量如下表:
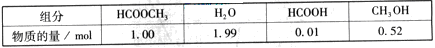
甲酸甲酯转化率在温度T1下随反应时间(t)的变化如下图:
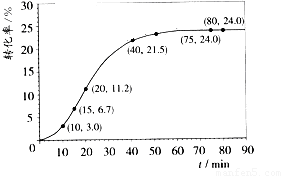
(1)根据上述条件,计算不同时间范围内甲酸甲酯的平均反应速率,结果见下表:

请计算15~20min范围内甲酸甲酯的减少量为 mol,甲酸甲酯的平均反应速率为 mol·min-1(不要求写出计算过程)。
(2)依据以上数据,推测该反应在10~40分钟间反应速率较快的原因: 。
(每空2分)(1)0.045 9.0×10-3
(2)该反应中甲酸具有催化作用;在反应中期,甲酸量逐渐增多,催化效果显著,反应速率明显增大。
【解析】
试题分析:(1)15min时,甲酸甲酯的转化率为6.7%,所以15min时,甲酸甲酯的物质的量为1mol-1.00mol×6.7%=0.933mol;20min时,甲酸甲酯的转化率为11.2%,所以20min时,甲酸甲酯的物质的量为1mol-1.00mol×11.2%=0.888mol,因此15至20min甲酸甲酯的减少量为0.933mol-0.888mol=0.045mol,则甲酸甲酯的平均速率=0.045mol/5min=0.009mol?min-1。
(2)从题给数据不难看出,该反应在10~40分钟间反应速率较快,这是由于该反应中甲酸具有催化作用;在反应中期,甲酸量逐渐增多,催化效果显著,反应速率明显增大。
考点:考查考生对化学反应速率概念,化学平衡的了解及其影响因素的理解
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,难易适中,在注重对学生基础知识巩固和训练的同时,侧重对学生知识迁移、读图及表达能力的培养,有利于培养学生的逻辑推理能力和创新思维能力,也有助于调动学生的学习兴趣,激发学生的求知欲。

 (2013?保定一模)甲酸甲酯水解反应方程武为:HCOOCH3(aq)+H2O(l)?HCOOCH(aq)+CH3OH(aq)△H>0.某温度下,VL溶液中各组分的起始量如表:HCOOCH3转化率随反 应时间(t)的变化如图(假设溶液体积不变)下列说法正确的是( )
(2013?保定一模)甲酸甲酯水解反应方程武为:HCOOCH3(aq)+H2O(l)?HCOOCH(aq)+CH3OH(aq)△H>0.某温度下,VL溶液中各组分的起始量如表:HCOOCH3转化率随反 应时间(t)的变化如图(假设溶液体积不变)下列说法正确的是( ) HCOOH(aq)+CH3OH(aq)
△H>0。某温度下,VL溶液中各组分的起始量如下表,HCOOCH3转化率随反应时间(t)的变化如下图(假设溶液体积不变),下列说法正确的是
HCOOH(aq)+CH3OH(aq)
△H>0。某温度下,VL溶液中各组分的起始量如下表,HCOOCH3转化率随反应时间(t)的变化如下图(假设溶液体积不变),下列说法正确的是