网址:http://m.1010jiajiao.com/timu_id_4449353[举报]
(1)CO2是一种重要的物质,但其过量排放,可能导致全球气温升高.下列措施不能够有效控制CO2所导致的温室效应的是
①大力发展低碳产业,提倡低碳生活,依法控制CO2的过量排放
②禁止滥砍滥伐,植树造林,恢复生态
③开发利用各种新型能源代替煤、石油、天然气等化石能源
④提倡使用脱硫煤、无铅汽油等清洁燃料
(2)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka=4.7×10-8.写出84消毒液露置在空气中发生反应的离子方程式
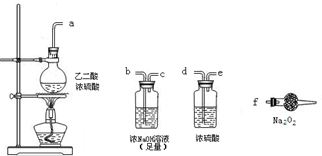
(3)CO具有还原性,某同学设计图示装置(固定装置及胶管略去)验证CO气体能否与Na2O2反应.
已知:H2C2O4
| ||
| △ |
(4)已知C(s)+O2(g)=CO2(g),△H=-393.5kJ?mol-1;CO(g)+
| 1 |
| 2 |
 运用化学反应原理研究氮、硫、氯等单质及其化合物的反应有重要的意义.
运用化学反应原理研究氮、硫、氯等单质及其化合物的反应有重要的意义.(1)放热反应2SO2(g)+O2(g)=2SO3(g)是硫酸工业上的重要反应,在体积不变的条件下,下列措施有利于提高SO2平衡转化率的有
A、升高温度 B、降低温度 C、减小压强 D、加入催化剂 E.移出氧气
(2)氮是大气中含量最多的一种元素,氮及其化合物在工农业生产、生活中有着重要应用.用CH4将氮氧化物(用NOx表示)催化还原为N2可以消除氮氧化物带来的污染,该反应的化学方程式为
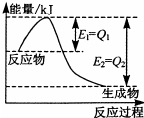
(3)如图是一定的温度和压强下,N2和H2反应生成1mol NH3过程中的能量变化图,请写出工业合成氨的热化学方程式
(4)在25℃下,将xmol/L的氨水与y mol/L的盐酸等体积混合,反应后溶液显中性,则c(NH4+ )
(5)已知:25℃时,Ksp(AgCl)=1.8×10-10、Ksp(AgBr)=4.9×10 -13.现在向0.001mol/L KBr和0.01mol/L KCl混合溶液中滴加0.1mol/L AgNO3溶液(反应过程中溶液体积变化忽略不计),当出现AgCl沉淀时.c(Br-)=
(12分)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
![]() (1)合成氨反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下,向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);使用催化剂后反应的△H(填“增大”“减小”或“不改变”) 。
(1)合成氨反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下,向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);使用催化剂后反应的△H(填“增大”“减小”或“不改变”) 。
(2)一定温度下,在恒容密闭容器中N2O5可发生化学反应:
![]() 2 N2O5(g) 4NO2(g)+O2(g) △H>0
2 N2O5(g) 4NO2(g)+O2(g) △H>0
①下表为反应T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| C(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
则500s内N2O5的分解速率为 。
②在T2温度下,反应1000s时测得NO2的浓度为4.98 mol·L-1,则T2 T1(填
“>”“<”“=”)
(3)已知肼分子(H2N—NH2)可以在氧气中燃烧生成氮气和水。
①利用肼、氧气与KOH溶液组成碱性燃料电池,请写出电池负极的电极反应式
②用电离方程式表示肼的水溶液呈碱性的原因
③肼是强还原剂,与氧化剂反应时放出大量的热,如:N2H4(1)+2H2O2(1)==N2(g)+4H2O(g) △H= —642.2kJ·mol-1
因此肼可以作为火箭推进剂。根据上述信息,你认为是否可以通过改变反应条件,由氮气和水蒸气来制取肼 。说明原因 。
查看习题详情和答案>>
运用化学反应原理研究碳的氧化物的性质具有重要意义。
(1)CO2是一种重要的物质,但其过量排放,可能导致全球气温升高。下列措施不能够有效控制CO2所导致的温室效应的是_________(填序号)
①大力发展低碳产业,提倡低碳生活,依法控制CO2的过量排放
②禁止滥砍滥伐,植树造林,恢复生态
③开发利用各种新型能源代替煤、石油、天然气等化石能源
④提倡使用脱硫煤、无铅汽油等清洁燃料
(2)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka =4.7×10-8。写出84消毒液露置在空气中发生反应的离子方程式___________________________。
(3)CO具有还原性,某同学设计图示装置(固定装置及胶管略去)验证CO气体能否与Na2O2反应。
已知: ,则实验选择的最简单的装置接口连接顺序为________;
,则实验选择的最简单的装置接口连接顺序为________;
若CO能够与Na2O2发生反应,则预测反应产物为____________。实验后用球形干燥管中的固体进行验证可选择的试剂是_______________________________。
(4)已知C(s)+O2(g)=CO2(g),△H="-393.5" kJ·mol -1 ;CO(g)+ O2(g)=CO2(g),△H="-283.0" kJ·mol -1,写出CO2和C(s)反应的热化学方程式___________________。以CO为燃料制作燃料电池,电池的正极通入O2和CO2,负极通入CO,电解质是熔融碳酸盐,放电时负极反应式为______________________。若使用该电池电解饱和食盐水制取1molNaClO,则理论上需要氧气的体积为(标准状况下)________L。
O2(g)=CO2(g),△H="-283.0" kJ·mol -1,写出CO2和C(s)反应的热化学方程式___________________。以CO为燃料制作燃料电池,电池的正极通入O2和CO2,负极通入CO,电解质是熔融碳酸盐,放电时负极反应式为______________________。若使用该电池电解饱和食盐水制取1molNaClO,则理论上需要氧气的体积为(标准状况下)________L。
(12分)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。 (1)合成氨反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下,向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);使用
(1)合成氨反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下,向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);使用 催化剂后反应的△H(填“增大”“减小”或“不改变”) 。
催化剂后反应的△H(填“增大”“减小”或“不改变”) 。
(2)一定温度下,在恒容密闭容器中N2O5可发生化学反应: 2 N2O5(g) 4NO2(g)+O2(g) △H>0
2 N2O5(g) 4NO2(g)+O2(g) △H>0
①下表为反应T1温度下的部分实验数据:
| t/s | 0 | 500[来源:学|科|网] | 1000 |
| C(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
 N2O5的分解速率为 。
N2O5的分解速率为 。②在T2温度下,反应1000s时测得NO2的浓度为4.98 mol·L-1,则T2 T1(填
“>”“<”“=”)
(3)已知肼分子(H2N—NH2)可以在
 氧气中燃烧生成氮气和水。
氧气中燃烧生成氮气和水。①利用肼、氧气与KOH溶液组成碱性燃料电池,请写出电池负极的电极反应式
②用电离方程式表示肼的水溶液呈碱性的原因
③肼是强还原剂,与氧化剂反应时放出大量的热,如:N2H4(1)+2H2O2(1)==N2(g)+4H2O(g) △H= —642.2kJ·mol-1
因此肼可以作为火箭推进剂。根据上述信息,你认为是否可以通过改变反应条件,由氮气和水蒸气来制取肼 。说明原因 。 查看习题详情和答案>>