网址:http://m.1010jiajiao.com/timu_id_4437178[举报]
制备海波的反应原理:Na2SO3+S
| ||

(1)实验开始时用lmL乙醇润湿硫粉的作用是.
A.有利于亚硫酸钠与硫磺的充分接触 B.防止亚硫酸钠溶解
C.控制溶液的pH D.提高产品的纯度
(2)趁热过滤的原因是
(3)滤液不采用直接蒸发发结晶的可能原因是
(4)抽滤过程中需要洗涤产品晶体,下列液体最适合的是
A.无水乙醇 B.饱和NaCl溶液 C,水 D.滤掖
(5)产品的纯度测定:取所得产品10.0g,配成500mL溶液,再从中取出25mL溶液于锥形瓶中,滴加几滴淀粉作指示剂,然后用0.050mol/L的标准碘水洛液滴定,重复三次,平高均消耗20mL 标准碘水,涉及的滴定反应方程式为:I2+2Na2S2O3═2NaI+Na2S4O6产品的中Na2S2O3?5H2O的纯度为
乙烯和苯是两种重要的化工原料,现有同学分别取这两种物质进行实验:
| 实验步骤 | 实验现象 | 解释及相关反应方程式 |
| 将乙烯通入溴水中 | | 发生了 反应(填反应类型),反应方程式: |
| 将苯与溴水混合振荡,静置 | | 溴在苯中的溶解度比在水中的溶解度 ;苯的密度比水 。 (填“大”或“小”) |
乙烯和苯是两种重要的化工原料,现有同学分别取这两种物质进行实验:
|
实验步骤 |
实验现象 |
解释及相关反应方程式 |
|
将乙烯通入溴水中 |
|
发生了 反应(填反应类型),反应方程式: |
|
将苯与溴水混合振荡,静置 |
|
溴在苯中的溶解度比在水中的溶解度 ;苯的密度比水 。 (填“大”或“小”) |
查看习题详情和答案>>
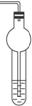
操作步骤:(1)如图装置Ⅰ所示,组装好实验装置。
(2)加入乙醇、乙酸及浓硫酸,点燃酒精灯缓慢加热。
(3)将产生的蒸气经导管导入装置A中,观察现象。
回答下列问题:
(1)请写出该反应的反应方程式:____________________。
(2)某同学在做实验时,为防止倒吸,对A装置进行的改进,请在右边虚框中画出改进部分装置图。
(3)若该同学用
①反应过程中升温过快过高,从而使一部分反应物未来得及充分反应
②该反应为可逆反应,反应不能进行彻底
③生成的乙酸乙酯未能充分冷凝下来
(4)为了提高反应物的利用率,另一同学认为采用了装置Ⅱ,你认为有何优点?__________________。
查看习题详情和答案>>硫化氢(H2S)是一种有毒的可燃性气体,用H2S、空气和KOH溶液可以组成燃料电池,其总反应式为2H2S+3O2+4KOH=2K2SO3+4H2O。
(1)该电池工作时正极应通入 。
(2)该电池的负极电极反应式为: 。
(3)该电池工作时负极区溶液的pH (填“升高”“不变”“降低”)
(4)有人提出K2SO3可被氧化为K2SO4,因此上述电极反应式中的K2SO3应为K2SO4,某学习小组欲将电池工作一段时间后的电解质溶液取出检验,以确定电池工作时反应的产物。实验室有下列试剂供选用,请帮助该小组完成实验方案设计。
0.01mol·L-1KMnO4酸性溶液,1mol·L-1HNO3,1mol·L-1H2SO4,1mol·L-1HCl,
0.1mol·L-1Ba(OH)2,0.1 mol·L-1 BaCl2。
|
|
实验步骤 |
实验现象及相关结论 |
|
① |
取少量电解质溶液于试管中,用pH试纸测其pH。 |
试纸呈深蓝色,经比对溶液的pH约为14,说明溶液中有残余的KOH。 |
|
② |
继续加入 溶液,再加入 溶液,振荡。 |
若有白色沉淀产生,则溶液中含有K2SO4。 若无白色沉淀产生,则溶液中没有K2SO4。 |
|
③ |
另取少量电解质溶液于试管中,先加 1 mol·L-1的H2SO4酸化,再滴入2~3滴0.01 mol·L-1KMnO4酸性溶液,振荡。 |
;
。 |
(5)若电池开始工作时每100mL电解质溶液含KOH56g,取电池工作一段时间后的电解质溶液20.00mL,加入BaCl2溶液至沉淀完全,过滤洗涤沉淀,将沉沉在空气中充分加热至恒重,测得固体质量为11.65g,计算电池工作一段时间后溶液中KOH的物质的量浓度 。 (结果保留四位有效数字,假设溶液体积保持不变,已知:M(KOH)=56,M(BaSO4)=233,M(BaSO3)=217)
查看习题详情和答案>>