摘要:一般窗玻璃里含Na2O为11.7%.CaO 12%,SiO2 75.3%.其余为杂质.现制取50kg窗玻璃.需用原料.NaCO3,CaCO3,SiO2各多少千克?
网址:http://m.1010jiajiao.com/timu_id_4418176[举报]
(2010?枣庄一模)(1)右图所示是实验室中制取气体的一种简易装置 .
.
①请简述检验它的气密性的方法
②利用右图所示装置可以制取
(2)张明同学设计下图所示装置,用粗铁粒与189g?L-1硝酸反应制取NO气体.请回答有关问题.

①189g?L-1硝酸的物质的量浓度为
②NO气体能用排水法收集,而不能用排空气法收集的可能原因是
③当打开止水夹a,关闭止水夹b时,A装置的干燥管中观察到的现象是
④该实验中,若去掉B装置,对实验结果是否有影响?
⑤将a mol铁与含b molHNO3的稀溶液充分反应后,若HNO3的还原产物只有NO,反应后Fe和HNO3均无剩余,则反应中转移电子的物质的量是
mol(2amol或3amol或2amol~3amol)
mol(2amol或3amol或2amol~3amol)(用含a或b的代数式表示).w⑥完全反应后,A装置烧杯里含铁的价态可能是
查看习题详情和答案>>
 .
.①请简述检验它的气密性的方法
关闭止水夹B,从A处加入水,使U形管两端形成液面差,一段时间后,液面差没有变化,说明气密性良好(没有关闭止水夹B不得分)
关闭止水夹B,从A处加入水,使U形管两端形成液面差,一段时间后,液面差没有变化,说明气密性良好(没有关闭止水夹B不得分)
.②利用右图所示装置可以制取
块状或较大颗粒状固体与液体不需要加热反应生成的
块状或较大颗粒状固体与液体不需要加热反应生成的
气体(填反应物状况及发生反应是否需要的条件).(2)张明同学设计下图所示装置,用粗铁粒与189g?L-1硝酸反应制取NO气体.请回答有关问题.

①189g?L-1硝酸的物质的量浓度为
3mol?L-1
3mol?L-1
.②NO气体能用排水法收集,而不能用排空气法收集的可能原因是
NO与空气中的O2反应,NO与空气密度接近
NO与空气中的O2反应,NO与空气密度接近
.③当打开止水夹a,关闭止水夹b时,A装置的干燥管中观察到的现象是
有红棕色气体出现
有红棕色气体出现
.B装置烧杯中液体的作用是吸收NO2
吸收NO2
.当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体.④该实验中,若去掉B装置,对实验结果是否有影响?
无影响
无影响
.⑤将a mol铁与含b molHNO3的稀溶液充分反应后,若HNO3的还原产物只有NO,反应后Fe和HNO3均无剩余,则反应中转移电子的物质的量是
| 3b |
| 4 |
| 3b |
| 4 |
+2价或+3价或+2价和+3价
+2价或+3价或+2价和+3价
.现有仪器和药品:试管和胶头滴管.0.1mol?L-1KSCN溶液、0.1mol?L-1KI溶液、0.2mol?L-1酸性KMnO4溶液、氯水等.请你设计一个简单实验,探究上述判断,填写下列实验报告:| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试管中滴入几滴KSCN溶液 | |
| 第二步 | 若溶液紫色退去,则说明含有Fe2+, 若无明显变化,则说明不含Fe2+ |
对溶液的研究和认识,在生产、生活和科研领域具有重要意义.
(1)现有一种含有弱酸HA和其钠盐NaA的溶液,请回答下列问题:
①组成该溶液的微观粒子有 .
②若向该溶液中加入少量盐酸时,发生反应的离子方程式是 ;
③若向该溶液中逐滴加入KOH溶液时,下列图象能表示Aˉ离子数目变化趋势的是 ;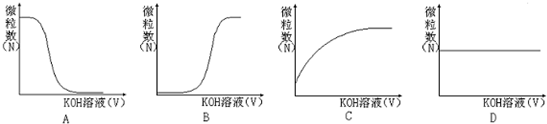
④现将1体积0.04mol?L-1HA溶液和1体积0.02mol?L-1NaOH溶液混合,得到2体积混合溶液.若该混合液显碱性,则其c(A-) 0.01mol?L-1(填“<”、“=”或“>”);若该混合液显酸性,溶液中所有离子的浓度由大到小的顺序是 .
(2)血液里含有的H2CO3和NaHCO3,与上述情况相似,对保持血液pH的稳定起到重要作用.
当c(H+)增大时,血液中消耗H+的离子方程式为 ;
当c(OH-)增大时,血液的pH也能保持基本稳定,试结合离子方程式简要说明 .
查看习题详情和答案>>
(1)现有一种含有弱酸HA和其钠盐NaA的溶液,请回答下列问题:
①组成该溶液的微观粒子有
②若向该溶液中加入少量盐酸时,发生反应的离子方程式是
③若向该溶液中逐滴加入KOH溶液时,下列图象能表示Aˉ离子数目变化趋势的是

④现将1体积0.04mol?L-1HA溶液和1体积0.02mol?L-1NaOH溶液混合,得到2体积混合溶液.若该混合液显碱性,则其c(A-)
(2)血液里含有的H2CO3和NaHCO3,与上述情况相似,对保持血液pH的稳定起到重要作用.
当c(H+)增大时,血液中消耗H+的离子方程式为
当c(OH-)增大时,血液的pH也能保持基本稳定,试结合离子方程式简要说明
 为11.7%,CaO为12%,
为11.7%,CaO为12%,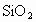 为75.3%,其余是杂质.现制取50kg窗玻璃,需用原料
为75.3%,其余是杂质.现制取50kg窗玻璃,需用原料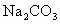 、
、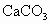 和
和 为11.7%,CaO为12%,
为11.7%,CaO为12%,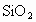 为75.3%,其余是杂质.现制取50kg窗玻璃,需用原料
为75.3%,其余是杂质.现制取50kg窗玻璃,需用原料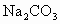 、
、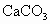 和
和