网址:http://m.1010jiajiao.com/timu_id_4416619[举报]
过氧化氢在催化剂作用下可快速产生氧气,它不仅是常用的消毒剂,还在航天和军事工业上有重要的用途。
(1)写出在过氧化氢溶液中加入MnO2粉末时,反应的化学方程式 。
(2)常用的消毒剂CH3COOOH(过氧乙酸),可以用冰醋酸和过氧化氢反应制取。制取时的化学反应方程式为 。该消毒剂中含有的少量过氧化氢,可以用它与高锰酸钾、次氯酸钠等强氧化剂的反应进行测定。请问,该消毒剂能否与漂粉精混合使用。
(3)过氧化氢和强还原剂液态肼(N2H4)可构成火箭推进剂。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4 rnol液态肼与足量的过氧化氢反应,生成氮气和水蒸气,放出236.64kJ的热量。
①写出该反应的热化学方程式 。
②又知H2O(l)=H2O(g);![]() 44 kJ?mol
44 kJ?mol![]() ,则16 g液态肼与过氧化氢反应生成液态水时放出的热量是 kJ。
,则16 g液态肼与过氧化氢反应生成液态水时放出的热量是 kJ。
③此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有―个很大的优点是
查看习题详情和答案>>(1)超音速飞机排放的尾气是平流层中NO的主要来源.它们破坏臭氧层的机理为:
①O3
| 光 |
②NO→NO2+O2
③NO2+O→NO+O2
上述反应的总反应式为
| ||
| ||

(2)汽车尾气中含有NOx、CO和碳氢化合物等.
①尾气净化装置里装有含Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用的机理如图1所示,尾气净化过程中发生的总反应化学方程式:
| ||
| ||
②NOx和碳氢化合物在阳光照射下发生光化学反应产生二次污染物的现象,称为“光化学烟雾”.有学者对某城市.天中光化学烟雾的变化情况进行测定,实验结果如图2.由图象可知,二次污染物有
③测定汽车尾气中Nox的方法之一是用3%的H2O2溶液吸收尾气中的NOx生成HNO3,再用NaOH标准溶液滴定HNO3.若要测定标准状况下尾气中NOx的体积分数,所需的数据有
A.所测尾气的总体积 B.两种氮氧化物的体积比
C.NaOH标准溶液的物质的量浓度 D.所消耗NaOH标准溶液的体积
E.从滴定开始到指示剂变色所需的时间
(3)硝酸工业尾气中的NOx可用纯碱溶液吸收,有关的化学反应为:
2NO2+Na2O=NaNO3+CO2
NO+NO2+Na2CO3=2NaNO3+CO2
现用0.5L 2mol/L的纯碱溶液恰好吸收一定量硝酸工业尾气中的NOx,吸收液质量增加44g(设C02全部排出).则NO2和NO的体积比为
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+ 2H2(g) CH3OH(g)
CH3OH(g)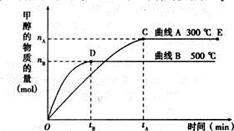
根据题意完成下列各题:
(1)5000C,从反应开始到平衡,甲醇的平均反应速率v(CH3OH)= (用nB、 tB 表示)
(2)在其他条件不变的情况下,将处于E点的体系的体积压缩到原来的1/2,下列有关该体系的说法正确的是
a .氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大
(3)可逆反应:CO(g)+ 2H2(g) CH3OH(g) 在恒容密闭容器中反应,达到平衡状态的标志是:
CH3OH(g) 在恒容密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成2n molH2的同时生成n mol CH3OH
②单位时间内生成2n molH2的同时,生成n mol CO
③用CO、H2、CH3OH 的物质的量浓度变化表示的反应速率的比为1 : 2 : 1的状态
④混 合气体的密度不再改变的状态
⑤ 混合气体的平均相对分子质量不再改变的状态
(4)改变下列哪些条件能增大甲醇的产量( )
| A.增大容器体积 | B.增大压强 | C.升高温度 | D.加催化剂 |
(6)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: (用化学方程式表示)。 查看习题详情和答案>>
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+ 2H2(g) CH3OH(g)
CH3OH(g)
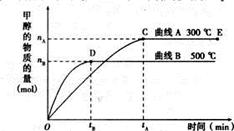
根据题意完成下列各题:
(1)5000C,从反应开始到平衡,甲醇的平均反应速率v(CH3OH)= (用nB、 tB 表示)
(2)在其他条件不变的情况下,将处于E点的体系的体积压缩到原来的1/2,下列有关该体系的说法正确的是
a .氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大
(3)可逆反应:CO(g)+ 2H2(g) CH3OH(g) 在恒容密闭容器中反应,达到平衡状态的标志是:
CH3OH(g) 在恒容密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成2n molH2的同时生成n mol CH3OH
②单位时间内生成2n molH2的同时,生成n mol CO
③用CO、H2、CH3OH 的物质的量浓度变化表示的反应速率的比为1 : 2 : 1的状态
④混 合气体的密度不再改变的状态
⑤ 混合气体的平均相对分子质量不再改变的状态
(4)改变下列哪些条件能增大甲醇的产量( )
A.增大容器体积 B.增大压强 C.升高温度 D.加催化剂
(5)反应达到平衡后再升高温度,K值 (填“增大”“减小”或“不变”)。
(6)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: (用化学方程式表示)。
查看习题详情和答案>>
A、提出假设.反应产物可能有:
猜想①一氧化碳;猜想②甲醇;猜想③甲醛; 猜想④甲酸;猜想⑤水;猜想⑥炭;猜想⑦二氧化碳.
B、查阅资料.①RCHO遇强碱生成RCH2OH和RC00H;②甲酸分子中含有醛基.
C、实验探究.
(一)主要药品:略
(二)实验装置:见下图(铁架台、酒精灯未画出),请在D方框内画出装有碱石灰的球形干燥管(含连接仪器)

实验操作:
| 序号 | 实验内容要点 | 实验现象, | 结论及解释 | ||||
| (1) | 加热后,缓慢通气体 | E中澄清石灰水不变浑浊,G中澄清石灰水变浑浊 | 猜想 ① ① 成立 | ||||
| (2) | 将D装置取走,连接好其余装置, 继续反应 |
观察到E中澄清石灰水始终不 变浑浊 |
猜想 ⑦ ⑦ 不成立 | ||||
| (3) | 用pH试纸测C中混和物pH | pH试纸变为 浅红或是红 浅红或是红 色,pH=3 |
猜想④成立. | ||||
| (4) | 取C中适量混和液,滴加稍过量 碳酸氢钠溶液蒸馏,取馏出物 碳酸氢钠溶液蒸馏,取馏出物 ,再与银氨溶液反应 |
出现银镜 | 猜想③成立,银镜反应离子方程式为 HCHO+2[Ag(NH3)2]++2OH-
HCHO+2[Ag(NH3)2]++2OH-
| ||||
| … | … | … |
I、研究小组甲、乙、丙、丁、戊五人有以下叙述,其中叙述正确的是
甲、A装置太复杂,用H装置代替
乙、A装置虽复杂,但也不能用H装置代替
丙、B装置中的细长铁管内,将催化剂分散在SiO2中的主要目的是:增大气体和催化剂的接触面积,加快反应速度
丁、猜想⑤是不需要经过实验证明就成立的.
戊、在B和C置之间增加I装置,昉止倒吸
II、B中自动恒温电加热器可任设某一温度,若再补充部份仪器,可研究