摘要: 该反应的化学方程式是 :CaC03+2HCl==CaC12+H2C03碳酸不稳定很易分解 :H2C03 ㄔㄔ H20+C02 ↑ 两式相加便是总的反应式 :CaC03+2HCl ㄔㄔ CaC12+H20+ CO2 ↑[ 讨论交流 ] 讨论课文第 134 页之 “讨论与交流 , 由学生表达 , 教师做适当评价归纳.[ 练习 ] 在制取 C02 及O2的实验中 , 相关性质的比较 , 请填写下表空格 : 反应物及其状态反应条件(是否加热或加人催化剂)其密度比空气的密度大或小是否与功发生反屈O2 C02 [ 讨论交流 ] 实验室制取气体的思路和方法 :( 师生交流.教师评价.归纳 )
网址:http://m.1010jiajiao.com/timu_id_435822[举报]
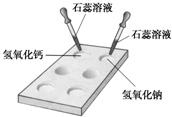 18、碱的化学性质活动与探究:?
18、碱的化学性质活动与探究:?(1)如图所示,在白色点滴板上进行实验,往氢氧化钠溶液和氢氧化钙溶液中滴加两滴紫色石蕊溶液,石蕊溶液都变
蓝
色.由实验现象分析可知,不同的碱溶液中都含有相同的OH-(或氢氧根离子)
.(2)氢氧化钠必须密封保存,因为氢氧化钠在空气中不仅吸收水分,还吸收空气中的
CO2(或二氧化碳)
,该反应的化学方程式是CO2+2 NaOH═Na2CO3+H2O
.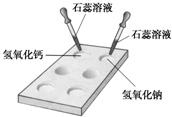 13、碱的化学性质活动与探究:?
13、碱的化学性质活动与探究:?(1)如图所示,在白色点滴板上进行实验,往氢氧化钠溶液和氢氧化钙溶液中滴加两滴紫色石蕊溶液,石蕊溶液都变
蓝
色.由实验现象分析可知,不同的碱溶液中都含有相同的OH-(或氢氧根离子)
;(2)氢氧化钠必须密封保存,因为氢氧化钠在空气中不仅吸收水分,还吸收空气中的
CO2(或二氧化碳)
,该反应的化学方程式是CO2+2 NaOH═Na2CO3+H2O
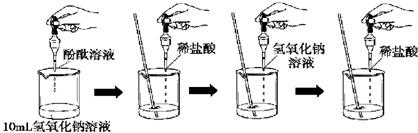
;(3)如下图所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显
红
色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色变无色
,此时中和反应恰好完成.接着用滴管返滴入1-2滴氢氧化钠溶液,溶液显红色
色,再次用滴管慢慢滴入足量的稀盐酸,溶液的颜色变无色
;
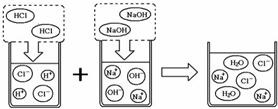
(4)氢氧化钠溶液和稀盐酸反应的实质可以用如下微观示意图表示.由该图的粒子变化可得出酸碱中和反应的实质是
OH-+H+=H2O
.
 双氧水常用于消毒、漂白等,它与MnO2混合在常温下即可迅速分解放出氧气,实验室可双氧水制取氧气(利用分液漏斗玻璃活塞的“开”、“关”,可随时向锥形瓶中滴加双氧水).试回答下列问题:
双氧水常用于消毒、漂白等,它与MnO2混合在常温下即可迅速分解放出氧气,实验室可双氧水制取氧气(利用分液漏斗玻璃活塞的“开”、“关”,可随时向锥形瓶中滴加双氧水).试回答下列问题:(1)该反应的化学方程式是
(2)在实验室中该装置还可用于制取哪些气体?请举出两例
(3)欲分离反应后混合物中的MnO2,用到的玻璃仪器有
(4)如果在实验室中用此方法代替KClO3与MnO2共热制取氧气,请简述其优点有哪些? 查看习题详情和答案>>
十八世纪法国化学家拉瓦锡为了研究空气的组成设计 了一个划时代意义的钟罩实验(如右图),该实验证明了空气中氧气约占空气的体积1/5。
①拉瓦锡在观察到汞面浮起红色渣滓后,还继续加热12天,至红色渣滓不再增加,这样做的理由是 (1) ,该反应的化学方程式是(2) 。
②拉瓦锡得到的红色渣滓是氧化汞,他又将氧化汞加热分解得到氧气,而现在实验室检验氧气的方法可以是(3) 。
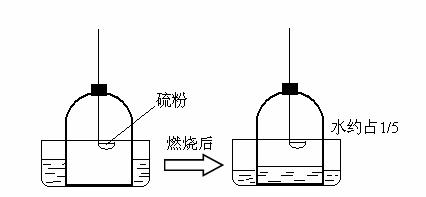 ③实验室常用白磷燃烧来验证空气中氧气约占1/5,小张同学利用实验室现有的药品硫粉和镁粉,利用下列钟罩装置进行实验,燃烧完毕冷却后的结果如图:
③实验室常用白磷燃烧来验证空气中氧气约占1/5,小张同学利用实验室现有的药品硫粉和镁粉,利用下列钟罩装置进行实验,燃烧完毕冷却后的结果如图:
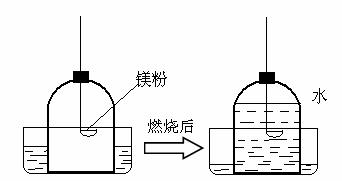
写出硫粉在钟罩内燃烧的化学方程式(4) ,燃烧的现象是(5) 。
如果实验仪器气密性良好,所用的硫粉、镁粉都是足量的。根据实验结果,推测可能的原因,硫粉燃烧后水进入约1/5的原因是(6) ;镁粉燃烧后水几乎占满整个钟罩的原因是(7) 。
④现在实验室中得到氧气,可以利用氯酸钾受热分解,实验操作时要用到酒精灯、导管、铁架台等,还需用到的玻璃仪器有(8) ;目前实验室不用氧化汞加热分解的方法制取氧气的理由是(9) 。
⑤若实验室利用12.25g氯酸钾与3gMnO2混合加热,请写出化学反应方程式,并列式计算最多可以得到多少物质的量的氧气?
查看习题详情和答案>>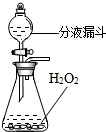 双氧水常用于消毒、漂白等,它与MnO2混合在常温下即可迅速分解放出氧气,实验室可双氧水制取氧气(利用分液漏斗玻璃活塞的“开”、“关”,可随时向锥形瓶中滴加双氧水).试回答下列问题:
双氧水常用于消毒、漂白等,它与MnO2混合在常温下即可迅速分解放出氧气,实验室可双氧水制取氧气(利用分液漏斗玻璃活塞的“开”、“关”,可随时向锥形瓶中滴加双氧水).试回答下列问题: