题目内容
 18、碱的化学性质活动与探究:?
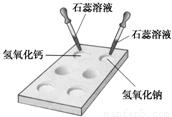
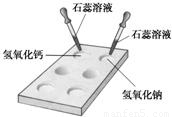
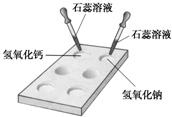
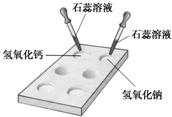
18、碱的化学性质活动与探究:?(1)如图所示,在白色点滴板上进行实验,往氢氧化钠溶液和氢氧化钙溶液中滴加两滴紫色石蕊溶液,石蕊溶液都变
蓝
色.由实验现象分析可知,不同的碱溶液中都含有相同的OH-(或氢氧根离子)
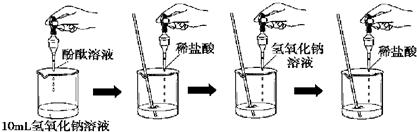
.(2)氢氧化钠必须密封保存,因为氢氧化钠在空气中不仅吸收水分,还吸收空气中的
CO2(或二氧化碳)
,该反应的化学方程式是CO2+2 NaOH═Na2CO3+H2O
.分析:(1)紫色石蕊遇碱变蓝色,实际上是碱中的氢氧根离子使石蕊变色,而碱中具有的相同的离子是氢氧根离子,
(2)二氧化碳会和氢氧化钠溶液反应生成碳酸钠而使氢氧化钠变质,根据反应物和生成物书写化学方程式,
(2)二氧化碳会和氢氧化钠溶液反应生成碳酸钠而使氢氧化钠变质,根据反应物和生成物书写化学方程式,
解答:解:(1)碱会使紫色石蕊变蓝色,但是不同的碱中具有相同的氢氧根离子.
故答案为:蓝,氢氧根离子,
(2)二氧化碳会和氢氧化钠溶液反应生成碳酸钠而使氢氧化钠变质,氢氧化钠吸水潮解后,会与氢氧化钠反应生成碳酸钠和水.
故答案为:二氧化碳,2NaOH+CO2=Na2CO3+H2O,
故答案为:蓝,氢氧根离子,
(2)二氧化碳会和氢氧化钠溶液反应生成碳酸钠而使氢氧化钠变质,氢氧化钠吸水潮解后,会与氢氧化钠反应生成碳酸钠和水.
故答案为:二氧化碳,2NaOH+CO2=Na2CO3+H2O,
点评:本题主要考查了酸碱指示剂遇酸碱后的不同显色知识,以及氢氧化钠变质的问题,是常规知识的训练,题目难度不大.

练习册系列答案
相关题目
 13、碱的化学性质活动与探究:?
13、碱的化学性质活动与探究:?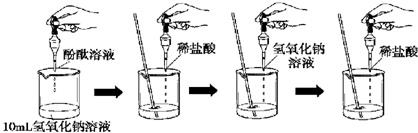
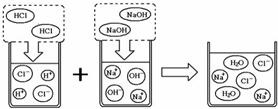
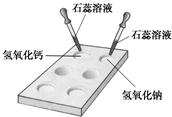 23、碱的化学性质活动与探究:
23、碱的化学性质活动与探究: