摘要:将干燥的石蕊试纸放入装有二氧化碳的试管中
网址:http://m.1010jiajiao.com/timu_id_435544[举报]
13、化学实验室学习化学的基础,请根据下列装置图回答问题.
(1)A图中制取CO2的化学方程式为
(2)将接口a和b连接,可观察到,仅有下面玻璃管内湿润的石蕊试纸变红,上面玻璃管内无明显现象产生.据此说明;①二氧化碳气体密度比空气密度
(3)已知:①CaCO3+CO2+H2O=Ca(HCO3)2;②Ca(HCO3)2 易溶于水,能与澄清石灰水或碳酸钠溶液反应都生成碳酸钙沉淀,也能与盐酸反应放出二氧化碳气体.将接口a和c连接,通入一定量的二氧化碳气体后,将试管静置,是固液分离,则上层溶液中可能含有的溶质是
查看习题详情和答案>>

(1)A图中制取CO2的化学方程式为
CaCO3+2HCl═CaCl2+2H2O+CO2↑
,浓硫酸的作用是干燥二氧化碳气体
.(2)将接口a和b连接,可观察到,仅有下面玻璃管内湿润的石蕊试纸变红,上面玻璃管内无明显现象产生.据此说明;①二氧化碳气体密度比空气密度
大
;②二氧化碳与水反应生成显酸
性物质.(3)已知:①CaCO3+CO2+H2O=Ca(HCO3)2;②Ca(HCO3)2 易溶于水,能与澄清石灰水或碳酸钠溶液反应都生成碳酸钙沉淀,也能与盐酸反应放出二氧化碳气体.将接口a和c连接,通入一定量的二氧化碳气体后,将试管静置,是固液分离,则上层溶液中可能含有的溶质是
Ca(OH)2
或Ca(HCO3)2
.请你设计实验方案加以验证.| 实验操作 | 实验现象 | 结论 |
| 取少量上层溶液于试管中,,然后滴加 盐酸 |
放出气体 |
溶质为 Ca(HCO3)2 |
请回忆老师做的“二氧化碳与水反应”的实验并分析下列四组对比实验回答问题:
(Ⅰ)组:向装有2mL稀醋酸的试管中滴加两滴紫色石蕊溶液;
(Ⅱ)组:向装有2mL蒸馏水的试管中滴加两滴紫色石蕊溶液;
(Ⅲ)组:向装满二氧化碳的干燥集气瓶中放入干燥的紫色石蕊试纸;
(Ⅳ)组:将二氧化钛通入盛有紫色石蕊溶液的试管.
(1)能使紫色石蕊溶液变红的是实验(Ⅰ)和实验(Ⅱ),它们验证的是酸能______的性质;
(2)实验(Ⅰ)和实验(Ⅱ)起到了对比作用,可以观察到的现象是______;实验(Ⅲ)说明______;
(3)将第(Ⅳ)组实验后的试管用酒精灯加入,观察到的现象是______.
查看习题详情和答案>>
(Ⅰ)组:向装有2mL稀醋酸的试管中滴加两滴紫色石蕊溶液;
(Ⅱ)组:向装有2mL蒸馏水的试管中滴加两滴紫色石蕊溶液;
(Ⅲ)组:向装满二氧化碳的干燥集气瓶中放入干燥的紫色石蕊试纸;
(Ⅳ)组:将二氧化钛通入盛有紫色石蕊溶液的试管.
(1)能使紫色石蕊溶液变红的是实验(Ⅰ)和实验(Ⅱ),它们验证的是酸能______的性质;
(2)实验(Ⅰ)和实验(Ⅱ)起到了对比作用,可以观察到的现象是______;实验(Ⅲ)说明______;
(3)将第(Ⅳ)组实验后的试管用酒精灯加入,观察到的现象是______.
(2009?昆明)请回忆老师做的“二氧化碳与水反应”的实验并分析下列四组对比实验回答问题:
(Ⅰ)组:向装有2mL稀醋酸的试管中滴加两滴紫色石蕊溶液;
(Ⅱ)组:向装有2mL蒸馏水的试管中滴加两滴紫色石蕊溶液;
(Ⅲ)组:向装满二氧化碳的干燥集气瓶中放入干燥的紫色石蕊试纸;
(Ⅳ)组:将二氧化钛通入盛有紫色石蕊溶液的试管.
(1)能使紫色石蕊溶液变红的是实验(Ⅰ)和实验(Ⅱ),它们验证的是酸能
(2)实验(Ⅰ)和实验(Ⅱ)起到了对比作用,可以观察到的现象是
(3)将第(Ⅳ)组实验后的试管用酒精灯加入,观察到的现象是
查看习题详情和答案>>
(Ⅰ)组:向装有2mL稀醋酸的试管中滴加两滴紫色石蕊溶液;
(Ⅱ)组:向装有2mL蒸馏水的试管中滴加两滴紫色石蕊溶液;
(Ⅲ)组:向装满二氧化碳的干燥集气瓶中放入干燥的紫色石蕊试纸;
(Ⅳ)组:将二氧化钛通入盛有紫色石蕊溶液的试管.
(1)能使紫色石蕊溶液变红的是实验(Ⅰ)和实验(Ⅱ),它们验证的是酸能
使紫色石蕊试液变红
使紫色石蕊试液变红
的性质; (2)实验(Ⅰ)和实验(Ⅱ)起到了对比作用,可以观察到的现象是
醋酸使紫色石蕊试液变红而水不能
醋酸使紫色石蕊试液变红而水不能
;实验(Ⅲ)说明二氧化碳不能使干燥的紫色石蕊试纸变红
二氧化碳不能使干燥的紫色石蕊试纸变红
;(3)将第(Ⅳ)组实验后的试管用酒精灯加入,观察到的现象是
变红的紫色石蕊溶液又变成紫色.
变红的紫色石蕊溶液又变成紫色.
.下表是某城市某日空气质量报告:

某研究性学习小组对表中首要污染物SO2导致酸雨的成因进行探究。(提示:SO2是一种无色、有刺激性气味的有毒气体,易溶于水,具有与CO2相似的化学性质)
【探究实验】实验一:用下图所示装置进行实验。
【探究实验】实验一:用下图所示装置进行实验。
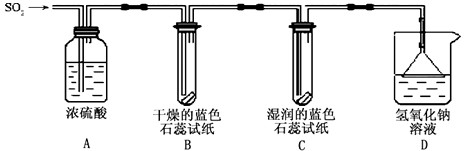
(1)A装置的作用是__________SO2气体。
(2)实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变红色,说明SO2与水反应生成一种_________________。
(3)D装置的作用是__________,发生反应的化学方程式是______________。
实验二:往盛有水的烧杯中通入SO2气体,测所得溶液的pH______7(填“>”“=”或“<”),然后每隔1小时测定其pH,发现pH逐渐变小,直至恒定,说明烧杯中溶液被空气中的氧气氧化最终生成H2SO4。 【查阅资料】SO2形成酸雨的另一途径:SO2与空气中的O2在飘尘的作用下反应生成SO3(飘尘的质量和性质在反应前后不发生变化),SO3溶于降水生成H2SO4。在此过程中飘尘作______________。
【探究结论】SO2与空气中的氧气、水反应生成硫酸而形成酸雨。该市可能易出现酸雨。
【模拟实验】(1)由于食醋和酸雨的酸度(pH)差不多,因此酸雨对大理石的作用可以通过大理石碎片放在醋中来模拟。当把2.0g大理石碎片放在醋中一整夜后,取出固体干燥称重,其质量可能是(醋酸钙易溶于水)__________。A.小于2.0g B.正好2.0g C.大于2.0g
(2)这组学生还做了另一个实验,即将大理石碎片放在蒸馏水中过夜,其实验的目的是_____________。
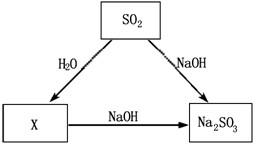
【知识联想】SO2具有与CO2相似的化学性质,根据下图给出的SO2及其化合物问的相互转化关系回答:X的化学式是_____,写出X与Na2SO3反应的化学方程___________________,反应类型是__________。
(2)实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变红色,说明SO2与水反应生成一种_________________。
(3)D装置的作用是__________,发生反应的化学方程式是______________。
实验二:往盛有水的烧杯中通入SO2气体,测所得溶液的pH______7(填“>”“=”或“<”),然后每隔1小时测定其pH,发现pH逐渐变小,直至恒定,说明烧杯中溶液被空气中的氧气氧化最终生成H2SO4。 【查阅资料】SO2形成酸雨的另一途径:SO2与空气中的O2在飘尘的作用下反应生成SO3(飘尘的质量和性质在反应前后不发生变化),SO3溶于降水生成H2SO4。在此过程中飘尘作______________。
【探究结论】SO2与空气中的氧气、水反应生成硫酸而形成酸雨。该市可能易出现酸雨。
【模拟实验】(1)由于食醋和酸雨的酸度(pH)差不多,因此酸雨对大理石的作用可以通过大理石碎片放在醋中来模拟。当把2.0g大理石碎片放在醋中一整夜后,取出固体干燥称重,其质量可能是(醋酸钙易溶于水)__________。A.小于2.0g B.正好2.0g C.大于2.0g
(2)这组学生还做了另一个实验,即将大理石碎片放在蒸馏水中过夜,其实验的目的是_____________。
【知识联想】SO2具有与CO2相似的化学性质,根据下图给出的SO2及其化合物问的相互转化关系回答:X的化学式是_____,写出X与Na2SO3反应的化学方程___________________,反应类型是__________。
叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某兴趣小组对其进行下列研究.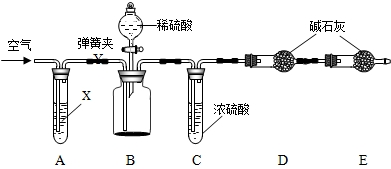
【查阅资料】
(1)汽车经撞击后,30毫秒内引发NaN3,迅速分解为Na、N2.
(2)将生成的金属钠与液态氨反应得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和气体X,该反应的化学方程式为2NaNH2+N2O=NaN3+NaOH+X.则为
【Na2CO3质量分数测定】
为进一步测定NaN3样品中Na2CO3的质量分数设计如下图装置(已知H2SO4溶液与NaN3,反应不生成气体).
实验步骤如下:
①按图连接装置,
②准确称得盛有碱石灰(固体氢氧化钠和氧化钙的混合物)的干燥管D的质量为a g;
③准确称得叠氮化钠(NaN3)样品的质量W g放入装置B的广口瓶中;
④打开装置B的分液漏斗旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后再称得干燥管D的总质量为b g.根据实验中测得的有关数据,可以算出样品中碳酸钠的质量分数.
试回答:(1)第⑤步缓缓鼓入空气的目的是
(2)若没有C装置,则会导致测定结果
(3)E装置的作用是
查看习题详情和答案>>

【查阅资料】
(1)汽车经撞击后,30毫秒内引发NaN3,迅速分解为Na、N2.
(2)将生成的金属钠与液态氨反应得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和气体X,该反应的化学方程式为2NaNH2+N2O=NaN3+NaOH+X.则为
NH3
NH3
,实验室检验该气体使用的试纸是湿润红色石蕊试纸
红色石蕊试纸
.根据制备反应,工业级NaN3中会含有Na2CO3.试分析工业级NaN3中含有Na2CO3的可能原因生成NaN2的同时有NaOH生成,NaOH吸收空气中的CO2生成Na2CO3
生成NaN2的同时有NaOH生成,NaOH吸收空气中的CO2生成Na2CO3
.【Na2CO3质量分数测定】
为进一步测定NaN3样品中Na2CO3的质量分数设计如下图装置(已知H2SO4溶液与NaN3,反应不生成气体).
实验步骤如下:
①按图连接装置,
检查装置的气密性
检查装置的气密性
;②准确称得盛有碱石灰(固体氢氧化钠和氧化钙的混合物)的干燥管D的质量为a g;
③准确称得叠氮化钠(NaN3)样品的质量W g放入装置B的广口瓶中;
④打开装置B的分液漏斗旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后再称得干燥管D的总质量为b g.根据实验中测得的有关数据,可以算出样品中碳酸钠的质量分数.
试回答:(1)第⑤步缓缓鼓入空气的目的是
将B中生成的二氧化碳赶往D中
将B中生成的二氧化碳赶往D中
,装置A中试剂X最适宜选用氢氧化钠溶液
氢氧化钠溶液
.写出B中生成气体的反应方程式Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
.(2)若没有C装置,则会导致测定结果
偏大
偏大
(填:“偏大”或“偏小”).(3)E装置的作用是
吸收空气中的水和二氧化碳
吸收空气中的水和二氧化碳
.