网址:http://m.1010jiajiao.com/timu_id_428288[举报]
生物体中有许多含过渡金属离子的蛋白,其中有些金属蛋白在一定条件下能够吸收、释放氧气以供机体生命活动之需。这些天然载氧体的结构较复杂。研究发现,某些简单配合物也具有类似的载氧性质,可用作载氧体的模型化合物。研究较多的是钴(II)配合物。制备模型化合物的方法如下:水杨酸(邻羟基苯甲醛)和乙二胺在95%的乙醇溶液中反应,生成黄色晶体人通入氮气,加热,待黄色晶体溶解后,缓慢地加入醋酸钴,生成棕色沉淀。继续加热并搅拌,沉淀全部转变为暗红色B后,冷至室温,撤去氮气,滤出结晶,干燥之B是二聚体,在室温下稳定,不吸收氧气。但B在某些溶剂中可与溶剂L(如DMF或Py等)配位,并迅速吸收氧气形成暗黑色的分子氧加合物C。C在氯仿或苯中有细微气泡放出,并转变为暗红色。载氧试验结果: 360 mg样品B 在 15℃, 102.9kPa及饱和水蒸气压 1.2 kPa下,吸收 O2(设为理想气体) 12.90cm3。
3-1.写出A的化学式。
3-2.计算载氧试验中,Co 与被吸收氧气的物质的量之比。
3-3.画出C的结构示意图。
3-4.写出C在氯仿中的反应方程式。
查看习题详情和答案>>(12分)
为了比较温室效应气体对目前全球增温现象的影响,科学家通常引用“温室效应指数”,以二氧化碳为相对标准。表1有(A)至(I)共九种气体在大气中的体积百分比及其温室效应指数。
结合表中列出的九种气体,试参与回答下列各题:
(1)下列由极性键形成的非极性分子是 。
A.N2 B.O2 C.H2O D.CO2 E.CH4
(2)下列说法正确的是 。
A.N2O与CO2, CCl3F与CCl2F2互为等电子体
B.CCl2F2无同分异构体,说明其中碳原子采用sp2方式杂化
C.CCl2F2是目前引起温室效应的主要原因
D.H2O沸点是九种物质中最高的,是因为水分子间能形成氢键
(3)在半导体生产或灭火剂的使用中,会向空气逸散气体如:NF3、CHClFCF3、C3F8,它们虽是微量的,有些确是强温室气体,下列推测正确的是 。
A.由价层电子对互斥理论可确定NF3分子呈平面三角形
B.C3F8在CCl4中的溶解度比水中大
C.CHClFCF3存在手性异构
D.电负性:N<O<F
(4)甲烷晶体的晶胞结构如图,下列有关说法正确的 。
A.甲烷在常温下呈气态,说明甲烷晶体属于分子晶体
B.晶体中1个CH4分子有6个紧邻的甲烷分子
C.CH4晶体熔化时需克服共价键
D.可燃冰(8CH4·46H2O)是在低温高压下形成的晶体
(5)水能与多种过渡金属离子形成络合物,已知某紫红色络合物的组成为CoCl3·5NH3·H2O。其水溶液显弱酸性,加入强碱并加热至沸腾有氨放出,同时产生Co2O3沉淀;加AgNO3于该化合物溶液中,有AgCl沉淀生成,过滤后再加AgNO3溶液于滤液中无变化,但加热至沸腾有AgCl沉淀生成,且其质量为第一次沉淀量的二分之一。则该配合物的化学式最可能为 。
A.[CoCl2(NH3)4 ]Cl·NH3·H2O B.[ CoCl(NH3)5]Cl2·H2O
C.[CoCl2(NH3)3(H2O)]Cl·2NH3 D.[ Co(NH3)5(H2O)]Cl3
(6)题(5)中钴离子在基态时核外电子排布式为: 。
查看习题详情和答案>>
为了比较温室效应气体对目前全球增温现象的影响,科学家通常引用“温室效应指数”,以二氧化碳为相对标准。表1有(A)至(I)共九种气体在大气中的体积百分比及其温室效应指数。
结合表中列出的九种气体,试参与回答下列各题:

(1)下列由极性键形成的非极性分子是 。
A.N2 B.O2 C.H2O D.CO2 E.CH4
(2)下列说法正确的是 。
A.N2O与CO2, CCl3F与CCl2F2互为等电子体
B.CCl2F2无同分异构体,说明其中碳原子采用sp2方式杂化
C.CCl2F2是目前引起温室效应的主要原因
D.H2O沸点是九种物质中最高的,是因为水分子间能形成氢键
(3)在半导体生产或灭火剂的使用中,会向空气逸散气体如:NF3、CHClFCF3、C3F8,它们虽是微量的,有些确是强温室气体,下列推测正确的是 。
A.由价层电子对互斥理论可确定NF3分子呈平面三角形
B.C3F8在CCl4中的溶解度比水中大
C.CHClFCF3存在手
 性异构
性异构D.电负性:N<O<F
(4)甲烷晶体的晶胞结构如图,下列有关说法正确的 。

A.甲烷在常温下呈气态,说明甲烷晶体属于分子晶体
B.晶体中1个CH4分子有6个紧邻的甲烷分子
C.CH4晶体熔化时需克服共价键
D.可燃冰(8CH4·46H2O)是在低温高压下形成的晶体
(5)水能与多种过渡金属离子形成络合物,已知某紫红色络合物的组成为CoCl3·5NH3·H2O。其水溶液显弱酸性,加入强碱并加热至沸腾有氨放出,同时产生Co2O3沉淀;加AgNO3于该化合物溶液中,有AgCl沉淀生成,过滤后再加AgNO3溶液于滤液中无变化,但加热至沸腾有AgCl沉淀生成,且其质量为第一次沉淀量的二分之一。则该配合物的化学式最可能为 。
A.[ CoCl2(NH3)4 ]Cl·NH3·H2O B.[ CoCl(NH3)5]Cl2·H2O
C.[ CoCl2(NH3)3(H2O)]Cl·2NH3 D.[ Co(NH3)5(H2O)]Cl3
(6)题(5)中钴离子在基态时核外电子排布式为: 。
(1)若A是常见金属,且A的合金用量最大,A与B的浓溶液在常温时发生钝化,但A与B的稀溶液反应产生无色气体并能迅速转化为红棕色.请写出过量的A与B的稀溶液反应的化学方程
(2)若A、D均可用于消毒,且C是家家户户的厨房必备的物质之一,写出该反应的离子方程式
(3)若A为黑色固体,C是黄绿色的单质气体,反应的化学方程式为
若向100mL 12.0mol?L-1的B中加入足量的A固体并加热,充分反应后在标准状况下生成C的体积是
A.等于6.72L B.小于6.72L
C.等于13.44L D.大于6.72L小于13.44L
(4)已知炭和浓硫酸在加热时也符合上述反应式,某同学设计如下实验证明其产物:
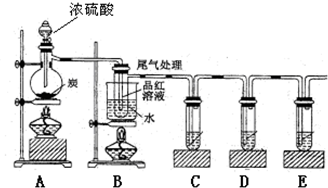
若证明有水生成,需要在A、B之间加装盛有