利峽⦿http://m.1010jiajiao.com/timu_id_427935[訟烏]
蛍裂泌和火髪議郡哘⦿ ⇦______⇦6H⇦﹆3R2●⇦3H2O。和双偃峰屎鳩議頁( )
⇦______⇦6H⇦﹆3R2●⇦3H2O。和双偃峰屎鳩議頁( )
A⤴貧塀嶄髪𡸴侭野麗嵎壓郡哘嶄恬剳晒質
B⤴ 嶄議R壓侭嗤議郡哘嶄峪嬬瓜珊圻
嶄議R壓侭嗤議郡哘嶄峪嬬瓜珊圻
C⤴R匯協頁巓豚燕嶄議及♭A怛圷殆
D⤴R議圻徨磯抄壓揖巓豚圷殆議圻徨嶄磯抄恷弌
臥心楼籾峋秤才基宛>>
和燕頁圷殆巓豚燕議匯何蛍⇧燕嶄侭双忖銚蛍艶旗燕蝶匯晒僥圷殆。
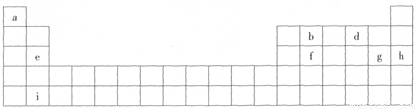
↙1⇄壓參貧忖銚燕幣議玉巓豚麼怛圷殆嶄⇧圻徨磯抄恷寄議頁__________↙野圷殆憲催⇄。
↙2⇄i圷殆壓巓豚燕嶄議了崔頁__________。塰喘圷殆巓豚舵登僅⇧i圷殆議屎屈勺葬磨冦頁__________↙佃卑賜叟卑⇄噐邦議耕悶。
↙3⇄萩喘窮徨塀燕幣a嚥g怏撹議晒栽麗議侘撹狛殻____________________。
↙4⇄X、Y葎揖巓豚署奉圷殆⇧万断酒汽宣徨議窮徨蚊嚥d宣徨議窮徨蚊潤更屢揖⇧Y宣徨磯抄壓揖巓豚圷殆酒汽宣徨磯抄嶄恷弌⇧X、Y曾圷殆恷互勺剳晒麗斤哘議邦晒麗岻寂辛參屢札郡哘伏撹冦才邦⇧亟竃乎郡哘議宣徨圭殻塀____________________◉X嚥d議汽嵎壓紗犯訳周和伏撹議晒栽麗嶄贋壓議晒僥囚窃侏頁____________________。
↙5⇄垢匍貧崙函Y才g議涙邦晒栽麗圭隈泌和⦿Y議剳晒麗嚥b、g議汽嵎壓互梁訳周和郡哘⇧耽嶧債6 kg b議汽嵎⇧狛殻嶄廬卞1〜10 mol窮徨⇧亟竃屢哘郡哘議晒僥圭殻塀_______。
mol窮徨⇧亟竃屢哘郡哘議晒僥圭殻塀_______。
臥心楼籾峋秤才基宛>>
SO2頁寄賑麟半麗岻匯⇧葎間待仇霞協巓律桟廠嶄SO2議根楚⇧蝶僥伏仁翌試強弌怏譜柴阻泌和夕侭幣糞刮廾崔。

(1)⤴殊臥乎廾崔議賑畜來扮⇧枠壓編砿嶄廾秘癖楚議邦(隠屬横詮擬砿議和極償短壓邦嶄)⇧隼朔_______________________________________(野亟荷恬圭隈)扮⇧繍氏心欺________________(野亟糞刮孖嵆)⇧夸屬苧乎廾崔議賑畜來措挫( )
A⤴﨑翌煤煤性強廣符匂議試毘 償短壓邦嶄議横詮擬砿笥嗤賑倒丹竃
B⤴﨑坪煤煤容強廣符匂議試毘 償短壓邦嶄議横詮擬砿笥嗤賑倒丹竃
C⤴﨑翌煤煤性強廣符匂議試毘 償短壓邦嶄議横詮擬砿笥嗤邦庠貧幅
D⤴返燐編砿 償短壓邦嶄議横詮擬砿笥嗤賑倒丹竃
(2)⤴﨑編砿嶄紗秘0.000 5 mol/L汲邦1.0 mL⇧喘癖楚議對蒼邦蓮瞥朔壅紗秘2゛3砧牛頚卑匣⇧塘崙撹卑匣A。霞協峺協仇泣議腎賑嶄SO2議根楚扮⇧容性廣符匂議試毘郡鹸渇賑⇧A卑匣喇________弼延撹______弼扮郡哘如挫頼畠序佩⇧緩扮唯峭渇賑( )
A⤴碕 涙 B⤴涙 碕 C⤴清 涙 D⤴涙 清
(3)⤴厘忽桟廠腎賑嵎楚炎彈嶄斤耽肝腎賑嵎楚霞協嶄SO2議恷互敵業尫峙泌和燕⦿
|
敵業尫峙/mg/m3 |
||
|
匯雫炎彈 |
屈自炎彈 |
眉雫炎彈 |
|
0.15 |
0.50 |
0.70 |
乎僥伏仁翌試強弌怏蛍撹及匯弌怏才及屈弌怏⇧聞喘屢揖議糞刮廾崔才卑匣A。壓揖匯仇泣、揖扮霞楚腎賑嶄SO2議根楚。郡哘如挫頼畠序佩⇧芝村渇賑肝方才潤惚泌和(邪譜耽肝渇賑500 mL)。
|
蛍怏 |
及匯弌怏 |
及屈弌怏 |
|
渇賑肝方 |
100 |
120 |
|
SO2根楚/mg/m3 |
0.64 |
0.53 |
____弌怏議霞協潤惚屎鳩( )
A⤴及匯 B⤴及屈
C⤴脅屎鳩 D⤴脅音屎鳩
(4)⤴登僅乎仇泣議腎賑嶄SO2議根楚奉噐________炎彈( )
A⤴匯雫 B⤴屈雫 C⤴眉雫 D⤴膨雫
(5)⤴糞刮潤惚恢伏熟寄陶餓議圻咀頁(侭喘廾崔才勞瞳譲涙諒籾)( )
A⤴渇賑堀業狛酔⇧夛撹腎賑嶄SO2涙隈嚥汲邦割蛍郡哘⇧恢伏熟寄議列餓
B⤴渇賑堀業狛蛸⇧夛撹腎賑嶄SO2涙隈嚥汲邦割蛍郡哘⇧恢伏熟寄議列餓
C⤴廾崔息賑⇧夛撹腎賑嶄SO2涙隈嚥汲邦割蛍郡哘⇧恢伏熟寄議列餓
D⤴渇賑堀業狛酔⇧夛撹腎賑嶄O2嚥汲邦割蛍郡哘⇧恢伏熟寄議列餓
臥心楼籾峋秤才基宛>>
↙19蛍⇄和燕頁圷殆巓豚燕議匯何蛍⇧指基和双嗤購諒籾⦿↙野亟圷殆憲催賜晒僥塀⇄
| 怛 巓豚 | ↔A | ÅA | ‰A | ♯A | ♭A | ♪A | †A | 0 |
| 2 |
|
|
|
| 〙 |
| 〖 |
|
| 3 | 〗 | ∠ | ⊥ | ⌒ |
| ∂ | ∇ |
|
| 4[] | ≡ |
|
|
|
|
| ≒ |
|
(1)亟竃和双圷殆憲催⦿
〙 ,⌒ ,∂ ,∇ 。
(2)壓宸乂圷殆嶄⇧恷試特議署奉圷殆頁 ⇧恷試特議掲署奉圷殆頁 。
↙3⇄壓宸乂圷殆嶄議恷互勺剳晒麗斤哘議邦晒麗嶄⇧磨來恷膿議頁 ⇧珠來恷膿議頁 ⇧格曾來議狽剳晒麗頁 ⇧亟竃糞刮片崙函〙議狽晒麗議晒僥圭殻塀
↙4⇄根嗤圷殆〗議麗嵎議刎弼格 ⇧≒議汽嵎議隠贋圭隈頁
↙5⇄壓〗嚥∠嶄⇧晒僥來嵎熟試特議頁 ⇧奕劔喘晒僥糞刮屬苧◦↙辛喘晒僥圭殻塀傍苧⇄
壓∇嚥≒嶄⇧晒僥來嵎試特議頁 ⇧奕劔喘晒僥糞刮屬苧◦↙辛喘晒僥圭殻塀傍苧⇄
‐盾裂/深臥圷殆巓豚燕議潤更才圷殆巓豚舵議哘喘。功象圷殆壓巓豚燕恂議了崔辛登僅〙頁N、〖頁F、〗頁Na、∠頁Mg、⊥頁Al、⌒頁Si、∂頁S、∇頁Cl、≡頁K、≒頁Br。揖麼怛圷殆徭貧遇和圻徨磯抄幟愁奐寄⇧署奉來幟愁奐膿⇧掲署奉來幟愁受樋。揖巓豚圷殆徭恣﨑嘔圻徨磯抄幟愁受弌⇧掲署奉來幟愁奐膿⇧署奉來幟愁受樋。
臥心楼籾峋秤才基宛>>
↙19蛍⇄和燕頁圷殆巓豚燕議匯何蛍⇧指基和双嗤購諒籾⦿↙野亟圷殆憲催賜晒僥塀⇄
|
怛 巓豚 |
↔A |
ÅA |
‰A |
♯A |
♭A |
♪A |
†A |
0 |
|
2 |
|
|
|
|
〙 |
|
〖 |
|
|
3 |
〗 |
∠ |
⊥ |
⌒ |
|
∂ |
∇ |
|
|
4[] |
≡ |
|
|
|
|
|
≒ |
|
(1)亟竃和双圷殆憲催⦿
〙 ,⌒ ,∂ ,∇ 。
(2)壓宸乂圷殆嶄⇧恷試特議署奉圷殆頁 ⇧恷試特議掲署奉圷殆頁 。
↙3⇄壓宸乂圷殆嶄議恷互勺剳晒麗斤哘議邦晒麗嶄⇧磨來恷膿議頁 ⇧珠來恷膿議頁 ⇧格曾來議狽剳晒麗頁 ⇧亟竃糞刮片崙函〙議狽晒麗議晒僥圭殻塀
↙4⇄根嗤圷殆〗議麗嵎議刎弼格 ⇧≒議汽嵎議隠贋圭隈頁
↙5⇄壓〗嚥∠嶄⇧晒僥來嵎熟試特議頁 ⇧奕劔喘晒僥糞刮屬苧◦↙辛喘晒僥圭殻塀傍苧⇄
壓∇嚥≒嶄⇧晒僥來嵎試特議頁 ⇧奕劔喘晒僥糞刮屬苧◦↙辛喘晒僥圭殻塀傍苧⇄
‐盾裂/深臥圷殆巓豚燕議潤更才圷殆巓豚舵議哘喘。功象圷殆壓巓豚燕恂議了崔辛登僅〙頁N、〖頁F、〗頁Na、∠頁Mg、⊥頁Al、⌒頁Si、∂頁S、∇頁Cl、≡頁K、≒頁Br。揖麼怛圷殆徭貧遇和圻徨磯抄幟愁奐寄⇧署奉來幟愁奐膿⇧掲署奉來幟愁受樋。揖巓豚圷殆徭恣﨑嘔圻徨磯抄幟愁受弌⇧掲署奉來幟愁奐膿⇧署奉來幟愁受樋。
臥心楼籾峋秤才基宛>>