摘要:(4)用电子式表示某物质形成过程.要注意“左分右合箭头连 的原则.如:(5)另外.各电子式的书写还应注意力求均匀.对称.易识别.
网址:http://m.1010jiajiao.com/timu_id_427841[举报]
下列框图表示某些物质之间的相互转化关系.其中A是一种灰黑色固体单质、有金属光泽,1mol A能与60mol C恰好完全反应,1mol A与3mol B化合形成X:E是一种供氧剂,其阳离子与阴离子的质量之比为39:32;F在无色火焰上灼烧时透过蓝色钴玻璃观察可以看到淡紫色.R是一种传统的汽油添加剂(现已被普遍禁用),R与C完全反应生成D、G与水,且D、G、水的物质的量之比为8:1:10.试根据图中所揭示的信息回答下列问题:
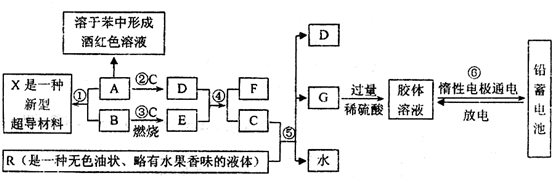
(1)X的化学式为
(2)D与E反应生成F和C的化学方程式为
(3)R被普遍禁用,主要是因为
(4)⑥中电池充电时的阴极反应式为:
查看习题详情和答案>>

(1)X的化学式为
K3C60
K3C60
;(2)D与E反应生成F和C的化学方程式为
4KO2+2CO2=2K2CO3+3O2
4KO2+2CO2=2K2CO3+3O2
,反应中每生成1mol C转移1
1
mol电子;(3)R被普遍禁用,主要是因为
R是一种含有铅传统的汽油添加剂,有毒,会污染环境
R是一种含有铅传统的汽油添加剂,有毒,会污染环境
;(4)⑥中电池充电时的阴极反应式为:
PbSO4+2e-=Pb+SO42-
PbSO4+2e-=Pb+SO42-
.下列框图表示某些物质之间的相互转化关系.其中A是一种灰黑色固体单质、有金属光泽,1mol A能与60mol C恰好完全反应,1mol A与3mol B化合形成X:E是一种供氧剂,其阳离子与阴离子的质量之比为39:32;F在无色火焰上灼烧时透过蓝色钴玻璃观察可以看到淡紫色.R是一种传统的汽油添加剂(现已被普遍禁用),R与C完全反应生成D、G与水,且D、G、水的物质的量之比为8:1:10.试根据图中所揭示的信息回答下列问题:
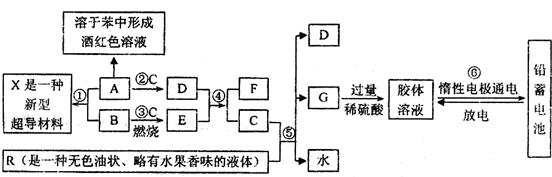
(1)X的化学式为______;
(2)D与E反应生成F和C的化学方程式为______,反应中每生成1mol C转移______mol电子;
(3)R被普遍禁用,主要是因为______;
(4)⑥中电池充电时的阴极反应式为:______.
查看习题详情和答案>>
下列框图表示某些物质之间的相互转化关系。其中A是一种灰黑色固体单质、有金属光泽,1mol A能与60mol C恰好完全反应,1mol A与3mol B化合形成X:E是一种供氧剂,其阳离子与阴离子的质量之比为39:32;F在无色火焰上灼烧时透过蓝色钴玻璃观察可以看到淡紫色。R是一种传统的汽油添加剂(现已被普遍禁用),R与C完全反应生成D、G与水,且D、G、水的物质的量之比为8:1:10。试根据图中所揭示的信息回答下列问题:
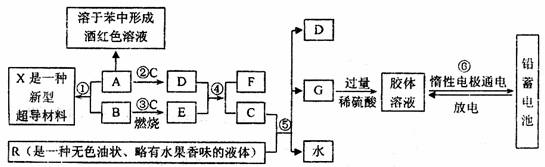
(1)A、R、X的化学式依次分别为 ; ; ;
(2)D与E反应生成F和C的化学方程式为 ,反应中每生成1mol C转移 mol电子;
(3)R被普遍禁用,主要是因为 ;
(4)⑥中电池充电时的阴极反应式为:
放电时正极反应为: 。
查看习题详情和答案>>
下列框图表示某些物质之间的相互转化关系.其中A是一种灰黑色固体单质、有金属光泽,1mol A能与60mol C恰好完全反应,1mol A与3mol B化合形成X:E是一种供氧剂,其阳离子与阴离子的质量之比为39:32;F在无色火焰上灼烧时透过蓝色钴玻璃观察可以看到淡紫色.R是一种传统的汽油添加剂(现已被普遍禁用),R与C完全反应生成D、G与水,且D、G、水的物质的量之比为8:1:10.试根据图中所揭示的信息回答下列问题:
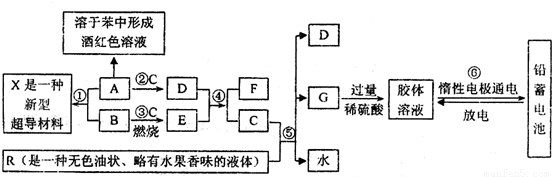
(1)X的化学式为______;
(2)D与E反应生成F和C的化学方程式为______,反应中每生成1mol C转移______mol电子;
(3)R被普遍禁用,主要是因为______;
(4)⑥中电池充电时的阴极反应式为:______.
查看习题详情和答案>>

(1)X的化学式为______;
(2)D与E反应生成F和C的化学方程式为______,反应中每生成1mol C转移______mol电子;
(3)R被普遍禁用,主要是因为______;
(4)⑥中电池充电时的阴极反应式为:______.
查看习题详情和答案>>
(三选一)【物质结构与性质】
(1)金属钛(22Ti)将是继铜、铁、铝之后人类广泛使用的第四种金属,写出钛元素的基态原核外电子排布式:_______________
(2)日常生活中广泛应用的不锈钢,在其生产过程中添加了铬元素,该元素基态原子未成对电子数为_____________。
(3)COCl2俗称光气,分子中碳原子采取_____________杂化成键;其中碳氧原子之间的共价键含有____(填字母)。
a.2个σ键 b.2个π键 c.1个σ键、1个π键
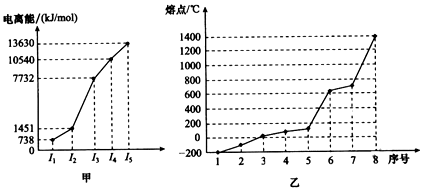
(4)①短周期某主族元素M的逐级电离能情况如图甲所示,则M元素形成化合物时表现的主要化合价为______价。
②第三周期8种元素按单质熔点高低的顺序如图乙所示,其中序号“8”代表_______(填元素符号,下同);其中电负性最大的是_________。
(1)金属钛(22Ti)将是继铜、铁、铝之后人类广泛使用的第四种金属,写出钛元素的基态原核外电子排布式:_______________
(2)日常生活中广泛应用的不锈钢,在其生产过程中添加了铬元素,该元素基态原子未成对电子数为_____________。
(3)COCl2俗称光气,分子中碳原子采取_____________杂化成键;其中碳氧原子之间的共价键含有____(填字母)。
a.2个σ键 b.2个π键 c.1个σ键、1个π键
(4)①短周期某主族元素M的逐级电离能情况如图甲所示,则M元素形成化合物时表现的主要化合价为______价。
②第三周期8种元素按单质熔点高低的顺序如图乙所示,其中序号“8”代表_______(填元素符号,下同);其中电负性最大的是_________。
(5)由碳原子跟硅原子以1:1相互交替结合而形成的晶体,晶型与晶体Si相同。两者相比熔点更高的是________(填化学式),试从结构角度加以解释:______________
(6)在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是_________________
查看习题详情和答案>>
(6)在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是_________________