网址:http://m.1010jiajiao.com/timu_id_41466[举报]
一、选择题:(共44分)
1.D 2.A 3.D 4.B 5.A 6.D 7.C 8.C 9.A 10.C 11.B
12.D 13.B 14.A 15.C 16.C 17.A 18.B 19.A 20.C 21.B 22.B
二. 填空题(本题共4小题,共48分)
23.(8分,每空2分) K2Cr2O7 是氧化剂, HCl 是还原剂,
Cl 元素被氧化, Cr 元素被还原,
Cl2 是氧化产物, CrCl3 是还原产物。
 |
K2Cr2O7 +14HCl=2KCl+2CrCl3+3Cl2↑+7H2O(标出电子转移方向和数目)
24.(14分,每空2分)
(1)化学式:A Ba(OH)2 B H2SO
(2)反应①、②、⑤的离子方程式
① SO42-+ 2H++ ba2++2oh-= baSo4↓+2H2O
② CO32-+ 2H+ = CO2 ↑+ H2O
⑤ Mg2+ + 2oh- = Mg(OH)2↓
25.(14分,每空2分)三种离子: OH- 、 K+ 、 Cl- 。
铁粉 , 银 ,
Ag+ 、 Fe3+ , NO3- 、 K+ 。
26.(12分,每空2分) (1)
(2)500mL容量瓶、烧杯、玻璃棒、胶头滴管。
(3)A、_无影响____ B、____偏高_
C、__偏低____ D、 _偏低_ 。
三. 计算题(本题共1小题,共8分)
27.(1)氧化剂是 MnO2 (2分 )
(2) ①168mL(3分 )
②1mol (3分 )

(1)某同学认为MnO2与浓HCl反应制得的Cl2中含有HCl气体,该同学设计如图1所示装量时行验证.
已知B中试剂为CCl4,则:
①判定含有HCl气体的实验现象为:
②装置A中两仪器名称分别为:
③有人认为可将D装置溶液换成另一溶液,你认为可能为:
(2)某课外研究小组设计如图所示的实验过程,用石油化学工业的废气催化剂(主要成份为Ag/α-Al2O3)来回收金属银和α-Al2O3,部分操作过程省略.α-Al2O3作为催化剂的载体,且不溶于硝酸:
Ag/α-Al2O3

①Ag/α-Al2O3加HNO3溶解可选用图2所示装置中的
②实验操作II中,所需要的主要玻璃仪器有
③实验操作II中能否用自来水代替蒸馏水?
④操作I中所发生的离子反应方程式:
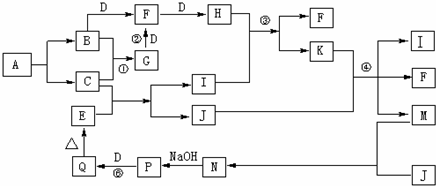
回答下列问题:
(1)A的电子式为
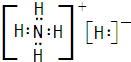
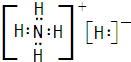
(2)K的浓溶液久置会变色,变色过程中发生反应的化学方程式为
(3)实验室检验含A中的阳离子的可溶性盐时的操作方法是
(4)反应②⑥的化学方程式为:②
| ||
| ||
查得资料:某品牌牙膏摩擦剂由二氧化硅、碳酸钙、碳酸镁组成,还可能含有氢氧化铝和碳酸氢钙;牙膏中其它成分易溶于水,遇到盐酸无气体生成.
Ⅰ、摩擦剂中碳酸氢钙和氢氧化铝的定性检验:取适量牙膏样品,加水搅拌、过滤.并设计如下实验方案对该品牌牙膏摩擦剂的成分进行测定、验证假设.请写出实验步骤以及预期现象和结论(可不填满).
限选试剂:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、二氧化碳
| 实验步骤 | 预期现象和结论 | 步骤1:取适量牙膏样品加水充分搅拌、过滤,得滤液A和沉淀B. | / | 步骤2:取适量滤液A于试管中, |
有 |
步骤3:取适量沉淀B于试管中,加入过量 |
/ | 步骤4:往所得滤液中通入过量二氧化碳. | 产生成白色沉淀, |
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定P中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.
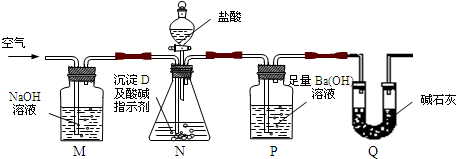
依据实验过程回答下列问题:
(1)实验过程中先后两次鼓入空气,第二次鼓入空气的目的是:
(2)实验中准确称取沉淀D1.76g样品三份,进行三次测定,测得BaCO3平均质量为3.94g.则D中碳酸钙的质量分数为
 [化学-化学与技术]
[化学-化学与技术]元素铝是在生产、生活中应用广泛的金属元素.
(1)从矿石提取氧化铝:矿石与NaOH溶液高温反应,然后降温析出晶体,再经净化和高温煅烧得到氧化铝.降温析出晶体时的反应方程式为:
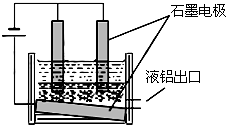
(2)氧化铝是工业电解冶炼铝的重要原料,生产中加入冰晶石(Na3AlF6),其作用是
①阴极的反应式
②在电解池工作过程中,需要不断补充阳极材料,原因是
(3)有资料介绍:溶液中铝元素以氢氧化物[用Al(OH)3表示]形式存在的pH范围是3.8~10.现有A、B两种均含铝元素形成的某种离子溶液,其pH分别为1、13,两溶液等体积混合时反应的离子方程式为
(4)一种新型高效净水剂PAFC--聚合氯化铁铝[A1Fe(OH)nCl6-n]m,广泛用于日常生活用水和工业污水的处理.有关PAFC的说法正确的是
A.PAFC中铁元素显+2价
B.PAFC用于净水时,比用相同量的氯化铝和氯化铁对水的pH改变小
C.PAFC可看作一定比例的氯化铁与氯化铝水解的中间产物
D.PAFC在强酸性和强碱性溶液中都能稳定存在.
(1)工业生产可以用NH3(g)与CO2(g)经过两步反应生成尿素,两步反应的能量变化示意图如图:
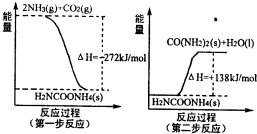
则NH3(g)与CO2(g)反应生成尿素的热化学方程式为
(2)已知反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H=akJ.mol-1.测得在不同温度下,该反应的平衡常数K随温度的变化如下:
| 温度/ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
②700℃反应达到平衡后,要使该平衡向右移动,其他条件不变时,可以采取的措施有
A.缩小反应器容积 B.增加Fe的物质的量
C.升高温度到900℃D.使用合适的催化剂
(3)硫酸厂常用NaOH溶液吸收SO2废气.当吸收液呈中性时,溶液中离子浓度关系正确的是[已知n(SO
2- 3 |
- 3 |
A、c(Na+)=2c(SO
2- 3 |
- 3 |
B、c(Na+)>c(HSO
- 3 |
2- 3 |
C、c(Na+)+c(H+)=c(SO
2- 3 |
- 3 |