网址:http://m.1010jiajiao.com/timu_id_411949[举报]
(11分)某研究性学习小组为证明2Fe3+ + 2I-  2Fe2+
+ I2为可逆反应(即反应存在一定的限度),设计如下几种方案。已知FeF63-是一种无色的稳定的络离子。
2Fe2+
+ I2为可逆反应(即反应存在一定的限度),设计如下几种方案。已知FeF63-是一种无色的稳定的络离子。
按要求回答下列问题。
方案甲:
取5mL 0.1mol/L KI溶液,滴加2ml 0.1mol/L 的FeCl3溶液,再继续加入2mL CCl4,充分振荡。静置、分层,再取上层清液,滴加KSCN溶液。
(1)甲方案中能证明该反应为可逆反应的现象是 。
(2)有同学认为该方案设计不够严密,即使该反应为不可逆反应也可能出现上述现象,其原因是 。
方案乙:
取5mL 0.1mol/L KI溶液,滴加2ml 0.1mol/L 的FeCl3溶液,溶液呈棕黄色,再往溶液中滴加NH4F溶液,若看到 现象,即可证明该反应为可逆反应,请解释产生该现象的原因 。
方案丙:
设计如图原电池装置,接通灵敏电流计,指针向右偏转(注:灵敏电流计指针总是偏向电源正极),随着时间进行电流计读数逐渐变小,最后读数变为零。
当指针读数变零后,在乙烧杯中加入1mol/L FeCl2溶液,若观察到灵敏电流计的指针向 方向偏转(填“左”、“右”或“不移动”),即可判断该反应为可逆反应,此时甲中石墨电极上的电极反应式为 。

【解析】(1)根据实验数据可知碘化钾是过量的,若反应是可逆反应,则溶液中一定存在铁离子,同时也必须生成单质碘。所以可以通过检验铁离子和单质碘来证明。
(2)因为碘离子和亚铁离子在空气中也可以被氧气氧化生成单质碘和铁离子,所以方案不是很严密。
(3)可以依据外界条件对平衡的影响来验证。因为Fe3+与F-络合生成无色的FeF63-,促使2Fe3+ +
2I-  2Fe2+ + I2平衡朝逆反应方向移动,所以溶液颜色会变浅。
2Fe2+ + I2平衡朝逆反应方向移动,所以溶液颜色会变浅。
(4)在原电池中负极是失去电子的,碘离子失去电子,所以电子是从甲池流向乙池,所以电流计的指针向左偏转。
查看习题详情和答案>>
(11分)某研究性学习小组为证明2Fe3+ + 2I- 2Fe2++ I2为可逆反应(即反应存在一定的限度),设计如下几种方案。已知FeF63-是一种无色的稳定的络离子。
按要求回答下列问题。
方案甲:
取5mL0.1mol/L KI溶液,滴加2ml 0.1mol/L 的FeCl3溶液,再继续加入2mL CCl4,充分振荡。静置、分层,再取上层清液,滴加KSCN溶液。
(1)甲方案中能证明该反应为可逆反应的现象是 。
(2)有同学认为该方案设计不够严密,即使该反应为不可逆反应也可能出现上述现象,其原因是 。
方案乙:
取5mL0.1mol/L KI溶液,滴加2ml 0.1mol/L 的FeCl3溶液,溶液呈棕黄色,再往溶液中滴加NH4F溶液,若看到 现象,即可证明该反应为可逆反应,请解释产生该现象的原因 。
方案丙:
设计如图原电池装置,接通灵敏电流计,指针向右偏转(注:灵敏电流计指针总是偏向电源正极),随着时间进行电流计读数逐渐变小,最后读数变为零。
当指针读数变零后,在乙烧杯中加入1mol/L FeCl2溶液,若观察到灵敏电流计的指针向 方向偏转(填“左”、“右”或“不移动”),即可判断该反应为可逆反应,此时甲中石墨电极上的电极反应式为 。
【解析】(1)根据实验数据可知碘化钾是过量的,若反应是可逆反应,则溶液中一定存在铁离子,同时也必须生成单质碘。所以可以通过检验铁离子和单质碘来证明。
(2)因为碘离子和亚铁离子在空气中也可以被氧气氧化生成单质碘和铁离子,所以方案不是很严密。
(3)可以依据外界条件对平衡的影响来验证。因为Fe3+与F-络合生成无色的FeF63-,促使2Fe3+ +2I- 2Fe2+ + I2平衡朝逆反应方向移动,所以溶液颜色会变浅。
(4)在原电池中负极是失去电子的,碘离子失去电子,所以电子是从甲池流向乙池,所以电流计的指针向左偏转。
查看习题详情和答案>>
(1)甲同学的实验说明FeCl3溶液和KI溶液发生了反应,用离子方程式表示
(2)乙同学在实验中观察不到甲同学的实验现象,其原因分析合理的是
A.Fe3+被F-还原成Fe2+,使溶液中不再存在Fe3+
B.Fe3+与F-结合成难电离物质,不再和I-结合
C.I-、F-、F-、NH4+结合成难电离的物质,不再和Fe3+反应
(3)乙同学所用的NH4F溶液是用塑料瓶盛装的,可否改用玻璃瓶
(1)下列说法中不正确的是
A.三氧化二铝属于碱性氧化物
B.用热的纯碱溶液洗涤沾有油污的物品时,发生的主要是化学变化
C.光导纤维的基本原料为SiO2
D.液氨、液氯、液态氯化氢都是非电解质
E.丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
(2)人们对酸碱的认识,已有几百年的历史,经历了一个由浅入深,由低级到高级的认识过程.
①1887年阿仑尼乌斯提出电离理论.
②1923年丹麦化学家布朗斯特和英国化学家劳莱提出了质子论.凡是能够释放质子(氢离子)的任何含氢原子的分子或离子都是酸;凡是能与质子(氢离子)结合的分子或离子都是碱.按质子理论:下列粒子的水溶液既可看作酸又可看作碱的是
A.H2O B.NH4+C.OH-D.HCO3-E.CH3COO-F.Cl-
③1923年路易斯(Lewis)提出了广义的酸碱概念.凡是能给出电子对而用来形成化学键的物质是碱;凡是能和电子对结合的物质都是酸.
如:酸(电子对接受体)碱(电子对给予体)反应产物H++[:OH]-→H:OH
试指出下列两个反应中的酸或碱:
H3BO3+H2O═H++[B(OH)4]-;该反应中的碱是
CuCl2+4NH3═[Cu (NH3)4]2++2Cl-;该反应中的酸是
| 编号 | 信 息 |
| 1 | D为地壳中含量最高的元素组成的单质 |
| 2 | E为酸性氧化物,不溶于水,能与某种酸反应 |
| 3 | F不溶于水,F用于制备干燥剂以及催化剂的载体 |
| 4 | H为淡黄色固体化合物 |
| 5 | 电解饱和J溶液是工业生产中的重要反应 |
| 6 | C为离子化合物,阴、阳离子均含有金属元素 |
| 7 | K为酸雨的主要成分 |
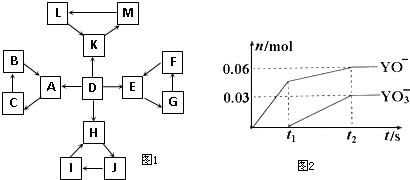
(1)写出H的电子式:
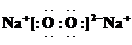
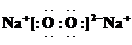
(2)常温下测得一定浓度的C溶液的pH=11,用离子方程式表示其原因:
(3)写出向C溶液中通入过量CO2的离子方程式:
(4)金属铜与L浓溶液反应生成K,该反应的化学方程式是:
| ||
| ||
若标准状况下,生成K的体积为56L,此时转移的电子数为
(5)电解饱和J溶液产物之一为Y2,将一定量的Y2 通入一定浓度的氢氧化钾溶液中,两者恰好完全反应时(已知反应过程放热),生成物中有三种含Y元素的离子,其中两种离子的物质的量(n)与反应时间(t)的变化示意图如图2所示.写出该氢氧化钾溶液中通入Y2的总化学方程式: