摘要:铜片:2H++2e―=H2↑实验1:在一个U形管中注入CuCl2溶液.插入2根石墨棒作电极.把湿润的碘化钾淀粉试纸放在与电池正极相连的电极附近.接通直流电源.观察U形管内发生的变化及试纸颜色的变化.现象与解释:接通直流电源后.电流表指针发生偏转.阴极石墨棒上逐渐覆盖一层红色物质.这是析出的金属铜,在阳极石墨棒上有气泡放出.并可闻到刺激性的气味.同时看到湿润的碘化钾淀粉试纸变蓝.可以断定放出的气体是Cl2.这一变化过程可表示如下:阳极:2Cl―-2e―=Cl2↑阴极:Cu2++2e―=Cu实验2:将上述“实验1 的装置中的CuCl2溶液换成饱和食盐水.进行类似的实验.现象与解释:在U形管的两个电极上都有气体放出.阳极放出的气体有刺激性气味.并能使湿润的碘化钾淀粉试纸变蓝.说明放出的是Cl2,阴极放出的气体是H2.同时发现阴极附近溶液变红.这说明溶液里有碱性物质生成.这一变化过程可表示如下:阳极:2Cl―-2e―=Cl2↑阴极:2H++2e―=H2↑
网址:http://m.1010jiajiao.com/timu_id_411285[举报]
将铜片和铝片用导线连接后插入盛有浓硝酸的烧杯中组成原电池,此原电池的负极及其电极反应分别是
A. Al, Al- 3e-=Al3+ B. Cu, Cu-2e-=Cu2+
C. Al, 2H++2e-=H2↑ D. Cu, 2H++NO3-+e-=NO2↑+H2O
查看习题详情和答案>>右图是某研究小组进行化学能与电能相互转化的实验装置图。
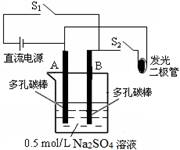 下列说法正确的是
下列说法正确的是
A.该装置中只存在2种形式的能量转化
B.只闭合S1时,A电极发生还原反应
C.闭合S1一段时间后断开,闭合S2,
A电极的反应式为:2H+ + 2e- = H2↑
D.闭合S1一段时间后断开,闭合S2,
溶液的pH升高
查看习题详情和答案>>
将铜片和铝片用导线连接后插入盛有浓硝酸的烧杯中组成原电池,此原电池的负极及其电极反应分别是
A. Al, Al- 3e-=Al3+ B. Cu, Cu-2e-=Cu2+
C. Al, 2H++2e-=H2↑ D. Cu, 2H++NO3-+e-=NO2↑+H2O
查看习题详情和答案>>
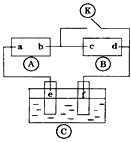
 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽。接通电路后发现
为电镀槽。接通电路后发现 上的c点显红色。为实现铁上镀锌,接通
上的c点显红色。为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述正确的是
后,使c、d两点短路.下列叙述正确的是