网址:http://m.1010jiajiao.com/timu_id_409394[举报]
(本题14分)铅是一种重金属,相对原子量为207。铅和铅的化合物有很多用途,如蓄电池等,但铅类化合物大多有毒,燃煤厂、金属冶炼厂等都有主要的铅污染源。铅一旦进入人体会累积,对人脑、肾脏和造血功能有损害。为了了解环境中的铅污染问题,小红他同学进行了如下的研究。
【小题1】在走访调查中,小红观察到某乡镇颜料厂排出的废水带有颜色,经鉴定含有铅。为了测定废水中铅的浓度,他设计了如下实验步骤:
(1)步骤中过滤需要的玻璃仪器是 、 和玻璃棒。
(2)步骤中a操作称为 ,缺少此操作,测得结果 (填“偏高”、“偏低”、或“无影响”)。
【小题2】通过研究,小红提出了一系列降低铅对环境污染的建议,下列建议中不恰当的是
| A.使用无铅汽油 |
| B.开发新的无铅燃料 |
| C.倡导使用铅蓄电池作动力的电动车 |
| D.燃煤电厂、金属冶炼厂的废气经除尘后排放。 |
(本题共15分)你注意到汽车加油站内的标牌了吗?某些省市加油站提供的汽油标号由90号、93号换成了E90、E93,后者是在汽油中加入了10%的燃料乙醇而制得的乙醇汽油。
【小题1】燃料乙醇的生产过程可由下图表示:
(1)粉碎玉米的目的是: 。
(2)生产过程中为了检验淀粉水解是否完全,可使用试剂是 。
(3)步骤a的操作是( )。
| A.蒸发 | B.萃取 | C.蒸馏 | D.分液 |
(5)以玉米等淀粉原料生产乙醇的化学反应可用下式表示:
根据上述反应式,可以算出100kg淀粉理论上可生产无水乙醇 kg。(相对原子质量:C-12 H-1 O-16)
【小题2】到目前为止,我国已有上百个地市使用乙醇汽油。
(1)为了便于区分燃料乙醇和食用乙醇,常在燃料乙醇中添加少量煤油,这里利用了煤油的物理性质是: 。
(2)含10%乙醇的汽油在储存和运输过程中应特别注意防水,如果混入了水,汽油中会出现的现象是 。
【小题3】右图是燃料乙醇的生产和消费过程示意图。虽然燃料乙醇的使用缓解了汽车能源的紧张状况,但仍存在一些问题。由此可知,燃料乙醇( )

| A.是最理想的绿色能源 |
| B.提供的能量来自于太阳能 |
| C.生产和消费过程对空气没有任何影响 |
| D.生产过程中将消耗大量粮食,以避免粮食过剩 |
(本题共15分)空气中CO2浓度的持续走高引起人们的高度重视。一些科学家认为,人类不仅要努力减少CO2的排放,还要尽快想办法清除空气中过多的CO2。为此,他们设想了一系列“捕捉”和“封存” CO2的方法。
【小题1】方法Ⅰ:一些科学家利用太阳能加热的反应器“捕捉”空气中的CO2,如下图所示。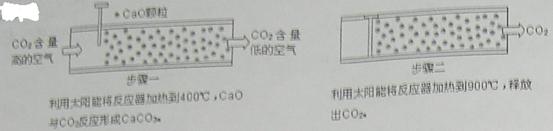
(1)步骤一中的CaO俗称 。
(2)步骤二中发生反应的化学方程式是 ,该反应 (填“是”或“不是”)步骤一中反应的逆反应。
【小题2】方法Ⅱ:另一些科学家利用NaOH溶液的喷淋“捕捉”空气中的CO2,如右图所示。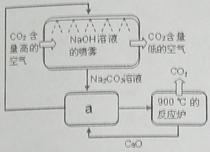
(1)NaOH溶液喷成雾状是为了 。
(2)右图a环节中,物质分离的基本操作是 。
(3)为了尽量减少成本,在整个流程中,循环利用的物质有CaO和 。
【小题3】下列溶液中,同样能用于“捕捉”二氧化碳的是( )。
| A.KNO3溶液 | B.CaCl2溶液 | C.CuSO4溶液 | D.Na2CO3溶液 |
①方法Ⅰ将受到地域的限制
②方法Ⅱ的能耗太大
③方法Ⅰ中使用的是氧化钙颗粒而不是氧化钙粉末
④方法Ⅱ中的物质可以循环利用,但方法Ⅰ中的却不能
| A.①③ | B.①② | C.②④ | D.③④ |
可见,要真正实现“碳捕捉”和“碳封存”的设想,科学家任重而道远。 查看习题详情和答案>>
(12分)(1)有A、B、C、D四种烃,在常温下A、C是气体,B、D是液体。A完全燃烧后生成二氧化碳与水物质的量之比是2:1;B的分子量是A的三倍;C既不能使酸性高锰酸钾溶液褪色也不能使溴水褪色,但在光照条件下最多可与六倍体积氯气发生反应;燃烧相同物质的量C与D,生成二氧化碳的体积比为1:4,D不能使溴水褪色但能使酸性高锰酸钾溶液褪色,在催化剂作用下1摩尔D能与3摩尔氢气完全反应;在铁粉存在下与溴反应生成一溴代物只有一种。试推断有机物A、B、C、D,分别写出结构简式:
A:______________ B:_____________
C:______________ D:___________
(2)相对分子质量为72的某烃,其分子式是___________,若此有机物的一氯代物分子中有两个-CH3、两个-CH2-、一个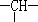 和一个-Cl,它可能的结构有__________种.(本题不考虑对映异构体)
和一个-Cl,它可能的结构有__________种.(本题不考虑对映异构体)
【解析】(1) A完全燃烧后生成二氧化碳与水物质的量之比是2:1,根据原子守恒可知A中碳原子和氢原子的个数比是1︰1,又因为A是气体,所以A是乙炔。B的分子量是A的三倍,则B的分子式为C6H6。因为B是液体,所以B是苯。根据C的性质可知C应是烷烃,在光照条件下最多可与六倍体积氯气发生反应,所以C是乙烷。燃烧相同物质的量C与D,生成二氧化碳的体积比为1:4,因此D中含有8个碳原子。根据D的性质可判断D是苯的同系物。在铁粉存在下与溴反应生成一溴代物只有一种,所以D是对二甲苯。
(2)因为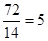 ……2,所以是烷烃,分子式为C5H12.2个甲基最多1个是支链,若2个甲基都不是支链,则氯原子的位置有2种,即2-氯戊烷和3-氯戊烷。若其中1个甲基是取代基,则甲基支链的位置也是2种,即3-甲基-1-氯丁烷和2-甲基-1-氯丁烷。
……2,所以是烷烃,分子式为C5H12.2个甲基最多1个是支链,若2个甲基都不是支链,则氯原子的位置有2种,即2-氯戊烷和3-氯戊烷。若其中1个甲基是取代基,则甲基支链的位置也是2种,即3-甲基-1-氯丁烷和2-甲基-1-氯丁烷。
查看习题详情和答案>>
(12分)(1)有A、B、C、D四种烃,在常温下A、C是气体,B、D是液体。A完全燃烧后生成二氧化碳与水物质的量之比是2:1;B的分子量是A的三倍;C既不能使酸性高锰酸钾溶液褪色也不能使溴水褪色,但在光照条件下最多可与六倍体积氯气发生反应;燃烧相同物质的量C与D,生成二氧化碳的体积比为1:4,D不能使溴水褪色但能使酸性高锰酸钾溶液褪色,在催化剂作用下1摩尔D能与3摩尔氢气完全反应;在铁粉存在下与溴反应生成一溴代物只有一种。试推断有机物A、B、C、D,分别写出结构简式:
A:______________ B:_____________
C:______________ D:___________
(2)相对分子质量为72的某烃,其分子式是___________,若此有机物的一氯代物分子中有两个-CH3、两个-CH2-、一个![]() 和一个-Cl,它可能的结构有__________种.(本题不考虑对映异构体)
和一个-Cl,它可能的结构有__________种.(本题不考虑对映异构体)
【解析】(1) A完全燃烧后生成二氧化碳与水物质的量之比是2:1,根据原子守恒可知A中碳原子和氢原子的个数比是1︰1,又因为A是气体,所以A是乙炔。B的分子量是A的三倍,则B的分子式为C6H6。因为B是液体,所以B是苯。根据C的性质可知C应是烷烃,在光照条件下最多可与六倍体积氯气发生反应,所以C是乙烷。燃烧相同物质的量C与D,生成二氧化碳的体积比为1:4,因此D中含有8个碳原子。根据D的性质可判断D是苯的同系物。在铁粉存在下与溴反应生成一溴代物只有一种,所以D是对二甲苯。
(2)因为![]() ……2,所以是烷烃,分子式为C5H12.2个甲基最多1个是支链,若2个甲基都不是支链,则氯原子的位置有2种,即2-氯戊烷和3-氯戊烷。若其中1个甲基是取代基,则甲基支链的位置也是2种,即3-甲基-1-氯丁烷和2-甲基-1-氯丁烷。
……2,所以是烷烃,分子式为C5H12.2个甲基最多1个是支链,若2个甲基都不是支链,则氯原子的位置有2种,即2-氯戊烷和3-氯戊烷。若其中1个甲基是取代基,则甲基支链的位置也是2种,即3-甲基-1-氯丁烷和2-甲基-1-氯丁烷。
查看习题详情和答案>>