摘要:2H2S+O22S+2H2O 关于改换溶剂法则是利用一种物质在不同溶剂中溶解度相差悬殊的性质来制备溶胶.如把松香的酒精溶液滴入水中.由于松香在水中溶解度很低.溶质以胶粒大小析出.即形成松香的水溶胶. 无论采用哪种方法.制得的溶胶常含有很多电解质或其他杂质.除了与胶粒表面吸附的离子维持平衡的适量电解质具有稳定胶体的作用外.过量的电解质反而会影响溶胶的稳定性.因此.制备好的溶胶常常需要作净化处理.最常用的净化方法就是渗析. 例题精讲例1下列物质中既属于无机物.又属于碱的是( ) A.Na2CO3 B.CH3OH C.CH3CH2OH D.Cu(OH)2 解析:Na2CO3是无机物.但属于盐,CH3OH和CH3CH2OH为有机物,Cu(OH)2为碱且为无机物.故答案应选D. 答案:D例2用特殊方法把固体物质加工到纳米级的超细粉末粒子.然后制得纳米材料.下列分散系中的分散质的粒子的大小和这种纳米粒子大小具有相同的数量级的是( ) A.溶液 B.悬浊液 C.胶体 D.乳浊液 解析:1nm-100nm就是胶体分散系中粒子的大小.跟这种超细粉末粒子大小具有相同数量级. 答案:C
网址:http://m.1010jiajiao.com/timu_id_404819[举报]
有A、B、C、D、E五种短周期元素,其元素特征信息如下表:
回答下列问题:
(1)写出下列元素的名称:C
(2)E在元素周期表中的位置是
(3)B、C、D的简单离子半径由大到小的顺序是
(4)写出D单质与A、E形成的化合物的水溶液反应的离子方程式:
查看习题详情和答案>>
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 其阴离子带两个单位的负电荷,单质是空气主要成分之一 |
| C | 其阳离子与B的阴离子具有相同的电子层结构,其原子的最外层电子数是次外层的1/4 |
| D | 其氢氧化物和氧化物都有两性,且与C同周期 |
| E | 与C同周期,其原子半径在该周期最小 |
(1)写出下列元素的名称:C
镁
镁
,E氯
氯
.(2)E在元素周期表中的位置是
三
三
周期ⅦA
ⅦA
族.(3)B、C、D的简单离子半径由大到小的顺序是
O2->Mg2+>Al3+
O2->Mg2+>Al3+
(用化学式表示).(4)写出D单质与A、E形成的化合物的水溶液反应的离子方程式:
2Al+6H+=2 Al3++3H2↑
2Al+6H+=2 Al3++3H2↑
.
盐R的化学式为XmYnZp(X、Y、Z为三种不同离子),其组成元素均为短周期元素,取两份等质量等浓度R的水溶液各5mL进行如下实验:
Ⅰ.取一份R的水溶液与过量的Ba(OH)2溶液反应,反应过程中生成白色沉淀,沉淀量先增加后减少,最终剩余沉淀甲2.33g,且甲不溶于稀盐酸.
Ⅱ.取另一份R的水溶液与过量的NaOH溶液混合加热,生成具有刺激性气味的气体乙0.112L(标准状况),乙能使湿润的红色石蕊试纸变蓝.
据此回答:
(1)写出R和甲的化学式:R ,甲 ,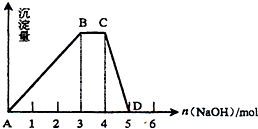
(2)另取1L R的水溶液,向其中逐滴加入NaOH溶液,所得沉淀与加入的NaOH的物质的量关系如图所示.则:
①R溶液的物质的量浓度为 ;
②BC段表示的含义是 ;
③CD段反应的离子方程式为 .
查看习题详情和答案>>
Ⅰ.取一份R的水溶液与过量的Ba(OH)2溶液反应,反应过程中生成白色沉淀,沉淀量先增加后减少,最终剩余沉淀甲2.33g,且甲不溶于稀盐酸.
Ⅱ.取另一份R的水溶液与过量的NaOH溶液混合加热,生成具有刺激性气味的气体乙0.112L(标准状况),乙能使湿润的红色石蕊试纸变蓝.
据此回答:
(1)写出R和甲的化学式:R

(2)另取1L R的水溶液,向其中逐滴加入NaOH溶液,所得沉淀与加入的NaOH的物质的量关系如图所示.则:
①R溶液的物质的量浓度为
②BC段表示的含义是
③CD段反应的离子方程式为