摘要:>4.4红橙黄酚酞5<8~10>10无色浅红红石蕊8<5~8>8红紫蓝(2)根据滴定曲线和指示剂的发色范围选用指示剂.从上面滴定曲线图可依次看出
网址:http://m.1010jiajiao.com/timu_id_404753[举报]
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
D
D
B
C
C
B
D
A
C
D
D
C
C
A
AD
B
17、3.2 ,D
18、(1)不会,当酚酞变色时的PH值条件下,HCl是与NaOh发生反应,不会与BaCO3作用。
(2)浅红色 无色
(3)不能。因滴定管下方刻度线距活塞处有一定空间,不能测出其所用的滴定液体积
(4)不能 偏高
19、(1)BDCEAF
(2)防止将标准液稀释
(3)偏大
(4)滴定管活塞;锥形瓶中溶液的颜色变化;锥形瓶中溶液的颜色由无色变浅红且保持30秒内不褪色。
(5)偏小 (6)偏大
20、NaOH+HCl====NaCl+H2O
Na2CO3+HCl====NaHCO3+NaCl
NaOH+HCl====NaCl+H2O
Na2CO3+2HCl====2NaCl+CO2↑+H2O;

 以下是某实验小组用CO2和NaOH溶液做喷泉实验的装置和测得的一组数据
以下是某实验小组用CO2和NaOH溶液做喷泉实验的装置和测得的一组数据| NaOH浓度(mol/L) | 0 | 0.4 | 0.5 | 0.8 | 1.0 | 1.4 | 1.6 | 1.8 |
| 现象 | 不能 形成 |
一段 液柱 |
形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 |
| 时间 | 6min | 1min | 35s | 10s | 6s | 6s | ||
| 烧瓶中水的体积(mL) | 7 | 41 | 71 | 125 | 240 | 240 |
C
C
A.CO2在水中的溶解度小,不宜用水直接吸收CO2来做喷泉实验
B.在一定的浓度范围内氢氧化钠溶液的浓度越大越易形成喷泉
C.NaOH浓度为1.6mol/L时,CO2还没有全部分被吸收
D.当氢氧化钠溶液的物质的量浓度为1.0mol/L时所得溶液不可能有氢氧化钠,烧瓶也没有充满.
(2012?吉林一模)氨氧化法制硝酸的主要反应是:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)
(1)①该反应的熵变△S
②升高温度,反应的平衡常数K值减小,则该反应的焓变△H
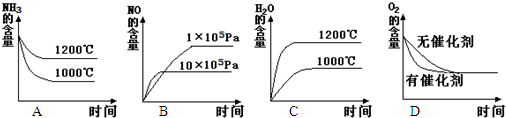
(2)若其他条件不变,下列关系图错误的是
(3)在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如下表:
①反应在第2min到第4min时,反应速率υ(O2)=
②反应在第2min时改变了条件,改变的条件可能是
查看习题详情和答案>>
(1)①该反应的熵变△S
>
>
0(填“>”、“<”或“=”).②升高温度,反应的平衡常数K值减小,则该反应的焓变△H
<
<
0(填“>”、“<”或“=”).(2)若其他条件不变,下列关系图错误的是
C
C
(选填序号).
(3)在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如下表:
| 时间/浓度/(mol?L-1) | c(NH3) | c(O2) | c(NO) | c(H2O) |
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第 2min | 3.2 | 4.5 4.5 |
0.8 | 1.2 |
| 第 4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第 6min | 2.0 | 3.0 | 2.0 | 3.0 |
0.75 mol?L-1?min-1
0.75 mol?L-1?min-1
;②反应在第2min时改变了条件,改变的条件可能是
升高温度(或使用催化剂)
升高温度(或使用催化剂)
.该条件下,反应的平衡常数K=3
3
(只写计算结果,不标单位).有A、B、C、D、E、F、G、H等常见物质,已知有如下图转化关系,其中B、C 为常见非金属单质;F为常见金属单质;B在C中燃烧时,火焰呈苍白色;A和D的焰色反应为黄色.G和D溶液混和,产生红褐色沉淀.

(1)反应(1)中若生成0.1mol B,则转移的电子的物质的量为
(2)图中所示的5个反应中属于氧化还原反应的有:
查看习题详情和答案>>

(1)反应(1)中若生成0.1mol B,则转移的电子的物质的量为
0.2mol
0.2mol
.写出C与F反应的化学方程式2Fe+3Cl2
2FeCl3
| ||
2Fe+3Cl2
2FeCl3
.(注明反应条件)
| ||
(2)图中所示的5个反应中属于氧化还原反应的有:
(1)、(2)、(3)、(4)、(5)
(1)、(2)、(3)、(4)、(5)
.(填写编号)