网址:http://m.1010jiajiao.com/timu_id_404607[举报]
(10分)实验室定量分析某样品中亚硫酸钠的一种方法是:
①在1.520g样品中加入碳酸氢钾溶液、0.13% I2的氯仿溶液,在分液漏斗中振荡15min。离子方程式为:SO32-+I2+2HCO3-=SO42-+2I-+2CO2↑+H2O
②取①中所得的水溶液,加入一定量乙酸、足量的饱和溴水溶液,充分振荡,其中碘离子被氧化成碘酸根离子,得到250mL溶液。
③在②所得溶液中取25mL,滴加甲酸,除去其中过量的Br2。
④将③所得溶液中加适量的醋酸钠,再加入足量的碘化钾溶液,振荡溶液。离子方程式为:6H++IO3-+5I-=3I2+3H2O
⑤用标准的硫代硫酸钠溶液滴定④中所得溶液,共消耗0.1120mol/L Na2S2O3 15.10mL。离子方程式为:I2+252O32-=2I-+S4O62-
回答下列问题:
(1)写出②、③三步操作中所发生反应的离子方程式。
(2)①中为什么要用0.13% I2的氯访溶液,而不直接用I2的水溶液?
(3)计算样品中亚硫酸钠的质量百分含量。
查看习题详情和答案>>①在1.520 g样品中加入碳酸氢钾溶液、0.13%I2的氯仿溶液,在分液漏斗中振荡15 min。离子方程式为:
![]() +I2+2
+I2+2![]() ====
====![]() +2I-+2CO2↑+H2O
+2I-+2CO2↑+H2O
②取①中所得的水溶液,加入一定量乙酸、足量的饱和溴水溶液,充分振荡,其中碘离子被氧化成碘酸根离子,得到250 mL溶液。
③在②所得溶液中取25 mL,滴加甲酸,除去其中过量的Br2。方程式为:Br2+HCOOH====2HBr+CO2↑
④将③所得溶液中加适量的醋酸钠,再加入足量的碘化钾溶液,振荡溶液。
⑤用标准的硫代硫酸钠溶液滴定④中所得溶液,共消耗0.112 0 mol·L-1 Na2S2O315.10 mL。
离子方程式为:I2+2![]() ====2I-+
====2I-+![]()
完成下列问题:
(1)写出②④两步操作中所发生反应的离子方程式。
(2)①中为什么要用0.13%I2的氯仿溶液,而不直接用I2的水溶液?
(3)计算样品中亚硫酸钠的质量百分含量。
查看习题详情和答案>> 常温下,向100mL 0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:
常温下,向100mL 0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:(1)由图中信息可知HA为
(2)常温下一定浓度的MA稀溶液的pH=a,则a
(3)请写出K点所对应的溶液中离子浓度的大小关系:
(4)K点对应的溶液中,c(M+)+c(MOH)
 Ⅰ常温下,向100mL0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:
Ⅰ常温下,向100mL0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:(1)由图中信息可知HA为
(2)N点对应溶液中离子浓度由大到的顺序为
(3)若K点所对应的溶液pH=10,则c(MOH)+c(OH-)-c(H+)=
Ⅱ复分解反应存在这样一个规律:一种较强酸与一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐,如:2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑
若换个角度看,它同时还揭示出另一条规律,即碱性较强的物质发生类似反应可以生成碱性较弱的物质.依照该规律回答下列问题:
(4)已知在常温下,测得浓度均为0.1mol/L的下列六种溶液的pH:
| 溶质 | CH3COONa | NaHCO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 10.3 | 11.1 | 11.3 |
(5)下列反应不能成立的是
A.CO2+H2O+2NaClO=Na2CO3+2HClO
B.CO2+H2O+NaClO=NaHCO3+HClO
C.CO2+H2O+C6H5ONa=NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
E.CH3COOH+NaCN=CH3COONa+HCN.
(18分) 三个课外实验小组用Na2SO3溶液、FeCl3溶液及其它试剂做了一系列实验:
第一组:烧瓶中盛装滴有酚酞的 Na2SO3溶液,并放置在盛有水的烧杯中,然后向烧杯中加入浓硫酸,实验过程中发现烧瓶中溶液红色_____(填“变深”、“变浅”或“不变”),下列有关叙述正确的是_________(填字母)。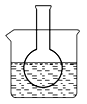
| A.溶液显浅红色是因为Na2SO3水解呈酸性 | B.水解反应为放热反应 |
| C.水解反应为吸热反应 | D.升高温度,Na2SO3水解程度增大 |
(1)用试管取适量Na2SO3溶液,加入BaCl2稀溶液,有白色沉淀生成,再加稀盐酸,沉淀全部溶解,然后再进行后续实验。该实验操作的目的是______________________。
(2)取5 mL FeCl3溶液于试管中,逐滴加入Na2SO3溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3溶液至过量,溶液颜色最终变为红褐色。这种红褐色液体是__________________。向红褐色液体中加足量盐酸,将所得溶液分成两份,其中一份加入KSCN溶液,溶液变成血红色,反应的离子方程式为________________________;另一份加入BaCl2稀溶液,产生少量白色沉淀,白色沉淀为________(填化学式)。
(3)由上述实验现象说明假设__________(填编号)是正确的。
第三组:用0.1000mol/L的酸性KMnO4溶液滴定未知浓度的Na2SO3溶液,用碱式滴定管量取25.00mL Na2SO3溶液于锥形瓶,用_____式滴定管盛装KMnO4溶液进行滴定,滴定终点颜色变化为:_____色变为_____色;重复三次实验,测得消耗的KMnO4溶液体积平均值为20.00mL,则Na2SO3的浓度为____________mol/L。 查看习题详情和答案>>