网址:http://m.1010jiajiao.com/timu_id_404110[举报]
元素周期表是学习化学的重要工具,它隐含许多信息和规律。下表所列是五种短周期元素的原子半径及主要化合价:
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
(1)在下表中标出上述五种元素在元素周期表中的对应位置(用元素符号)。
(2)在下表中标明通常寻找催化剂材料的区域(用斜线阴影)。
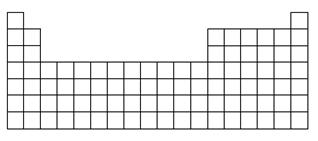
(3)A、B、E三种元素各自形成简单离子,其中半径最大的为________(填离子符号)。
(4)证明B元素的单质与A元素的单质在化学性质上有明显不同的离子方程式为:________________________。
(5)周期表中有些处于对角(左上→右下)位置的元素,它们的单质及其化合物的性质存在“对角线相似”的现象,请写出D的氧化物与强碱溶液反应的离子方程式:________________________。 查看习题详情和答案>>
请回答下列问题:
(1)CO可以和很多过渡金属形成配合物,CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO分子里的共价键的类型按原子轨道的重叠方向分有
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的.但
31 |
30 |
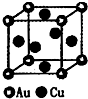
(3)如图是金与铜形成的金属互化物合金,它的化学式可表示为
(4)已知Ti3+可形成配位数为6的配合物;现有含钛的两种颜色的晶体,一种为紫色,另一为绿色,但相关实验证明,两种晶体 的组成皆为TiCl3?6H2O.为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种晶体样品配成待测溶液;
b.分别向待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水 溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的
| 2 |
| 3 |
则绿色晶体配合物的化学式为
(5)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化.有关甲醛、苯、二氧化碳及水说法正确的是
A.苯与B3N3H6互为等电子体
B.甲醛、苯和二氧化碳中碳原子均采用Sp2杂化
C.苯、二氧化碳是非极性分子,水和甲醛是极性分子
D.水的沸点比甲酸高得多,是因为水分子间形成了氢键.
现有A、B、C、D、E、F六种中学常见的元素,其原子序数依次增大。①D的一种含氧酸根离子与H+结合生成D的单质、D的氧化物和水;该D的氧化物通入品红溶液,溶液褪色,加热溶液又变红色;②在短周期元素中,只有C的氧化物和烧碱反应生成的溶液与过量盐酸混合产生白色沉淀;③A与D的原子最外层电子数相同;④B的单质既能与盐酸反应,又能与氢氧化钠溶液反应;⑤E有多种含氧酸,其氧化性与“同元素价态越高,其氧化性越强”一般规律相悖,它是生活调味品和农药的组成元素 ⑥E单质+F单质![]() 红棕色烟,D单质+F单质
红棕色烟,D单质+F单质![]() 黑色固体,A单质+F单质
黑色固体,A单质+F单质![]() 黑色固体。F的最高价钾盐是一种绿色环保型净水剂。
黑色固体。F的最高价钾盐是一种绿色环保型净水剂。
根据上述信息,回答下列问题:
(1)A的简单离子结构示意图为 ;具有强氧化性的E的含氧酸结构式为 ;
(2)向一定量的烧碱溶液中缓慢通入DA2,得到中性溶液,其溶质的化学式为 ;
(3)下列“根据”能证明B、F单质活泼性强弱的是 ;
a.根据它们分别与D单质反应产物的价态
b.根据它们最高价氧化物的水化物在氢氧化钠溶液中溶解情况
c.根据它们分别与盐酸反应产生气泡快慢
d.根据它们在空气中稳定性
(4)工业上冶炼C单质的化学方程式为 。
(5)CE4在湿空气中产生大量白雾,可以用于海战。写出发生的化学方程式: 。
(6)C、D、E最高价氧化物对应的水化物酸性强弱顺序为(用化学式表示): 。
查看习题详情和答案>> 红棕色烟,D单质+F单质
红棕色烟,D单质+F单质 黑色固体,A单质+F单质
黑色固体,A单质+F单质 黑色固体。F的最高价钾盐是一种绿色环保型净水剂。
黑色固体。F的最高价钾盐是一种绿色环保型净水剂。根据上述信息,回答下列问题:
(1)A的简单离子结构示意图为 ;具有强氧化性的E的含氧酸结构式为 ;
(2)向一定量的烧碱溶液中缓慢通入DA2,得到中性溶液,其溶质的化学式为 ;
(3)下列“根据”能证明B、F单质活泼性强弱的是 ;
a.根据它们分别与D单质反应产物的价态
b.根据它们最高价氧化物的水化物在氢氧化钠溶液中溶解情况
c.根据它们分别与盐酸反应产生气泡快慢
d.根据它们在空气中稳定性
(4)工业上冶炼C单质的化学方程式为 。
(5)CE4在湿空气中产生大量白雾,可以用于海战。写出发生的化学方程式: 。
(6)C、D、E最高价氧化物对应的水化物酸性强弱顺序为(用化学式表示): 。
元素周期表是学习化学的重要工具,它隐含许多信息和规律。下表所列是五种短周期元素的原子半径及主要化合价:
元素代号ABCDE
原子半径/nm0.160.1430.1020.0890.074
主要化合价+2+3+6,-2+2-2
(1)在下表中标出上述五种元素在元素周期表中的对应位置(用元素符号)。
(2)在下表中标明通常寻找催化剂材料的区域(用斜线阴影)。

(3)A、B、E三种元素各自形成简单离子,其中半径最大的为________(填离子符号)。
(4)证明B元素的单质与A元素的单质在化学性质上有明显不同的离子方程式为:________________________。
(5)周期表中有些处于对角(左上→右下)位置的元素,它们的单质及其化合物的性质存在“对角线相似”的现象,请写出D的氧化物与强碱溶液反应的离子方程式:________________________。
查看习题详情和答案>>