摘要:⑶每一周期排布元素的种类满足以下规律:设n为周期序数.则奇数周期中为种.偶数周期中为种. ⑷同主族相邻元素的原子序数差别有以下二种情况:①第ⅠA.ⅡA族.上一周期元素的原子序数+该周期元素的数目=下一同期元素的原子序数,②第ⅣA-ⅦA族.上一周期元素的原子序数+下一周期元素的数目=下一周期元素的原子序数. ⑸设主族元素族序数为a.周期数为b.则有:①a/b<1时.为金属元素.其最高氧化物为碱性氧化物.最高氧化物对应的水化物为碱,②a/b=1时.为两性元素.其最高氧化物为两性氧化物.最高氧化物对应的水化物为两性氢氧化物,③a/b>1时.为非金属元素.其最高氧化物为酸性氧化物.最高氧化物对应的水化物为酸.无论是同周期还是同主族元素中.a/b的值越小.元素的金属性越强.其最高氧化物对应水化物的碱性就越强,反之.a/b的值越大.元素的非金属性越强.其最高氧化物对应水化物的酸性就越强. ⑹元素周期表中除第Ⅷ族元素以外.原子序数为奇数的元素.元素所在族的序数及主要化合价也为奇数. ⑺元素周期表中金属和非金属之间有一分界线.分界线右上方的元素为非金属元素.分界线左下方的元素为金属元素.分界线两边的元素一般既有金属性.也有非金属性.
网址:http://m.1010jiajiao.com/timu_id_403985[举报]
(二)1、 C 2、AD 3、C 4、BC
5、⑴ Ar 、K 、 F 、Br 、M
⑵ H2O HCl PH3 、PH3 ⑶ Cl
6 ⑴ 79 ⑵ 略 ⑶K 、Mg 、Cl 、Se 、C
⑷HClO4、 H2SeO4 、H2CO3 、 Mg(OH)2、 KOH
7 H 、O 、Na 、S 、极性 、共价、 略、NaHSO4+NaHSO3=Na2SO4+H2O+SO2 ↑
8 ⑴Ca 、C 、S 、 ⑵CaC2+2H2O → Ca(OH)2+C2H2↑
⑶CaC2、CS2
9⑴ ⑵> ⑶NH4++H2O
⑵> ⑶NH4++H2O
 NH3?H2O+H+
NH3?H2O+H+
(12分)图表法、图象法是常用的科学研究方法。
下表列出前20号元素中的某些元素性质的一些数据:
| 元素 性质 | A | B[ | C | D | E | F | G | H | I | J |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | — | -2 | — | -4 | -3 | -1 | — | -3 | -4 |
(1)已知H为Na元素,则以上10种元素中第一电离能最小的是: (填编号)。比元素B原子序数大10的元素其基态原子的核外电子排布是
 。
。(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是 (写分子式,写出一种即可),元素G、I分别和J形成的两种化合物的晶体类型分别是 。
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。其一分子中共形
成
 个σ键, 个π键。
个σ键, 个π键。(4)短周期某主族元素K的电离能情况如图(A)所示。
则K元素位于周期表的第 族。

图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第 族元素氢化物的沸点的变化规律。
不同同学对某主族元素的氢化物的沸点的变化趋势画出了两条折线—折线a和折线b,你认为正确的是 ,理由是 查看习题详情和答案>>
(12分)图表法、图象法是常用的科学研究方法。
下表列出前20号元素中的某些元素性质的一些数据:
试回答下列问题:
(1)已知H为Na元素,则以上10种元素中第一电离能最小的是: (填编号)。比元素B原子序数大10的元素其基态原子的核外电子排布是 。
。
(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是 (写分子式,写出一种即可),元素G、I分别和J形成的两种化合物的晶体类型分别是 。
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。其一分子中共形
成 个σ键, 个π键。
个σ键, 个π键。
(4)短周期某主族元素K的电离能情况如图(A)所示。
则K元素位于周期表的第 族。
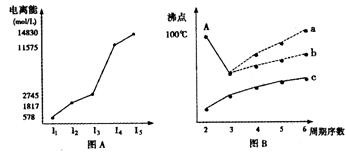
图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第 族元素氢化物的沸点的变化规律。
不同同学对某主族元素的氢化物的沸点的变化趋势画出了两条折线—折线a和折线b,你认为正确的是 ,理由是
下表列出前20号元素中的某些元素性质的一些数据:
| 元素 性质 | A | B[ | C | D | E | F | G | H | I | J |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | — | -2 | — | -4 | -3 | -1 | — | -3 | -4 |
(1)已知H为Na元素,则以上10种元素中第一电离能最小的是: (填编号)。比元素B原子序数大10的元素其基态原子的核外电子排布是
 。
。(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是 (写分子式,写出一种即可),元素G、I分别和J形成的两种化合物的晶体类型分别是 。
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。其一分子中共形
成
 个σ键, 个π键。
个σ键, 个π键。(4)短周期某主族元素K的电离能情况如图(A)所示。
则K元素位于周期表的第 族。

图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第 族元素氢化物的沸点的变化规律。
不同同学对某主族元素的氢化物的沸点的变化趋势画出了两条折线—折线a和折线b,你认为正确的是 ,理由是
[化学──选修物质结构与性质]
图表法、图象法是常用的科学研究方法.下表列出前20号元素中的某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中第一电离能最小的是: (填编号).比元素B原子序数大10的元素在元素周期表中的位置: 周期, 族,其基态原子的核外电子排布是 .
(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是 (写分子式,写出两种即可),元素G、I分别和J形成的两种化合物的晶体类型分别是 .
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子.其分子中共形成 个σ键, 个π键.
(4)短周期某主族元素K的电离能情况如图(A)所示.则K元素位于周期表的第 族.

图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第 族元素氢化物的沸点的变化规律.不同同学对某主族元素的氢化物的沸点的变化趋势画出了两条折线-折线a和折线b,你认为正确的是 ,理由是 .
查看习题详情和答案>>
图表法、图象法是常用的科学研究方法.下表列出前20号元素中的某些元素性质的一些数据:
| 元素 性质 |
A | B | C | D | E | F | G | H | I | J |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
(1)以上10种元素中第一电离能最小的是:
(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子.其分子中共形成
(4)短周期某主族元素K的电离能情况如图(A)所示.则K元素位于周期表的第

图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第