网址:http://m.1010jiajiao.com/timu_id_3917[举报]
将4 mol SO3气体和4 mol NO置于2 L容器中,在一定条件下发生如下可逆反应(不考虑NO2和N2O4之间的相互转化):
2SO3(g)![]() 2SO2+O2;2NO+O2
2SO2+O2;2NO+O2![]() 2NO2。
2NO2。
(1)当上述系统达到平衡时,O2和NO2的物质的量分别为n(O2)=0.1 mol、n(NO2)=3.6 mol,则此时SO3气体的物质的量是多少?(写出计算过程)
(2)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少需要知道两种气体的平衡浓度,但这两种气体不能同时是SO3和______,或NO和________(填分子式)。
(3)若在另外一个2 L的容器中只发生反应2NO+O2![]() 2NO2,其中NO、O2、NO2的起始浓度依次是0.2 mol?L-1、0.1 mol?L-1、0.2 mol?L-1,当反应达到平衡时,各物质的浓度可能是________(选填字母代号)。
2NO2,其中NO、O2、NO2的起始浓度依次是0.2 mol?L-1、0.1 mol?L-1、0.2 mol?L-1,当反应达到平衡时,各物质的浓度可能是________(选填字母代号)。
A.c(NO)=0.35 mol?L-1或c(NO)=0.09 mol?L-1
B.c(NO2)=0.4 mol?L-1
C.c(NO2)=0.35 mol?L-1
D.c(O2)=0.2 mol?L-1或c(NO)=0.4 mol?L-1
查看习题详情和答案>>某化学课外活动小组在实验室做了如下一系列实验:
(1)该小组设计了如图所示的一套气体发生、收集和尾气吸收装置以探究装置的多功能
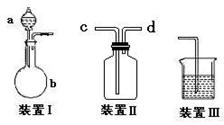 性。
性。
① 甲同学认为装置Ⅰ可作为实验室制氧气的快速发生器,则装置Ⅰ的a仪器中可加
入 或 ,装置Ⅱ从 管口进气即可作为O2的收集装置。
 ② 乙同学认为利用装置Ⅱ,可收集NO,试简述操作方法:
② 乙同学认为利用装置Ⅱ,可收集NO,试简述操作方法:
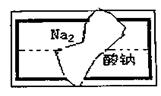
(2)小组在整理实验室的化学试剂时,发现一盛有
无色溶液的试剂瓶。标签破损(如图),请你根
据已掌握的知识,对该试剂可能是什么物质的溶
液作出二种猜想,并设计实验验证,写出任一种
的实验操作、现象和结论。
| 猜想物质的化学式 | 检验所需要的试剂 | 操作、现象和结论 | |
| ① | |||
| ② |
|
(3)该小组从ZnSO4、FeCl3的混合溶液中制取ZnSO4?7H2O过程如下:
a.在混合液中加入6 mol?L―1NaOH溶液,至pH=8为止。
b.过滤后得到沉淀,用蒸馏水多次洗涤沉淀。
c.向洗涤后的沉淀中加入2 mol?L―1的硫酸,保持溶液的pH在4~6,加热煮沸,
趁热过滤,滤液即为ZnSO4溶液
d.滤液中注入2 mol?L―1的硫酸,使其pH保持为2……
已知部分阳离子以氢氧化物的形式开始沉淀至完全沉淀时溶液的pH见下表,回答下列
问题:
| 沉淀物 | Fe(OH)3 | Zn(OH)2 |
| pH | 1.5~3.2 | 6.4~8.0 |
① 步骤a中用pH试纸控制溶液pH=8,使用pH试纸的操作是 ;步骤b中如何
检验沉淀已经洗涤干净? 。
② 要制得ZnSO4?7H2O的步骤d还缺少的操作是 ,所用的主要硅酸盐
仪器是 。
查看习题详情和答案>>