网址:http://m.1010jiajiao.com/timu_id_383684[举报]
一、选择题(本题包括
1.D 2.C 3.C 4.D 5.C 6.C 7.D 8.D 9.C l0.C
l1.B 12.C 13.C 14.C 15.D 16.C l 7.B l 8.D 19.B 20.A
二、本题包括1小题,共12分。
21.(12分)
(1)B中装无水硫酸铜,检验水蒸气;C中装澄清的石灰水,检验二氧化碳;(每空1分)
(2)验纯后点燃E处的气体,火焰呈蓝色。(2分,不答“验纯”扣1分)
(3)点燃前应验纯;CO有毒,实验要通风;加热时要均匀受热等。(2分)
(4)挥发出来的草酸蒸气与石灰水反应生成了草酸钙沉淀,会干扰CO2的检验(2分)
在装置B和C装置间增加一个装有水(或烧碱溶液)的洗气装置(2分)
三、本题包括3小题,共38分。
22.(每空2分,共12分)
(2)>
(3)A1 +3NH3?H2O=Al(OH)3↓ +3NH
+3NH3?H2O=Al(OH)3↓ +3NH
(4)NH4Al(SO4)2
(5)336
23.(每空2分,共l 2分)
(1)A:Si B:Mg
(2)抑制氯化镁水解
(3)①Si+2NaOH+H2O=Na2SiO3+2H2↑
③ Mg2Si+4HCl=SiH4↑+2MgCl2
24.(每空2分,共14分)
(1)
(2)O2+2CO2+4e =2CO
=2CO
(3)CO2 负极反应产物
②
③ 560
四、本题包括l小题,共l0分。
25.(1)Fe+H2SO4=FeSO4+H2↑(2分)
FeSO4+(NH4)2SO4+6H2O=(NH4)2Fe(SO4)2?6H2O(2分)
(2)解:设生成(NH4)2Fe(SO4)2?6H2O的物质的量为x mol。由上述方程式知:
H2SO4~FeSO4~(NH4)2Fe(SO4)2?6H2 O
1 mol l mol
15×3×10 mol x
mol
mol x
mol
x=0.045
生成(NH4)2Fe(SO4)2?6H2O的质量为:0.045 mol×
(3)① 5、1、8、1、5、4 H2O(2分)
② 83.33%。(2分)
(10分)下图表示800℃时,A、B、C三种气体物质的浓度随时间变化的情况,t表示时间。试回答: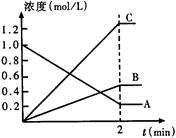
(1)该反应的反应物是 。
(2)该反应的化学方程式为 。
(3)达到平衡状态的所需时间是2min,A物质的平均反应速率为
(4)其他条件不变,压缩容器容积,平衡______________(填向正或逆方向或不)移动;若正方向吸热,则升高温度,平衡平衡___________(填向正或逆方向或不)移动。
(10分)下图表示800℃时,A、B、C三种气体物质的浓度随时间变化的情况,t表示时间。试回答:

(1)该反应的反应物是 。
(2)该反应的化学方程式为 。
(3)达到平衡状态的所需时间是2min,A物质的平均反应速率为
(4)其他条件不变,压缩容器容积,平衡______________(填向正或逆方向或不)移动;若正方向吸热,则升高温度,平衡平衡___________(填向正或逆方向或不)移动。
查看习题详情和答案>>
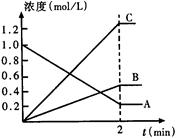
(1)该反应的反应物是 。
(2)该反应的化学方程式为 。
(3)达到平衡状态的所需时间是2min,A物质的平均反应速率为
(4)其他条件不变,压缩容器容积,平衡______________(填向正或逆方向或不)移动;若正方向吸热,则升高温度,平衡平衡___________(填向正或逆方向或不)移动。
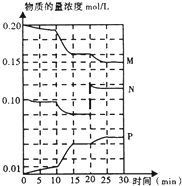 如图所示是某反应体系中的三种气态物质M、N、P的物质的量浓度随时间的变化情况,则下列判断不正确的是( )
如图所示是某反应体系中的三种气态物质M、N、P的物质的量浓度随时间的变化情况,则下列判断不正确的是( )| A、该反应的化学方程式可表达为2M+N?2P | B、当反应时间为20 min时,曲线开始发生变化的原因可能是由于增大压强引起的 | C、反应在10 min时,若曲线的变化是由于升温造成的(其他条件不变),则该反应的正反应一定为吸热反应 | D、在反应时间段10 min~15 min内,物质P的反应速率约为0.0001 mol/(L?s) |
(I)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
(1)目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作冷剂已成为一种趋势,这一做法对环境的积极意义在于 。
(2)将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
以上反应中,最节能的是 ,原子利用率最高的是 。
(3)为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:
在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-49.0kJ/mol
测得CO2和CH3OH(g)的浓度随时间变化如图所示。

①从反应开始到平衡,氢气的平均反应速率v(H2)= 。
②该反应的平衡常数表达式为 ,升高温度,平衡常数的数值将
(填“增大”、“减小”或“不变”)。
③下列措施中能使n(CH3OH)/n(CO2)增大的是 .
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1molCO2和3molH2
(II)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N2(g)+3H2(g) 2NH3(g) △H=-93.4kJ/mol
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如下图所示。

图t1时引起平衡移动的条件可能是 。
其中表示平衡混合物中NH3含量最高的一段时间是 。
②温度为T°C时,将3amolH2和amolN2放入右图所示的密闭容器中,如果活塞能左右自由移动,充分反应后测得N2的转化率为50%。如果在相同温度下将3amolH2、amolN2和2amolNH3气体放入该容器中,平衡时H2的体积分数为 。
查看习题详情和答案>>



