摘要:22.
网址:http://m.1010jiajiao.com/timu_id_383163[举报]
 二氧化硫和氮氧化物是常用的化工原料,也会给大气带来严重污染,综合治理其污染是环境化学当前的重要研究内容之一.
二氧化硫和氮氧化物是常用的化工原料,也会给大气带来严重污染,综合治理其污染是环境化学当前的重要研究内容之一.(1)汽车尾气中主要含有CO、NO2、SO2、CO2气体,其中
NO2、SO2
NO2、SO2
能导致酸雨的形成;目前采用的是在汽车排气装置中安装一个净化器,可以有效的将尾气中的有害气体转化.如:CO(g)+NO2(g)═NO(g)+CO2(g)△H=-akJ?mol-1(a>0)
2CO(g)+2NO(g)═N2(g)+2CO2(g)△H=-bkJ?mol-1(b>0)
据此回答:若用标准状况下3.36升CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为
0.3
0.3
mol,放出的热量为| 3(2a+b) |
| 80 |
| 3(2a+b) |
| 80 |
(2)在火力发电厂产生的废气中含有SO2、N2、CO等气体,为除去SO2,常用Ca(OH)2悬浊液洗涤废气,为了废物利用,再通入空气使反应产物转化为石膏(CaSO4?2H2O).写出有关的化学反应方程式
SO2+Ca(OH)2=CaSO3↓+H2O、2CaSO3+O2+4H2O=2CaSO4?2H2O
SO2+Ca(OH)2=CaSO3↓+H2O、2CaSO3+O2+4H2O=2CaSO4?2H2O
.(3)硫酸工业生产中,SO2催化氧化生成SO3:
2SO2(g)+O2(g)
| 催化剂 |
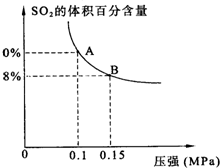
某温度下达到平衡时,SO2的体积百分含量与体系的总压强的关系如图所示:
据此图回答下列问题:
①平衡状态由A变到B时,反应体系
释放
释放
(填“吸收”或“释放”)能量.②将5molSO2和7molO2通入10L密闭容器中,平衡时体系的总压强为0.1MPa.该反应在该温度下的平衡常数等于
32
32
. 二甲醚(CH3OCH3)是一种重要的清洁能源,工业上制二甲醚是在一定的温度(230~290℃)和催化剂条件下进行的,反应中发生了下列一些反应:CO(g)+2H2(g)
二甲醚(CH3OCH3)是一种重要的清洁能源,工业上制二甲醚是在一定的温度(230~290℃)和催化剂条件下进行的,反应中发生了下列一些反应:CO(g)+2H2(g)
|
|
|
(1)反应器中的总反应可表示为3CO(g)+3H2(g)
|
-246.1kJ/mol
-246.1kJ/mol
.(2)二甲醚燃料电池的工作原理如图所示,请回答下列问题:
①B电极上的电极反应式是
CH3OCH3-12e-+3H2O═2CO2+12H+
CH3OCH3-12e-+3H2O═2CO2+12H+
.②若燃料电池中通入二甲醚(沸点为-24.9℃)的速率为1.12L/h(标准状况),以该燃料电池作为电源电解2mol?L-1CuSO4溶液500mL,则通电0.5h后理论上在阴极可析出的金属铜为
7.2
7.2
g.(假设整个过程中,能量利用率为75%)二氧化碳碳捕获与封存技术(CCS)可以减少化石燃料燃烧以及其他工业用途的二氧化碳排放量,从而有助于减少温室气体的排放.该技术引起了各国的普遍重视.
Ⅰ.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3molH2,一定条件下发生反应:
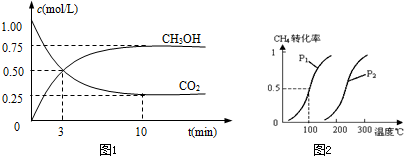
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol测得CO2和CH3OH(g)的浓度随时间变化如图1所示.
①从反应开始到平衡,氢气的平均反应速率v(H2)=
②下列措施中能使n(CH3OH)/n(CO2)增大的是
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3molH2.
Ⅱ.工业上也可以通过下列反应①和②,用CH4和H2O为原料来制备甲醇.
①CH4(g)+H2O(g)?CO(g)+3H2(g)△H1;②CO(g)+2H2(g)?CH3OH(g)△H2
将0.20mol CH4和0.30molH2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如图2.
(1)温度不变,缩小体积,增大压强,①的反应速率
(2)反应①的△H1
,压强为P1,100℃时的平衡常数值是
查看习题详情和答案>>
Ⅰ.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3molH2,一定条件下发生反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol测得CO2和CH3OH(g)的浓度随时间变化如图1所示.

①从反应开始到平衡,氢气的平均反应速率v(H2)=
0.225
0.225
mol/(L?min).②下列措施中能使n(CH3OH)/n(CO2)增大的是
CD
CD
.A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3molH2.
Ⅱ.工业上也可以通过下列反应①和②,用CH4和H2O为原料来制备甲醇.
①CH4(g)+H2O(g)?CO(g)+3H2(g)△H1;②CO(g)+2H2(g)?CH3OH(g)△H2
将0.20mol CH4和0.30molH2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如图2.
(1)温度不变,缩小体积,增大压强,①的反应速率
增大
增大
(填“增大”、“减小”或“不变”),平衡向逆反应
逆反应
方向移动.(2)反应①的△H1
>
>
0(填“<”、“=”或“>”),其平衡常数表达式为K=| c(CO)?c3(H2) |
| c(CH4)?c(H2O) |
| c(CO)?c3(H2) |
| c(CH4)?c(H2O) |
1.35×10-3
1.35×10-3
.