摘要:c.应用余热蒸干溶液d.应蒸发至有较多晶体析出时为止(2)由MgCl2溶液得到MgCl2?6H2O也需要蒸发.根据溶解度曲线.蒸发的目的是 .a.得到热饱和溶液 b.析出晶体(3)若在空气中加热MgCl2?6H2O.生成的是Mg(OH)Cl.写出反应的化学方程式: ,用电解法制取金属镁时.需要无水氯化镁.在干燥的HCl气流中加热MgCl2?6H2O时.能得到无水MgCl2.其原因是 .(4)该流程产生的物质中.除Ca2+能被海洋生物利用外.还需综合利用的物质是 .
网址:http://m.1010jiajiao.com/timu_id_356296[举报]
(16分)某小组同学利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,倒入大试管中迅速振荡混合均匀,再加入硫酸,开始计时,通过测定混合溶液褪色所需时间来判断反应的快慢(已知反应方程式为:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O)。该小组设计了如下方案。
| 编号 | H2C2O4溶液 | KMnO4溶液 | 硫酸溶液 | 温度/℃ | ||
| | 浓度 (mol/L) | 体积 (mL) | 浓度 (mol/L) | 体积 (mL) | | |
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 50 |
(2)该小组同学由此实验发现反应进行一些时间后,有一时间段反应速率不断加快。同学们分析除了反应放热使体系温度升高外,可能还有其它原因,他们联想到教材上的科学探究实验,推断出反应混合溶液中的__________(填化学式)也加速了此反应的进行。
(3)上述实验①中充分反应后H2C2O4过量,假设理论上能通过用酸性KMnO4溶液滴定的方法来测定反应混合液中过量的H2C2O4,请回答下列问题:
①取用反应混合液的滴定管用__________滴定管(填“酸式”或“碱式”,下同),盛装KMnO4溶液的滴定管用__________滴定管。
②下列操作中可能使测出的H2C2O4剩余量比理论值偏低的是__________。
A.读取酸性KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
B.滴定前盛放反应混合液的锥形瓶用蒸馏水洗净但没有干燥
C.盛装KMnO4溶液的滴定管滴定前有气泡,滴定后气泡消失
D.盛装KMnO4溶液的滴定管未润洗就直接注入酸性KMnO4溶液
③此滴定实验是否需要滴加指示剂________(填“是”或“否”);怎么确定此滴定的终点:_________。 查看习题详情和答案>>
 (1)①要配制500mL 0.200mol?L-1的H2SO4溶液,需要的仪器除量筒、烧杯外还有
(1)①要配制500mL 0.200mol?L-1的H2SO4溶液,需要的仪器除量筒、烧杯外还有玻璃棒、500mL容量瓶、胶头滴管
玻璃棒、500mL容量瓶、胶头滴管
.需要98%的浓硫酸(密度1.84g?cm-3)
5.4
5.4
mL.②下列操作会使所配的溶液浓度偏小的是
B
B
(填代号).A.用量筒取一定体积的98%的浓硫酸,稀释后未经冷却即转入容量瓶内
B.稀释硫酸所用的小烧杯未洗涤
C.定容时俯视观察液面
D.用蒸馏水洗涤后的容量瓶未干燥
E.定容摇匀后,倒入干燥的试剂瓶中储存时,有少量溶液溅出瓶外
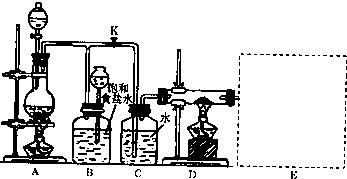
(2)如图是一个实验室制到氯气并以氯气为原料进行特定反应的装置
①A是氯气发生装置,其中发生的离子方程式为
MnO2+4H++2Cl-═Mn2++Cl2↑+2H2O
MnO2+4H++2Cl-═Mn2++Cl2↑+2H2O
.②实验开始时,先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处酒精灯,Cl2通过C瓶后再进入D.D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为CO2和HCl.则该反应的化学方程式为
2Cl2+2H2O+C
CO2+4HCl
| ||
2Cl2+2H2O+C
CO2+4HCl
.
| ||
③该装置图尚未画完,请在E处补充完整,并注明试剂名称.
④D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,则B的作用是
储存氯气
储存氯气
.⑤若实验中使用12mol?L-1的 浓盐酸10mL与足量的MnO2反应,则生成的Cl2的物质的量总是小于0.03mol,试分析可能存在的原因是
随反应进行HCl消耗、且HCl的挥发,盐酸变稀与MnO2不反应
随反应进行HCl消耗、且HCl的挥发,盐酸变稀与MnO2不反应
.下列实验操作中错误的是
A.蒸发操作时,使溶液中的水大部分蒸发时,就停止加热利用余热蒸干
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
查看习题详情和答案>>
 (1)①要配制500mL 0.200mol?L-1的H2SO4溶液,需要的仪器除量筒、烧杯外还有______.
(1)①要配制500mL 0.200mol?L-1的H2SO4溶液,需要的仪器除量筒、烧杯外还有______.
需要98%的浓硫酸(密度1.84g?cm-3)______mL.
②下列操作会使所配的溶液浓度偏小的是______(填代号).
A.用量筒取一定体积的98%的浓硫酸,稀释后未经冷却即转入容量瓶内
B.稀释硫酸所用的小烧杯未洗涤
C.定容时俯视观察液面
D.用蒸馏水洗涤后的容量瓶未干燥
E.定容摇匀后,倒入干燥的试剂瓶中储存时,有少量溶液溅出瓶外
(2)如图是一个实验室制到氯气并以氯气为原料进行特定反应的装置
①A是氯气发生装置,其中发生的离子方程式为______.
②实验开始时,先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处酒精灯,Cl2通过C瓶后再进入D.D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为CO2和HCl.则该反应的化学方程式为______.
③该装置图尚未画完,请在E处补充完整,并注明试剂名称.
④D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,则B的作用是______.
⑤若实验中使用12mol?L-1的 浓盐酸10mL与足量的MnO2反应,则生成的Cl2的物质的量总是小于0.03mol,试分析可能存在的原因是______.
查看习题详情和答案>>
下列实验操作中错误的是
| A.蒸发操作时,使溶液中的水大部分蒸发时,就停止加热利用余热蒸干 |
| B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |