网址:http://m.1010jiajiao.com/timu_id_322945[举报]
第Ⅰ卷(选择题)
一、选择题(每题6分,共78分)
1.C 2.A 3.D 4.B 5.D
6.C 7.D 8.C 9.D 10.B 11.B 12.C 13.A
二、选择题(本题包括8小题。在每小题给出的四个选项中,有的只有一个选项正确,有的有多个选项正确,全部选对的得6分,选对但不全的得3分,有选错的得0分)
14.D 15.C 16.A 17.D 18.B 19.AD 20.C 21.AC
第Ⅱ卷(非选择题)
三、非选择题(本题共10小题)
22.⑴球1和球2的质量m1和m2,立柱的高h,桌面离地面的高H (3分)
m1 =m1
=m1 +m
+m (3分)
(3分)
⑵①电路图如图。(6分) ②实物图略 (5分)

23.解:⑴依题意得甲乙两同学的奔跑加速度相同,设为a,达到的最大速度为vm,由 得:
得: ① (2分)
① (2分)
设乙全力奔跑的距离为s1时,速度达到奔跑最大速度的80%,有:
 ② (2分)
② (2分)
联立①②解得:s1=
⑵设乙应在距离甲为s0时起跑,从此时开始到接棒所用的时间为t,在t内甲、乙的位移关系是: ④ (4分)
④ (4分)
而: ⑤ (1分)
⑤ (1分)  ⑥ (1分)
⑥ (1分)
 ⑦ (1分)
⑦ (1分)
联立③④⑤⑥⑦解得: m (2分)
m (2分)
24.解:⑴子弹进入小车的过程中,子弹与小车组成的系统动量守恒,由动量守恒定律得:
m1v0=(m2+m1)v1 ① (3分)
由三物体组成的系统动量守恒,由动量守恒定律得:
(m2+m1)v1=(m2+m1+m3)v2 ② (3分)
设小车最小长度为L,三物体相对静止后,对系统利用能量守恒定律得:
 (m2+m1)v12-
(m2+m1)v12- (m2+m1+m3)v22=μm3gL ③ (6分)
(m2+m1+m3)v22=μm3gL ③ (6分)
联立以上方程解得:L=
车与物体的共同速度为:v2= m/s) (2分)
m/s) (2分)
⑵以m3为研究对象,利用动量定理可得:μm3gt=m3v2 ④(4分)
解得:t=0.52s(或 s)
(2分)
s)
(2分)
25.解:⑴正电荷 (4分)
⑵依题意可知小球在BC间做匀速直线运动。
 在C点的速度为:
在C点的速度为: (2分)
(2分)
在BC段其受力如图所示,设重力和电场力合
力为F。
F=qvCB (1分)
又 F=mg/cos37°=5N(1分)
解得: (1分)
(1分)
在D处由牛顿第二定律可得:
 (2分)
(2分)
将 代入上式并化简得:
代入上式并化简得:
 解得
解得  (1分)
(1分)
小球离开D点后作类平抛运动,其加速度为:a=F/m (1分)
由 得:
得: (1分)
(1分)
 (1分)
(1分)
⑶CD段克服摩擦力做功Wf
由动能定理可得: (3分)
(3分)
解得:Wf=27.6J (2分)
26.(14分)
⑴C:
 (2分) B:第三周期,第IIIA族(2分)
(2分) B:第三周期,第IIIA族(2分)
⑵
 (2分)
(2分)
⑶2Al+2OH-+2H2O=2AlO2-+3H2↑(2分)
⑷Fe-2e-=Fe2+(2分),4Fe2++10H2O+O2=4Fe(OH)3↓+8H+(2分)
⑸FeO(2分)
27.(16分)
⑴(NH4)2SO3(1分) 
 (1分)
(1分)
⑵(NH4)2SO3+2NaOH
 Na2SO3+2NH3↑+2H2O(3分)
Na2SO3+2NH3↑+2H2O(3分)
Na2SO3+H2SO4=Na2SO4+SO2↑+H2O(3分)
⑶c(NH4+)>c(NO3-)>c(OH-)>c(H+)(2分)
⑷①90%(3分)
②0.4+0.1w(3分)
28.(17分)
⑴①d步骤中在点燃H2前没有先验纯。(2分)
②可能的原因是:一是分液漏斗的活塞没有打开,二是量气管中液面高于分液漏斗中液面。(4分)
⑵①A、B、E(3分,错选一个倒扣1分)
②A、B、C、D(3分,错选一个倒扣1分)
⑶①保持装置A和装置B液面相平(2分)
②CH2OHCH2OH(3分)
29.(13分)
⑴
 (3分)
(3分)
⑵不合理,因为酚羟基更容易被氧化(3分)
⑶
 (3分)
(3分)
 ⑷(各2分,共4分)
⑷(各2分,共4分)
30.(22分)
Ⅰ.(12分,每空2分)
⑴通入空气 培养液、老叶(缺一不得分) K
⑵下降 上升
⑶C3(或三碳化合物)
Ⅱ.(10分)
⑴抗原 体液 免疫细胞(说明:答体液免疫、细胞免疫亦可,顺序不能颠倒)(每空1分)
⑵病毒是专性活细胞内寄生(或病毒不能独立繁殖)(1分)
⑶①A:蛋白质与双缩脲试剂反应显紫色(或蛋白质液在碱性条件下与Cu2+反应显紫色)(2分)
B:DNA液与二苯胺试剂共热显蓝色(2分)
②酶处理(或水解法)(2分)
31.(每空2分,共20分)
⑴4、aaBb、矮生红果∶矮生黄果=3∶1
⑵13或11(只答13或只答11不得分) 正常或矮生(只答正常或只答矮生不得分)
⑶Y Y突变体的蛋白质氨基酸的改变比X突变体可能更多(X突变的蛋白质可能只有一个氨基酸发生变化,Y突变的蛋白质氨基酸序列可能从第一个氨基酸后都改变)
⑷①答案一:B 通过转基因技术,一是抑制正常植株A基因的表达,二是使A基因在矮生植株过量表达。C 测定两个实验组植株的赤霉素含量和株高。(答案二:B 通过转基因技术,使A基因在矮生植株过量表达,测定其赤霉素的含量和株高。C 通过转基因技术,抑制正常植株A基因的表达,测定其赤霉素的含量和株高。注:B和C次序不作要求)。②与对照比较,正常植株在A基因表达被抑制后,赤霉素的含量降低,株高降低;与对照比较,A基因在矮生植株过量表达后,该植株赤霉素的含量增加,株高增加。
某研究性学习小组在做氯气的喷泉实验时(装置如图),发现含有酚酞的NaOH溶液喷入烧瓶后,溶液的红色褪去。
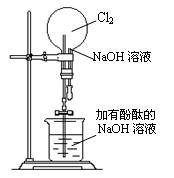
甲、乙两位同学对此现象分别做了如下推测:
甲:因为氯气与NaOH溶液反应,使溶液碱性减弱甚至呈酸性,所以溶液红色褪去。
乙:因为氯气溶于水并与水反应生成HClO,由于HClO的氧化漂白作用而使溶液褪色。
(1)验证甲同学的推测是否正确的方法是:______________;
验证乙同学的推测是否正确的方法是:_______________。
(2)如果将NaOH溶液改成酸性KMnO4溶液,把Cl2换成SO2气体,试问用图示所给的装置完成喷泉实验是否合理?_______(填“合理”或“不合理”)。如果认为不合理,请说明你的理由_____________________________________________________。
(3)类似“褪色喷泉实验”的还有多种“变色喷泉实验”,请你按实验要求分别设计2个“变色喷泉实验”并填写下列表格:
| 实验要求 | 烧杯中的溶液 | 滴管中的液体 | 烧瓶中的气体 | |
| ① | 无色变红色喷泉 | H2O | ||
| ② | 红色变无色喷泉 | SO2 |
(2)某学生判断SO2和Na2O2反应能生成硫酸钠,你认为他的判断合理吗?(填“合理”或“不合理”)__________。简要说明理由___________________________________________。
(3)该同学无法确定反应中是否有氧气生成,拟用如下图所示装置进行实验。
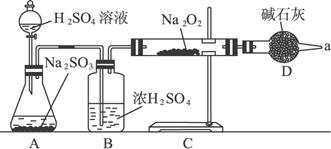
装置B的作用是_________________________________________________。D的作用是:________________________________________。
(4)为确认反应产物,请完成下表中所列实验
操作 | 现象与结论 |
①确认是否有氧气产生的操作是: |
|
②确认是否有硫酸钠产生的操作是: |
|
某同学设计如图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:
(1)如何检验如图所示装置的气密性: 。
(2)该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行? (填“可行”或“不可行”),原因是 。
(3)实验Ⅲ烧瓶中发生反应的化学方程式是 ,打开开关K,产生的气体经验纯后点燃,现象是 。
(4)实验Ⅱ中量气管中的液体最好是____(填字母编号,下同)
a.浓NaOH溶液 b.氨水 c.煤油 d.饱和氯化铵溶液
该实验剩余的NH3需吸收处理。以下各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有
(5)本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,② ,③视线与凹液面最低处相平。
(6)实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
| 编号 | 镁铝合金质量 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 1.0g | 10.0mL | 346.3mL |
| ② | 1.0g | 10.0mL | 335.0mL |
| ③ | 1.0g | 10.0mL | 345.7mL |
根据上述数据,可计算出镁铝合金中铝的质量分数为__ 。
查看习题详情和答案>>
某同学设计如图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:

(1)如何检验如图所示装置的气密性: 。
(2)该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行? (填“可行”或“不可行”),原因是 。
(3)实验Ⅲ烧瓶中发生反应的化学方程式是 ,打开开关K,产生的气体经验纯后点燃,现象是 。
(4)实验Ⅱ中量气管中的液体最好是____(填字母编号,下同)
a.浓NaOH溶液 b.氨水 c.煤油 d.饱和氯化铵溶液
该实验剩余的NH3需吸收处理。以下各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有

(5)本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,② ,③视线与凹液面最低处相平。
(6)实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
|
编号 |
镁铝合金质量 |
量气管第一次读数 |
量气管第二次读数 |
|
① |
1.0g |
10.0mL |
346.3mL |
|
② |
1.0g |
10.0mL |
335.0mL |
|
③ |
1.0g |
10.0mL |
345.7mL |
根据上述数据,可计算出镁铝合金中铝的质量分数为__ 。
查看习题详情和答案>>
(2)某学生判断SO2和Na2O2反应能生成硫酸钠,你认为他的判断合理吗?___________。简要说明理由_________________________________________________________________。
(3)该同学无法断定SO2和Na2O2反应中是否有氧气生成,拟用下列装置进行实验。
(已知:Na2SO3+2H2SO4![]() Na2SO4+H2O+SO2↑)
Na2SO4+H2O+SO2↑)
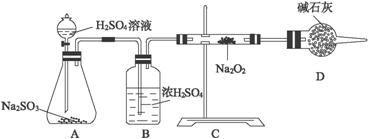
装置B的作用是__________________________________________________________。
D的作用是____________________________________________________________。
(4)为确认SO2和Na2O2的反应产物,该同学设计了以下实验步骤,请你从中挑选出正确的选项并按操作顺序排列(填序号)_______________。
A.用带火星的木条靠近干燥管口,观察木条是否复燃
B.用C装置中反应后的固体物质溶于适量水配成溶液
C.在配成的溶液中加入用硝酸酸化的硝酸钡溶液,观察是否有沉淀生成
D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀生成
查看习题详情和答案>>