网址:http://m.1010jiajiao.com/timu_id_3207938[举报]
硫酸工业在国民经济中占有极其重要的地位。
(1)硫酸的最大消费渠道是化肥工业,用硫酸制造的常见化肥有________________(任写一种)。
(2)硫酸生产中,根据化学平衡原理来确定的条件或措施有________________(填写序号)。
A.矿石加入沸腾炉之前先粉碎
B.使用V2O5作催化剂
C.转化器中使用适宜的温度
D.净化后的炉气中要有过量的空气
E.催化氧化在常压下进行
F.吸收塔中用98.3%的浓硫酸吸收SO3
(3)在硫酸工业中,通过下列反应使二氧化硫转化为三氧化硫:
2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-98.3 kJ·mol-1
2SO3(g) ΔH=-98.3 kJ·mol-1
在实际工业生产中,常采用“二转二吸法”,即将第一次转化生成的SO2分离后,将未转化的SO2进行二次转化,假若两次SO2的转化率均为95%,则最终SO2的转化率为___________。
(4)硫酸的工业制法过程涉及三个主要的化学反应及相应的设备(沸腾炉、转化器、吸收塔)。
①三个设备分别使反应物之间或冷热气体间进行了“对流”。请简单描述吸收塔中反应物之间是怎样对流的。
_____________________________________________________________。
②工业生产中常用氨—酸法进行尾气脱硫,以达到消除污染、废物利用的目的。用化学方程式表示其反应原理。(只写出2个方程式即可)
_____________________________________________________________________。
查看习题详情和答案>>
CO(g)+2H2(g)?CH3OH(g).
(1)图1是反应时CO和CH3OH(g)的浓度随时间变化情况.从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=
(2)图2表示该反应进行过程中能量的变化.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.该反应是
(3)该反应平衡常数K的表达式为
| c(CH3OH) |
| c(CO)×c2(H2) |
| c(CH3OH) |
| c(CO)×c2(H2) |
(4)恒容条件下,下列措施中能使
| n(CH3OH) |
| n(CO) |
a.升高温度; b.充入He气 c.再充入1molCO和2molH2 d.使用催化剂.
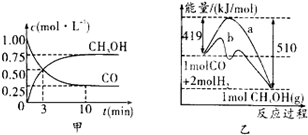
CO(g)+2H2(g) CH3OH(g).
(1)图甲是反应时CO(g)和CH3OH(g)的浓度随时间的变化情况.从反应开始到平衡,用CO浓度变化表示的平均反应速率v(CO)=
a.改变反应的热效应 b.降低生产能耗
c.加快反应速率 d.提高反应物的转化率
(3)在2L密闭容器中发生反应CO(g)+2H2(g) CH3OH(g),若T℃时,加入2mol CH3OH,反应达到平衡后,生成CO1 mol,此时向容器中同时加入2molCH3OH和4 mol的H2混合气体(保持温度不变),则平衡将
(4)恒容条件下,下列措施中能使n(CH3OH)/n(CO)增大的有
a.升高温度 b.使用催化剂 c.再充入2molH2 d.再充入1molCO.
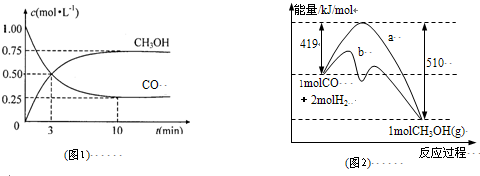
(1)图1是反应时CO和CH3OH(g)的浓度随时间变化情况.从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=
(2)图2表示该反应进行过程中能量的变化.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.该反应是
(3)该反应平衡常数K的表达式为
| c(CH3OH) |
| c(CO)×c2(H2) |
| c(CH3OH) |
| c(CO)×c2(H2) |
(4)恒容条件下,下列措施中能使
| n(CH3OH) |
| n(CO) |
a.升高温度; b.充入He气 c.再充入1molCO和2molH2 d.使用催化剂
II.(13分)某化学课外活动小组设计实验探究氮的化合物的性质,装置如下图所示(A装置未画出),其中A为气体发生装置.A中所用试剂从下列固体物质中选取:a.NH4HCO3、b.NH4Cl、c.Ca(OH)2、d.NaOH.
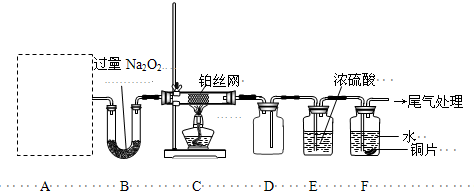
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯.部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解.
(1)实验室制取A中气体时若只用一种试剂,该试剂是
(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:
(3)对于C中发生的可逆反应,下列说法正确的是
a.增大一种反应物的浓度可以提高另一种反应物的转化率
b.工业上进行该反应时,可采取高压的条件提高反应物转化率
c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
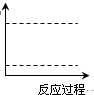
(4)请在图坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式.
(5)待实验结束后,将B中固体混合物溶于500mL1mol?L-1 盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是
工业上用CO生产燃料甲醇。一定条件下发生反应:
CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。

(1)该反应的平衡常数表达式为:K=
(2)图1是反应时CO和CH3OH(g)的浓度随时间的变化情况。从反应开始到平衡,用CO浓度变化表示的平均反应速率v(CO)= 。
(3)适宜的催化剂能 (选填序号)。
a.改变反应的热效应 b.降低生产能耗 c.加快反应速率
d.提高反应物的转化率
(4)在2 L密闭容器中发生反应 CO(g)+2H2(g) ![]() CH3OH(g) 若T℃时,加入2mol CH3OH,反应达平衡后,生成CO 1 mol,此时向容器中同时加入2 mol的CH3OH和4mol的H2混合气体(保持温度不变),则平衡将 (填“向正反应方向”、“向逆反应方向”或“不”)移动,达到新平衡后平衡常数K的值为
CH3OH(g) 若T℃时,加入2mol CH3OH,反应达平衡后,生成CO 1 mol,此时向容器中同时加入2 mol的CH3OH和4mol的H2混合气体(保持温度不变),则平衡将 (填“向正反应方向”、“向逆反应方向”或“不”)移动,达到新平衡后平衡常数K的值为
(5)恒容条件下,下列措施中能使n (CH3OH)/n (CO)增大的有 (选填序号)。
a. 升高温度 b. 使用催化剂 c.再充入2mol H2 d.再充入1mol CO
(6)甲醇可与氧气构成燃料电池,该电池用多孔的惰性电极浸入浓氢氧化钾溶液,写出该电池的负极反应式___________________
查看习题详情和答案>>