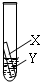摘要:(2)甲同学认为通过实验①和③可比较锌和铁的金属活动性.他依据的实验现象是 .(3)乙同学认为上述实验方案不足以得出四种金属的活动性顺序.并 在上述实验的基础上.补充了一个实验.实现了探究目的.则:乙同学的实验:X是金属 .Y是 溶液,
网址:http://m.1010jiajiao.com/timu_id_320508[举报]
一、选择题(本题包括15小题,每小题2分,共30分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
答案
A
C
A
C
D
B
C
B
D
B
D
C
B
A
C
二、选择题(本题共5小题,每小题2分,共10分)若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给1分,选两个且都正确的给2分,但只要选错一个,该小题就为0分。
题号
16
17
18
19
20
答案
B
C
AC
CD
BC
三、(本题共7小题,每空1分,共31分)
21.E C B A
22.(1)蛋白质 锌 (2)不要高温加热 食醋
(3)甲醛(一氧化碳、黄曲霉毒素等)
23.(1)⑤④①②③
(2)3┱1 化合
24.(1)B (2)Na + Na2O (3)MgS
(4)原子的电子层数等于周期数(其他合理答案也给分)


 ,CaCO3的质量:35g-15g=20g。样品中钙元素、碳元素和氧元素的质量比:
,CaCO3的质量:35g-15g=20g。样品中钙元素、碳元素和氧元素的质量比:
 某学习小组的三位同学为测定镀锌铁皮的锌镀层的厚度,提出了各自的设计方案.(忽略锌镀层的氧化)
某学习小组的三位同学为测定镀锌铁皮的锌镀层的厚度,提出了各自的设计方案.(忽略锌镀层的氧化)
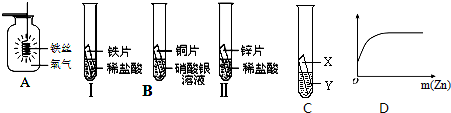
 在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)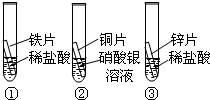 在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:
在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验: