网址:http://m.1010jiajiao.com/timu_id_295354[举报]
(物理部分67分) 2009.3
一、单选题:(每小题2分,共20分)13―17:ADBBD 18―22:CCBCC
二、填空及简答题:(每空1分,共17分)
23、10.0(左右) 2.8 2.8×103 24、 (1) 力的方向 (2)电路中的总功率过大 (3)重力作用 (4)小猴分得多,根据杠杆平衡条件,粗的一端力臂小,所以粗的一端重力大 25、= 液体不流动时,连通器内液面相平 > b管下端细,此处流速大,压强小 26、 5 1.2 83.3% 5 27、 ①液体密度 ②物体排开液体的体积(重力)
三、实验探究题:(每空1分,图1分,共17分)
32、 B 从A到B 图略 33、二力平衡 2.8 没有控制压力保持不变 34、 150 117 倒出盐水的体积V/ml 30 1.1×103
35、(一) (1)电压表正负接线柱接反了 电压表指针反偏 (2) B (3)电流表指针偏转较小,误差较大,应选小量程 (4) 10 (二) 小亮
四、计算应用题:(第39小题7分,第40小题6分,共13分)
39、解:(1)电 ----(1分) 机械----(1分)
(2)v=s/t=
(3)∵P=W/t ∴W=Pt=100W×1800s=1.8×105J
∵W=Fs ∴F=W/s=1.8×105J/9×
∵匀速 ∴ F=f=20N ----(1分)
W总=UIt=32V×
(4)η=W有/W总=1.8×105J/230400J=78%----(1分)
40、解:(1)开关接1,R1 、R2 串联
∴U1= U- U2=9 V―3 V=6 V ----(1分)
∴I1 =U1/R1=6V/6Ω=
∴R2= U2/ I2= 3 V/
∴Q2=
U2I2t=3 V×
(2)开关接2,L 、R2 串联
L正常 UL= U- U2〃=9 V―6 V=3V ----(1分)
I2〃 =U2〃/R2=6V/3Ω=
2009年第一次模拟检测理科综合参考答案
(化学部分53分) 2009.3
一、单选题:(每小题2分,共24分)1―5:CADCC 6―12:BDACBBC
二、填空及简答题:(每空1分,共14分)
28、(1)⑥ (2)⑤ (3)③
29、(1) NaCl (2)+1 (3)H2SO4+Ca(OH)2=CaSO4+2H2O
30、(1)加入C物质或升高温度 (2)a (3)150
(4)16.7%
31、(1)CO (2)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
(3)Cu+2AgNO3=Cu(NO3)2+2Ag 置换反应
三、实验探究题:(每空1分,共10分)
36、(1)B (2)只有水或只有氧气的情况下,铁钉的生锈情况
(3)铜绿中含有C元素 (4)除去空气中的CO2
氧气、水和二氧化碳
37、加Ca(OH)2 研磨,有刺激性气味 1.没有OH-1 2.CO32-
3.有白色沉淀 NH4Cl
四、计算应用题:(第38小题5分)
38、解:(1)得出产生
(2)化学方程式 ----(1分)
比例式 ----(1分)
得出含
得出硫酸的质量分数19.6% ----(1分)
完全正确,格式有问题减1分。
(2)用上述配制的稀硫酸与一定量的氢氧化钾溶液混合,完全反应后溶液呈中性,求生成的硫酸钾为多少克?
(已知反应的化学方程式:H2SO4+2KOH═K2SO4+2H2O) 查看习题详情和答案>>
(1)将10g溶质的质量分数为98%的浓硫酸稀释为质量分数10%的稀硫酸,稀释后溶液的质量为多少克?稀释所需的水为多少毫升?(水的密度为1.0g?cm-3)
(2)用上述配制的稀硫酸与一定量的氢氧化钾溶液混合,完全反应后溶液呈中性,求生成的硫酸钾为多少克?
(已知反应的化学方程式:H2SO4+2KOH═K2SO4+2H2O)
查看习题详情和答案>>
(2)用上述配制的稀硫酸与一定量的氢氧化钾溶液混合,完全反应后溶液呈中性,求生成的硫酸钾为多少克?
(已知反应的化学方程式:H2SO4+2KOH═K2SO4+2H2O)
硫酸是柳州市的一种重要工业产品,下图是工业采用接触法生产硫酸的工艺流程图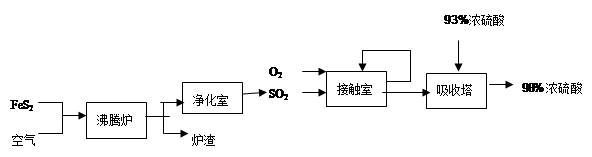 (1)从硫酸厂的生产流程中不难发现,吸收塔中SO2不可能是100%吸收,所以尾气必须处理,否则含大量SO2的尾气会造成环境的污染,最大的危害是形成 ;为了减少这种污染,对此生产流程可采取的措施是 (选填下列做法的序号)。
(1)从硫酸厂的生产流程中不难发现,吸收塔中SO2不可能是100%吸收,所以尾气必须处理,否则含大量SO2的尾气会造成环境的污染,最大的危害是形成 ;为了减少这种污染,对此生产流程可采取的措施是 (选填下列做法的序号)。
①杜绝用煤做燃料;②把工厂的烟囱加高;③用烧碱溶液吸收后再排放;
④开发新能源; ⑤研究经济高效的回收SO 2的技术。
(2)沸腾炉中发生的主要反应是4FeS2+11O2高温2R +8SO2,推断炉渣的主要成分R的化学式是
(3)为了提高硫铁矿(主要成份是FeS2)的利用率,在工业生产中,需要将硫铁矿粉碎后再进行生产的原因是什么?
(4)写出接触室发生的反应的化学方程式并指出其所属的基本反应类型(3分)
(5)为了提高硫酸的利用率,吸收塔选用93%的浓硫酸来吸收,写出吸收塔内发生的反应的化学方程式
(6)若将100g质量分数为98%的浓硫酸稀释为10%的稀硫酸需加水 g。
(7)浓硫酸具有强烈腐蚀性,生产时每个工人必须严格按照规程进行操作,如果不慎将少量的浓硫酸沾到皮肤或衣服上,你的处理方法是什么?