摘要:设降温至t1时.析出的晶体的质量为x根据公式:100+S-S=高温下饱和溶液质量∶析出晶体质量=∶xx=250g[评价]对学生讨论的情况进行小结.充分肯定学生的正确回答.激励学生积极思考和回答问题.学生回答问题后归纳出:某温度下.饱和溶液的溶质质量分数可直接由溶解度的数据所推出的公式进行计算.因为某温度下.用100g水配制饱和溶液所需溶质的质量等于该温度下溶质的溶解度.而该温度下用100g水所配制的饱和溶液的溶质质量分数和用任意质量的水配制成的饱和溶液的溶质质量分数相等.[指导练习]A.B两种化合物的溶解度曲线如图1-4.要用结晶法从A.B混合物中提取A(不考虑A.B共存时.对各自溶解度的影响).(1)取50g混合物将它溶于100g热水.然后冷却至20℃.若要使A析出.B不析出.则混合物中B的质量分数(B%)最高不超过多少?(2)取Wg混合物.将它溶于100g热水.然后冷却至10℃.若仍要使A析出B不析出.请写出下列两种情况下.混合物中A的质量分数(A%)应满足什么关系式.当W<a+b时.A% .当W>a+b时.A% .
网址:http://m.1010jiajiao.com/timu_id_287080[举报]
摩尔质量为Mg·mol-1的某物质(不含结晶水)的溶解度曲线如下图,现有t2℃ 300 g该物质的溶液,蒸发掉50 g水后,恢复到原温度,溶液恰好达到饱和,此饱和溶液的密度为ρg·mL-1,则下列说法不正确的是?

A.该饱和溶液的质量分数为:![]()
B.该饱和溶液的物质的量浓度为:![]() mol·L-1??
mol·L-1??
C.将该饱和溶液降温至t1 ℃时,析出的晶体的质量为:![]() ?
?
D.原溶液的质量分数为:![]()
右图是几种盐的溶解度曲线,下列说法正确是
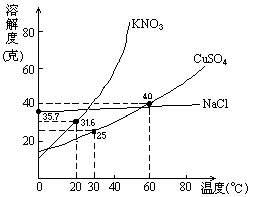 (A)40℃时,将35克食盐溶于100克水中,降温至0℃时,可析出氯化钠晶体
(A)40℃时,将35克食盐溶于100克水中,降温至0℃时,可析出氯化钠晶体
(B)20℃时,硝酸钾饱和溶液的质量百分比浓度是31.6%
(C)60℃时,200克水中溶解80克硫酸铜达饱和.当降温至30℃时,可析出30克硫酸铜晶体
(D)30℃时,将35克硝酸钾和35克食盐同时溶于100克水中, 蒸发时,先析出的是氯化钠
 (2013?天河区一模)海水晒盐能够得到粗盐和卤水.卤水中含有MgCl2、KCl和MgSO4等物质,如图是它们的溶解度曲线.完成下列填空.
(2013?天河区一模)海水晒盐能够得到粗盐和卤水.卤水中含有MgCl2、KCl和MgSO4等物质,如图是它们的溶解度曲线.完成下列填空.(1)在t1℃时,向100g水中加入150g MgCl2,形成
饱和
饱和
(填“饱和”或“不饱和”)溶液,将其温度升高到t2℃时,此时溶液中溶质的质量分数为50%
50%
.(2)t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是
MgCl2
MgCl2
.将t2℃时MgCl2、KCl和MgSO4三种物质的饱和溶液降温至t1℃时,可能会析出的晶体有C
C
(填字母序号).A.MgCl2和KCl
B.只有MgSO4
C.MgCl2、KCl和MgSO4.
海水晒盐能够得到粗盐和卤水.卤水中含有MgCl2、KCl和MgSO4等物质,如图是它们的溶解度曲线.完成下列填空.
(1)在t1℃时,向100g水中加入150g MgCl2,形成______(填“饱和”或“不饱和”)溶液,将其温度升高到t2℃时,此时溶液中溶质的质量分数为______.
(2)t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是______.将t2℃时MgCl2、KCl和MgSO4三种物质的饱和溶液降温至t1℃时,可能会析出的晶体有______(填字母序号).
A.MgCl2和KCl
B.只有MgSO4
C.MgCl2、KCl和MgSO4.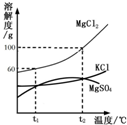
查看习题详情和答案>>
(1)在t1℃时,向100g水中加入150g MgCl2,形成______(填“饱和”或“不饱和”)溶液,将其温度升高到t2℃时,此时溶液中溶质的质量分数为______.
(2)t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是______.将t2℃时MgCl2、KCl和MgSO4三种物质的饱和溶液降温至t1℃时,可能会析出的晶体有______(填字母序号).
A.MgCl2和KCl
B.只有MgSO4
C.MgCl2、KCl和MgSO4.

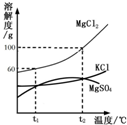 海水晒盐能够得到粗盐和卤水.卤水中含有MgCl2、KCl和MgSO4等物质,如图是它们的溶解度曲线.完成下列填空.
海水晒盐能够得到粗盐和卤水.卤水中含有MgCl2、KCl和MgSO4等物质,如图是它们的溶解度曲线.完成下列填空.