摘要:12.8 10
网址:http://m.1010jiajiao.com/timu_id_285426[举报]
10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH
(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言
查看习题详情和答案>>
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
HCO3-+H2O?H2CO3+OH-
HCO3-+H2O?H2CO3+OH-
.乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于
大于
(填“大于”或“小于”)NaHCO3.丙同学认为甲、乙的判断都不充分.丙认为:(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则
乙
乙
(填“甲”或“乙”)判断正确.试剂X是B
B
.A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH
等于
等于
(填“高于”、“低于”或“等于”)8.3,则甲
甲
(填“甲”或“乙”)判断正确.(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言
乙
乙
(填“甲”或“乙”)判断是错误的.10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
甲同学认为,该溶液的pH升高的原因是HCO
水解程度增大,故碱性增强,该反应的离子方程式为
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度
丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH
(3)查阅资料发现NaHCO3的分解温度为150℃,丙断言
查看习题详情和答案>>
| 温度/℃ | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
- 3 |
HCO3-+H2O?H2CO3+OH-
HCO3-+H2O?H2CO3+OH-
.乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度
大于
大于
NaHCO3(填“大于”或“小于”).丙同学认为甲、乙的判断都不充分.丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则
乙
乙
(填“甲”或“乙”)判断正确.试剂X是B
B
(填选项).A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH
等于
等于
8.3(填“大于”“小于”或“等于”),则甲
甲
(填“甲”或“乙”)判断正确.(3)查阅资料发现NaHCO3的分解温度为150℃,丙断言
乙
乙
(填“甲”或“乙”)判断是错误的,理由是碳酸氢钠的分解温度是150℃,常压下加热NaHCO3的水溶液,溶液的温度达不到150℃,所以碳酸氢钠不分解
碳酸氢钠的分解温度是150℃,常压下加热NaHCO3的水溶液,溶液的温度达不到150℃,所以碳酸氢钠不分解
.10℃时加热NaHCO3饱和溶液,测得该溶液的PH发生如下变化:
甲认为,该溶液的PH升高的原因是HCO3-离子的水解程度增大,所以碱性增强,该反应的离子方程式为
(1)只要在加热煮沸的溶液中加入足量的试剂X,如果产生白色沉淀,则
A.氢氧化钡溶液 B.氯化钡溶液 C.氢氧化钠溶液 D.澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的PH等于8.3,则
(3)查阅资料发现,NaHCO3的分解温度为150℃,丙断言
查看习题详情和答案>>
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| PH | 8.3 | 8.4 | 8.5 | 8.8 |
HCO3-+H2O?H2CO3+OH-
HCO3-+H2O?H2CO3+OH-
;乙认为,溶液PH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于
大于
(填“大于”或“小于”) NaHCO3.丙认为甲、乙的判断都不准确,丙认为:(1)只要在加热煮沸的溶液中加入足量的试剂X,如果产生白色沉淀,则
乙
乙
(填“甲”或“乙”)判断正确,该试剂是B
B
(填编号)A.氢氧化钡溶液 B.氯化钡溶液 C.氢氧化钠溶液 D.澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的PH等于8.3,则
甲
甲
(填“甲”或“乙”).(3)查阅资料发现,NaHCO3的分解温度为150℃,丙断言
乙
乙
(填“甲”或“乙”)的判断是错误的,理由是常压下加热NaHCO3的水溶液,溶液的温度达不到150℃
常压下加热NaHCO3的水溶液,溶液的温度达不到150℃
.10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
甲同学认为,该溶液的pH值升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为 .
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度 (填“大于”或“小于”)NaHCO3.
丙同学认为甲、乙的判断都不充分.丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则 (填“甲”或“乙”)判断正确.试剂X是 .A、Ba(OH)2溶液 B、BaCl2溶液 C、NaOH溶液 D、澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH (填“高于”、“低于”或“等于”)8.3,则 (填“甲”或“乙”)判断正确.
(3)常温下,在测得PH都等于9的NaOH溶液和Na2CO3溶液中,由水电离的OH-浓度分别为amol/L和bmol/L,则a与b的关系: .
查看习题详情和答案>>
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度
丙同学认为甲、乙的判断都不充分.丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则
(2)将加热后的溶液冷却到10℃,若溶液的pH
(3)常温下,在测得PH都等于9的NaOH溶液和Na2CO3溶液中,由水电离的OH-浓度分别为amol/L和bmol/L,则a与b的关系:
10℃时,在烧杯中加入0.1mol/L的NaHCO3溶液400mL,加热,测得该溶液的PH发生如下变化:
(1)甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为: ;
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度 (填“大于”或“小于”)NaHCO3;
(3)丙同学认为,要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液pH,若pH 8.3(填“>”、“<”或“=”),说明乙正确;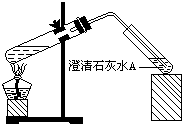
(4)丁同学设计如下实验方案对甲、乙同学的解释进行判断:实验装置如图,加热煮沸NaHCO3溶液,发现试管A中产生沉淀,说明 (填“甲”或“乙”)推断正确;
(5)将一定体积0.1mol/L的NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为10.4;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为9.5.据此资料可以判断 (填“甲”或“乙”)推测正确,原因是 .
查看习题详情和答案>>
| 温度(℃) | 10 | 20 | 30 | 40 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度
(3)丙同学认为,要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液pH,若pH

(4)丁同学设计如下实验方案对甲、乙同学的解释进行判断:实验装置如图,加热煮沸NaHCO3溶液,发现试管A中产生沉淀,说明
(5)将一定体积0.1mol/L的NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为10.4;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为9.5.据此资料可以判断