摘要:
网址:http://m.1010jiajiao.com/timu_id_284026[举报]


从分类角度看,金属可分为黑色金属和有色金属.铁是日常生活中最常见的黑色金属,请回答下列问题:
问题1:铁为何称为黑色金属?
(1)同学们经百度查询,得到以下两种解释,你认为下列解释正确的是
A.因为铁表面上有黑色的铁的氧化物,所以叫黑色金属.
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属.
(2)已知某黑色粉末为铁和四氧化三铁的混合物.请定性证明其中含有Fe3O4(只要求简述实验方法)?
(3)将适量FeO粉末溶于过量稀硫酸中,并将所得溶液分为两份.一份溶液加入少量硝酸钾晶体,发现溶液颜色发生改变,此反应的离子方程式为
问题2:已知CuO在高温时可分解为Cu2O和O2,为探究Fe2O3高温灼烧时是否分解为FeO和O2,同学们设想了两种探究方法:
C.看灼烧前后固体颜色是否变化. D.看灼烧前后固体质量改变情况.
(4)实验时应将Fe2O3放在
(5)方法C中,如果高温灼烧后固体颜色发生明显改变,说明Fe2O3发生了变化.能否说明产物一定为FeO?
(6)方法D中,测得实验结果是固体灼烧前后的质量比为30:29,则高温灼烧后固体生成物是
查看习题详情和答案>>
问题1:铁为何称为黑色金属?
(1)同学们经百度查询,得到以下两种解释,你认为下列解释正确的是
A
A
.(填字母)A.因为铁表面上有黑色的铁的氧化物,所以叫黑色金属.
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属.
(2)已知某黑色粉末为铁和四氧化三铁的混合物.请定性证明其中含有Fe3O4(只要求简述实验方法)?
用干燥的氢气与黑色粉末加热反应,用无水硫酸铜检测显蓝色或用纯净的CO与黑色粉末加热反应,用澄清石灰水检验有白色沉淀生成,说明其中含有Fe3O4
用干燥的氢气与黑色粉末加热反应,用无水硫酸铜检测显蓝色或用纯净的CO与黑色粉末加热反应,用澄清石灰水检验有白色沉淀生成,说明其中含有Fe3O4
.(3)将适量FeO粉末溶于过量稀硫酸中,并将所得溶液分为两份.一份溶液加入少量硝酸钾晶体,发现溶液颜色发生改变,此反应的离子方程式为
3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
,另一份溶液加入一定量氢氧化钠溶液,所见主要实验现象为产生白色絮状沉淀,并迅速变成灰绿色,最后变成红褐色
产生白色絮状沉淀,并迅速变成灰绿色,最后变成红褐色
.问题2:已知CuO在高温时可分解为Cu2O和O2,为探究Fe2O3高温灼烧时是否分解为FeO和O2,同学们设想了两种探究方法:
C.看灼烧前后固体颜色是否变化. D.看灼烧前后固体质量改变情况.
(4)实验时应将Fe2O3放在
坩埚
坩埚
中灼烧.(填仪器名称)(5)方法C中,如果高温灼烧后固体颜色发生明显改变,说明Fe2O3发生了变化.能否说明产物一定为FeO?
不能
不能
,(填“能”或“不能”)理由是Fe3O4也是黑色的
Fe3O4也是黑色的
.(6)方法D中,测得实验结果是固体灼烧前后的质量比为30:29,则高温灼烧后固体生成物是
Fe3O4
Fe3O4
.从分类角度看,金属可分为黑色金属和有色金属.铁是日常生活中最常见的黑色金属,请回答下列问题:
问题1:铁为何称为黑色金属?
(1)同学们经百度查询,得到以下两种解释,你认为下列解释正确的是______.(填字母)
A.因为铁表面上有黑色的铁的氧化物,所以叫黑色金属.
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属.
(2)已知某黑色粉末为铁和四氧化三铁的混合物.请定性证明其中含有Fe3O4(只要求简述实验方法)?______.
(3)将适量FeO粉末溶于过量稀硫酸中,并将所得溶液分为两份.一份溶液加入少量硝酸钾晶体,发现溶液颜色发生改变,此反应的离子方程式为______,另一份溶液加入一定量氢氧化钠溶液,所见主要实验现象为______.
问题2:已知CuO在高温时可分解为Cu2O和O2,为探究Fe2O3高温灼烧时是否分解为FeO和O2,同学们设想了两种探究方法:
C.看灼烧前后固体颜色是否变化. D.看灼烧前后固体质量改变情况.
(4)实验时应将Fe2O3放在______中灼烧.(填仪器名称)
(5)方法C中,如果高温灼烧后固体颜色发生明显改变,说明Fe2O3发生了变化.能否说明产物一定为FeO?______,(填“能”或“不能”)理由是______.
(6)方法D中,测得实验结果是固体灼烧前后的质量比为30:29,则高温灼烧后固体生成物是______.
查看习题详情和答案>>
从分类角度看,金属可分为黑色金属和有色金属.铁是日常生活中最常见的黑色金属,请回答下列问题:
问题1:铁为何称为黑色金属?
(1)同学们经百度查询,得到以下两种解释,你认为下列解释正确的是______.(填字母)
A.因为铁表面上有黑色的铁的氧化物,所以叫黑色金属.
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属.
(2)已知某黑色粉末为铁和四氧化三铁的混合物.请定性证明其中含有Fe3O4(只要求简述实验方法)?______.
(3)将适量FeO粉末溶于过量稀硫酸中,并将所得溶液分为两份.一份溶液加入少量硝酸钾晶体,发现溶液颜色发生改变,此反应的离子方程式为______,另一份溶液加入一定量氢氧化钠溶液,所见主要实验现象为______.
问题2:已知CuO在高温时可分解为Cu2O和O2,为探究Fe2O3高温灼烧时是否分解为FeO和O2,同学们设想了两种探究方法:
C.看灼烧前后固体颜色是否变化. D.看灼烧前后固体质量改变情况.
(4)实验时应将Fe2O3放在______中灼烧.(填仪器名称)
(5)方法C中,如果高温灼烧后固体颜色发生明显改变,说明Fe2O3发生了变化.能否说明产物一定为FeO?______,(填“能”或“不能”)理由是______.
(6)方法D中,测得实验结果是固体灼烧前后的质量比为30:29,则高温灼烧后固体生成物是______.
查看习题详情和答案>>
问题1:铁为何称为黑色金属?
(1)同学们经百度查询,得到以下两种解释,你认为下列解释正确的是______.(填字母)
A.因为铁表面上有黑色的铁的氧化物,所以叫黑色金属.
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属.
(2)已知某黑色粉末为铁和四氧化三铁的混合物.请定性证明其中含有Fe3O4(只要求简述实验方法)?______.
(3)将适量FeO粉末溶于过量稀硫酸中,并将所得溶液分为两份.一份溶液加入少量硝酸钾晶体,发现溶液颜色发生改变,此反应的离子方程式为______,另一份溶液加入一定量氢氧化钠溶液,所见主要实验现象为______.
问题2:已知CuO在高温时可分解为Cu2O和O2,为探究Fe2O3高温灼烧时是否分解为FeO和O2,同学们设想了两种探究方法:
C.看灼烧前后固体颜色是否变化. D.看灼烧前后固体质量改变情况.
(4)实验时应将Fe2O3放在______中灼烧.(填仪器名称)
(5)方法C中,如果高温灼烧后固体颜色发生明显改变,说明Fe2O3发生了变化.能否说明产物一定为FeO?______,(填“能”或“不能”)理由是______.
(6)方法D中,测得实验结果是固体灼烧前后的质量比为30:29,则高温灼烧后固体生成物是______.
从分类角度看,金属可分为黑色金属和有色金属.铁是日常生活中最常见的黑色金属,请回答下列问题:
问题1:铁为何称为黑色金属?
(1)同学们经百度查询,得到以下两种解释,你认为下列解释正确的是 .(填字母)
A.因为铁表面上有黑色的铁的氧化物,所以叫黑色金属.
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属.
(2)已知某黑色粉末为铁和四氧化三铁的混合物.请定性证明其中含有Fe3O4(只要求简述实验方法)? .
(3)将适量FeO粉末溶于过量稀硫酸中,并将所得溶液分为两份.一份溶液加入少量硝酸钾晶体,发现溶液颜色发生改变,此反应的离子方程式为 ,另一份溶液加入一定量氢氧化钠溶液,所见主要实验现象为 .
问题2:已知CuO在高温时可分解为Cu2O和O2,为探究Fe2O3高温灼烧时是否分解为FeO和O2,同学们设想了两种探究方法:
C.看灼烧前后固体颜色是否变化. D.看灼烧前后固体质量改变情况.
(4)实验时应将Fe2O3放在 中灼烧.(填仪器名称)
(5)方法C中,如果高温灼烧后固体颜色发生明显改变,说明Fe2O3发生了变化.能否说明产物一定为FeO? ,(填“能”或“不能”)理由是 .
(6)方法D中,测得实验结果是固体灼烧前后的质量比为30:29,则高温灼烧后固体生成物是 . 查看习题详情和答案>>
问题1:铁为何称为黑色金属?
(1)同学们经百度查询,得到以下两种解释,你认为下列解释正确的是 .(填字母)
A.因为铁表面上有黑色的铁的氧化物,所以叫黑色金属.
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属.
(2)已知某黑色粉末为铁和四氧化三铁的混合物.请定性证明其中含有Fe3O4(只要求简述实验方法)? .
(3)将适量FeO粉末溶于过量稀硫酸中,并将所得溶液分为两份.一份溶液加入少量硝酸钾晶体,发现溶液颜色发生改变,此反应的离子方程式为 ,另一份溶液加入一定量氢氧化钠溶液,所见主要实验现象为 .
问题2:已知CuO在高温时可分解为Cu2O和O2,为探究Fe2O3高温灼烧时是否分解为FeO和O2,同学们设想了两种探究方法:
C.看灼烧前后固体颜色是否变化. D.看灼烧前后固体质量改变情况.
(4)实验时应将Fe2O3放在 中灼烧.(填仪器名称)
(5)方法C中,如果高温灼烧后固体颜色发生明显改变,说明Fe2O3发生了变化.能否说明产物一定为FeO? ,(填“能”或“不能”)理由是 .
(6)方法D中,测得实验结果是固体灼烧前后的质量比为30:29,则高温灼烧后固体生成物是 . 查看习题详情和答案>>
(2013?兰州一模)[化学--选修3 物质结构与性质]
Ni、Fe是重要的金属,它们的单质及化合物在科学研究和工业生产中具有许多用途.
(1)基态Ni原子电子排布式为
(2)第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是
A.离子键 B.极性键 C.金属键
D.配位键 E.氢键 F.非极性键
(3)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂.固态Ni(CO)4属于
CO与N2结构相似,CO分子内σ键与π键个数之比为
(4)Ni2+和Fe2+的半径分别为69pm和78pm,则熔点NiO
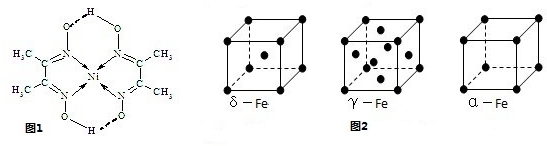
(5)铁有δ、γ、α三种同素异形体(图2),γ、α两种晶胞中铁原子的配位数之比为
cm(设NA为阿伏伽德罗常数,用含ρ和NA的代数式表示).
查看习题详情和答案>>
Ni、Fe是重要的金属,它们的单质及化合物在科学研究和工业生产中具有许多用途.
(1)基态Ni原子电子排布式为
1s22s22p63s23p63d84s2
1s22s22p63s23p63d84s2
;(2)第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是
C
C
.Ni的一种配合物的分子结构如图1所示,该配合物中C原子的杂化轨道类型是sp3、sp2
sp3、sp2
,配合物分子内不含有AC
AC
(填序号).A.离子键 B.极性键 C.金属键
D.配位键 E.氢键 F.非极性键
(3)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂.固态Ni(CO)4属于
分子
分子
晶体.配合物Ni(CO)4中CO与N2结构相似,CO分子内σ键与π键个数之比为
1:2
1:2
;(4)Ni2+和Fe2+的半径分别为69pm和78pm,则熔点NiO
>
>
FeO(填“<”或“>”);(5)铁有δ、γ、α三种同素异形体(图2),γ、α两种晶胞中铁原子的配位数之比为
2:1
2:1
.若δ晶体的密度为ρg?cm-3,该晶胞棱长为| 3 |
| ||
| 3 |
| ||
